高二化学学业水平测试模拟考试(三)
化 学 试 题 2008.3.31
(考试时间 75分钟 ; 总分 100分)
本卷可能用到的相对原子质量 H:1 O:16 Na:23 Mg:24 S:32 Fe:56
 一、单项选择题:在每题的四个选项中,只有一个选项是符合要求的(本大题17题,每题3分,共51分)。
一、单项选择题:在每题的四个选项中,只有一个选项是符合要求的(本大题17题,每题3分,共51分)。
1.2008年北京奥运会火炬以中国传统祥云符号和纸卷轴为创意,由铝合
金制成,使用的燃料为丙烷。下列说法不正确的是
A.丙烷与甲烷互为同系物 B.丙烷燃烧是吸热反应
C.铝柄有一层致密的氧化膜可防止其腐蚀
D.火炬燃料用丙烷比用煤油更环保
2.水作为生命之液哺育着人类和万千生物。下列有关水的说法中不正确的是
A.用太阳能蒸馏海水是海水淡化的方法之一
B.提倡全社会节约用水,合理使用水资源
C.水厂常同时使用硫酸亚铁和氯气处理水,既可杀菌消毒,又可除去水中悬浮杂质
D.在化学反应中水只能作还原剂
3.“善待地球――科学发展。”下列行为中不符合这一主题的是
A.发展循环经济,构建资源节约型社会
B.大量砍伐森林,以满足人们对木材的需求
C.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
D.采用“绿色化学”工艺,建立环境友好型化工体系
4.石油是一种不可再生能源,2008年1月2日纽约市场原油期货价格一度突破每桶100美元的关口。下列有关石油的说法中不正确的是
A.石油被称为“工业的血液”
B.衡量一个国家石油化工工业水平发展的标志是乙烯的产量
C.石油的主要成分与植物油相同
D.在海洋里航行的油轮发生泄漏时,会对海洋产生严重的污染
5.钢筋、水泥和沙石是重要的建筑材料,有关说法不正确的是
A.铁合金是目前使用量最大的金属材料 B.制造水泥的主要原料是石灰石和黏土
C.沙子的主要成分是SiO2 D.铁是地壳中含量最多的金属元素
6.食品级NH4HCO3可用作膨松剂以使面粉为原料制作的糕点松软可口。这是因为NH4HCO3
①热稳定性差 ②增加甜味 ③分解产生气体 ④提供NH4+
A.②③ B.①③ C.①④ D.③④
7.下列分离混合物的操作中,必须加热的是
A. 过滤 B.蒸馏 C.分液 D.萃取
8.下列做法存在安全隐患的是
A.将水沿烧杯内壁缓缓加入浓硫酸中,并用玻璃棒不断搅拌
B.取用金属Na或K时,用剩的药品要放回原瓶
C.厨房发生煤气泄漏时,应关闭阀门并检查煤气泄漏原因
D.废旧电池回收处理
![]() 9.我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为2KNO3+S+3C K2S+N2↑+3CO2↑。该反应中被还原的元素是
9.我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为2KNO3+S+3C K2S+N2↑+3CO2↑。该反应中被还原的元素是
A.N B.C C.N和S D.N和C
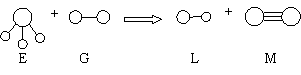 10.已知E是氨分子,它和双原子分子G反应,生成两种双原子分子L和M(组成E、G的各元素原子序数均小于10)如下图所示。则下列判断错误的是
10.已知E是氨分子,它和双原子分子G反应,生成两种双原子分子L和M(组成E、G的各元素原子序数均小于10)如下图所示。则下列判断错误的是
A.该反应属于复分解反应 B.G是最活泼的非金属单质
C.E能使紫色石蕊试液变蓝色 D.M气体约占空气体积的![]()
11.下列关于有机物的说法正确的是
A.甲烷易发生加成反应 B.常温下乙烯易发生取代反应
C.乙酸乙酯是高分子化合物 D.乙醇催化氧化可生成乙醛
12.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、K+、OH-、Cl- B.Na+、Cu2+、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl- D.Ba2+、HCO3-、NO3-、K+
13.德国科学家格哈德・埃特尔因在“固体表面化学过程”研究中作出的贡献获得2007年度诺贝尔化学奖。表面化学对于化学工业很重要,有助于了解诸如钢铁为什么生锈、燃料电池如何工作、汽车尾气处理时催化剂的工作原理等。下列涉及该研究的项目中,说法正确的是
A.纯铁比生铁更易生锈
B.硝酸工业中,NH3和O2在铂催化剂表面生成NO和H2O
C.氢氧燃料电池中,燃料在正极失去电子被氧化
D.臭氧层的破坏主要与CO2排放有关
14.下列离子方程式书写不正确的是
A.铜与稀硝酸反应:Cu+2H+=Cu2++H2↑
B.FeCl3溶液中加入铁粉:2Fe3++Fe=3Fe2+
C.常温下氯气与烧碱溶液反应:Cl2+2OH-=Cl-+ClO-+H2O
D.Ca(NO3)2溶液中滴加少量的K2CO3溶液:Ca2++CO32-=CaCO3↓
15.已知N2(g)+3H2(g)![]() 2NH3(g)。现向一密闭容器中充入1molN2和3molH2,在一定条件下使该反应发生。下列有关说法正确的是
2NH3(g)。现向一密闭容器中充入1molN2和3molH2,在一定条件下使该反应发生。下列有关说法正确的是
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,正反应和逆反应的速率都为零
C.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
D.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
16.设NA表示阿伏加德罗常数,下列叙述错误的是
A.2.4g金属镁变为镁离子时失去的电子数为0.2NA
B.在标准状况下,22.4 L H2O含有水分子的个数为NA
C.16 g臭氧(O3)中含有氧原子的个数为NA
D.1 L 1 mol/L NaCl溶液中含有钠离子的个数为NA
17.某原子的最外电子层上只有1个电子,则它跟氯结合能形成的化学键是
A.一定是共价键 B.一定是离子键
C.可能是共价键,也可能是离子键 D.以上说法均不正确
二、单项选择题:在每题的四个选项中,只有一个选项是符合要求的(本大题包括“A.化学与生活”和“B.有机化学基础”两个模块各6题,每题3分,每个模块18分。每位考生只可选择其中的一个模块作答)。
A.化学与生活
18.治理太湖污染是我省目前重要的环保工程,措施之一是在太湖流域推广使用无磷洗衣粉。下列有关说法正确的是
A.磷促进水中动植物尸体的分解 B.磷是营养元素,促进鱼类大量繁殖
C.磷促进水体富营养化,导致水体缺氧 D.磷是有毒物质,能杀死水中的动植物
19.下列做法正确的是
A.为使火腿肠颜色更鲜红,多加一些亚硝酸钠
B.为增加婴儿对食品的兴趣,在婴儿食品中尽量多添加合成着色剂
C.烧鱼时放点醋,可软化鱼骨
D.味精的主要成分为蛋白质,烧菜时可加入适量
20.长期吸食或注射毒品会危及人体健康。下列各组物质中都属于毒品的是
A.冰毒、黄连素 B.味精、麻黄碱 C.纤维素、尼古丁 D.大麻、摇头丸
21.下列事实不能用电化学理论解释的是
A.镀锌铁比镀锡铁更耐用B.铝制品不需要采用特殊方法保护
C.轮船吃水线以下的船壳上装有一定数量的锌块
D.钢铁在潮湿空气中比在干燥空气中腐蚀的快
![]() 22.某物质的结构简式为:
,下列有关该物质的说法不正确的是
22.某物质的结构简式为:
,下列有关该物质的说法不正确的是
A.分子式为C5H10O2N2 B.在一定条件下能发生脱水反应
C.是由一种氨基酸形成的二肽 D.既能和酸反应又能和碱反应
23.糖类、油脂、蛋白质和维生素是食物中常见的有机物。下列有关说法中正确的是( )
A.糖类、油脂、蛋白质都属碱性食物 B.蛋白质在人体中发生水解的产物是葡萄糖
C.油脂只有在碱性条件下才能水解
D.维生素C能防治坏血病,且溶液显酸性,故又称为抗坏血酸
B.有机化学基础
18.有关CH3CHCl2的说法正确的是
A.可由氯乙烯与HCl加成得到 B.不存在同分异构体
C.可由乙烯与Cl2加成得到 D.一定不能发生水解
19.下列有机物分子中,所有原子均在同一平面上的是
A.环丙烷 B.甲苯 C.甲烷 D.苯
20.欲将蛋白质从水中析出而又不改变它的性质,可加入的物质是
A.饱和硫酸钠溶液 B.甲醛溶液 C.硫酸铜溶液 D.浓硝酸
21.橡胶是重要的工业原料,生胶的弹性好但强度较差;硫化后强度增大但弹性减弱,硫化程度越高,强度越大、弹性越差。下列橡胶制品中,硫化程度最高的是
A.气球 B.橡皮筋 C.汽车外胎 D.医用乳胶手套
22.下列操作中,不正确的是
A.苯酚沾在手上应立即用酒精洗涤
B.燃着的酒精灯打翻起火,应用水扑灭
C.石油分馏、制乙烯时均需在反应器中加入少量碎瓷片
![]() D.点燃甲烷、乙烯等可燃性气体前必须先检验其纯度
D.点燃甲烷、乙烯等可燃性气体前必须先检验其纯度
23.咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为 。下列关于咖啡酸的说法中,正确的是
A.属于芳香烃 B.分子式为C9H7O2
C.不能使酸性KMnO4溶液褪色 D.能与FeCl3溶液发生显色反应
三、本大题包括2题,共10分。每题分为A题和B题,每位考生只可选做一题。选学《化学与生活》模块的考生答A题,选做《有机化学基础》模块的考生答B题。
24.(5分)
A.人体所需要的营养素主要有糖、油脂、 、无机盐、维生素和水。根据维生素的溶解性,一般可把它们分为水溶性和 两大类。糖尿病患者的血液中葡萄糖的浓度很高,其中大部分的去向是 。将过量的维生素C溶液滴入碘水中,反应后单质碘转化为 ,为证明该反应的发生,常用试剂 检验。
B.(4分)下列各组物质:①O2和O3 ②H2、D2和T2 ③12C和14C
④CH3CH2CH2CH3和(CH3)2CHCH3 ⑤乙烯和丁烯
⑥CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5
用序号填空:
⑴互为同系物的是 ; ⑵互为同分异构体的是 ;
⑶互为同位素的是 ; ⑷互为同素异形体的是 。
25.(5分)
A.化学兴趣小组查阅资料得知:甲醛是一种无色有刺激性气味的气体,沸点为-19.5oC,易溶于水,易被高锰酸钾氧化生成其他气体。大多数装修材料中含有甲醛。请回答下列问题:
(1)甲醛对人的皮肤和 有强烈的刺激作用。
(2)CO使人中毒是因为很容易和人体血液中的 结合。
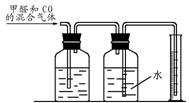
(3)该兴趣小组收集V1 L含有甲醛和CO的某居室空气,用下图装置测定其中甲醛和CO的含量。则装置A中盛放的试剂是 ,实验中还需要测定的数据是 。为了获得较准确的实验结论,他们需要采取的方法是 (填序号)。
a. 仔细做好每步操作,只做一次实验
b. 在A、B间加一个干燥装置
c. 重复做2~3次上述实验
 |
A B C
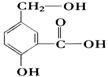
B.(6分)有机物A的分子中具有酚羟基、醇羟基、羧基等官能团,其结构如上图所示。
⑴A不可能具有的性质是____________________(填写序号);
①能与NaOH溶液反应 ②能发生消去反应
③能与溴水发生取代反应 ④能与冰醋酸发生酯化反应
⑵A跟NaHCO3溶液反应的化学方程式是______________________________________;
⑶A在一定条件下跟Na反应的化学方程式是___________________________________。
四、本大题3题,共21分。
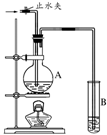
26.(5分)在下图所示的实验装置中,A中盛有品红溶液,B 中盛有NaOH溶液。
 请回答下列问题:
请回答下列问题:
(1) 若向A中通入足量的二氧化硫气体,A中的现象是 。
(2) 若向A中通入足量的氯气后,再加热A,A中的溶液
(填“能”或“不能”)恢复到原来的颜色。
(3) 如果A中盛的是氨水,B中盛的是无色酚酞溶液,微热,B中
溶液会变为红色,则此时表现氨水的化学性质有碱性和 性。
(4) 如果A中盛的是浓硫酸,加入铜,加热反应,此反应中表现浓硫酸的酸性和 性。
(5) 如果A中盛的是盐酸,加入铜粉,为了让铜粉溶解,可以加入NaNO3,反应离子方
程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,请用单线桥标出其电子转移的方向和数目。
27.(6分)下图中A~H均为中学化学中常见的物质,它们之间有如下转化关系。其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应。(反应过程中生成的水及其他产物已略去)
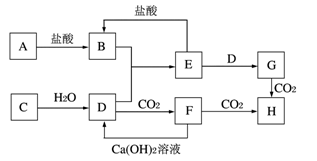
请回答以下问题:
(1)B是_________,H是_________。(填化学式)
(2)写出E转化为G的离子方程式____________。
(3)A在常温下也可与NaOH溶液反应生成G,写出此反应的化学方程式 _______。
28.(10分)化学学习小组为测定某补血剂中硫酸亚铁的含量进行了以下探究:
【查阅资料】本品为糖衣片,除去糖衣后显淡蓝绿色,主要成分硫酸亚铁(FeSO4・7H2O)。
【实验步骤】取本品10片,在适当的条件下配成100mL溶液,分别准确量取20mL溶液,用下列两种方法进行实验:
方法一、用一定物质的量浓度的酸性高锰酸钾溶液滴定。(高锰酸钾被还原为+2价的锰)
方法二、加过量H2O2溶液,然后再加入过量NaOH溶液,得红褐色沉淀,将沉淀过滤并充分加热得红棕色固体,称量该固体的质量。
请回答下列问题:
(1)方法一中,配制一定物质的量浓度的酸性高锰酸钾溶液时,所需要的玻璃仪器除量筒、玻璃棒、胶头滴管、烧杯外还有 。
(2)方法二中,加过量H2O2溶液的目的是 。有的同学认为使用氯气也能达到此目的,和使用氯气相比,用H2O2溶液的好处是 。
(3)在方法一中,若每消耗1mL酸性高锰酸钾溶液相当于0.152 g FeSO4,则该溶液中高锰酸钾的物质的量浓度是 。在方法二中,若称得红棕色固体的质量为a g,则每片补血剂含FeSO4 g。