高二化学上学期五校重点高中联考期末试题
(新课标选修4)
命题人:孙丽丽(13中学) 考试时间:90分钟 考试分值:100分
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。试题共四大页,30题,
满分值:100分,考试时间:90分钟。考生只交第Ⅰ卷的答题卡和第Ⅱ卷的答题纸。
参考相对原子量:H:1 Na:23 Mg:24 Al:27 Fe:56 K:39 Cu:64 Ag:108 C:12 O:16 S:32 Cl:35.5
第Ⅰ卷 选择题(共50分)
一、选择题(每小题只有一个正确选项,每题2分,共50分)
1、改变下列一个条件,通过提高活化分子的百分率来提高反应速率的是
A.加热 B.加压 C.加负催化剂 D.加大反应物浓度
2、用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A.加热 B.不用稀硫酸,改用98%浓硫酸
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
3、下列变化的熵变大于零的是
![]()
![]() A.H2O(l) H2O(g) B.CO2(g) CO2(s)
A.H2O(l) H2O(g) B.CO2(g) CO2(s)
C.NaOH(aq)+HCl(aq) = NaCl(aq)+H2O D.NH3(g)+HCl(g)=NH4Cl(s)
4、在一定温度下的定容密闭容器中,当下列物理量不再改变时,不能表明反应
A(s)+2B(g)![]() C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.混合气体的相对分子质量 D.C气体的总物质的量浓度
5、已知反应X+Y= M+N为放热反应,,对该反应的下列说法中正确的
A、X的能量一定高于M
B、Y的能量一定高于N
C、X和Y的总能量一定高于M和N的总能量
D、因该反应为放热反应,故不必加热就可发生
6、下列事实不能用勒夏特列原理解释的是
A.将氯化铁溶液加热蒸干最终得不到氯化铁固体
B.钢铁在潮湿的空气中容易生锈
C.温度过高对合成氨不利
D.常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5
7、在一支25mL的酸式滴定管中盛入0.1mol/L HCl溶液,其液面恰好在5mL刻度处。若把滴定管内溶液全部放入烧杯中,再用0.1mol/L NaOH溶液进行中和,则所需NaOH溶液的体积 为
A.大于20mL B.小于20mL C.等于20mL D.等于5mL
8、强酸和强碱在稀溶液中的中和热可表示为:
H+(aq)+OH-(aq)=H2O(l); △H= -57.3 kJ·mol-1,又知在溶液中反应有:
CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l); △H=-Q1kJ·mol-1,
H2SO4(浓)+NaOH(aq)=Na2SO4(aq)+H2O(l)
; △H= -Q2 kJ·mol-1
HNO3(aq)+KOH(aq)![]() KNO3(aq)+H2O(l) ; △H= -Q3 kJ·mol-1,
KNO3(aq)+H2O(l) ; △H= -Q3 kJ·mol-1,
则Q1、Q2、Q3的关系正确的是 ( )
A. Q1 = Q2 = Q3 B.Q2 > Q1 > Q3 C. Q2 > Q3 > Q1 D. Q2 = Q3 > Q1
9、为了除去MgCl2酸性溶性中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸.这种试剂是
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
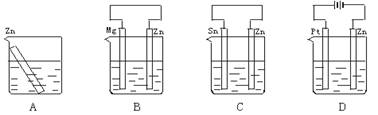
10、分别放置在下图所示装置(都盛有0.1 mol·L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是
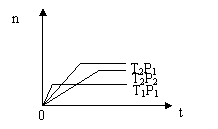 11、反应2X(g)+Y(g)
11、反应2X(g)+Y(g)![]() 2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
A.T1<T2,P1<P2
B.T1<T2,P1>P2
C.T1>T2,P1>P2
D.T1>T2,P1<P2
12、若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是 Cu + 2H+ ===Cu2+ + H2 ↑,则下列关于该装置的有关说法正确的是
A.该装置可能是原电池,也可能是电解池
B.该装置只能是原电池,且电解质溶液为硝酸
C.该装置只能是电解池,且金属铜为该电解池的阳极
D.该装置只能是原电池,电解质溶液不可能是盐酸
![]()
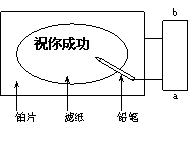 13、某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
13、某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
![]() A.铅笔端作阳极,发生还原反应
A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是电源的负极,b点是电源的正极
14、已知NaHSO4在水中的电离方程式为:NaHSO4===Na++H++SO![]() 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,
不正确的是
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
15、一定条件下反应N2+3H2![]() 2NH3达平衡,当单独改变下述条件后有关叙述一定错误的是
A.加催化剂,v(正)和v(逆)都发生变化,且变化的倍数相等
2NH3达平衡,当单独改变下述条件后有关叙述一定错误的是
A.加催化剂,v(正)和v(逆)都发生变化,且变化的倍数相等
B.加压,v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数
C.降温,v(正)和v(逆)都减少,且v(正)减少倍数大于v(逆)减少倍数
D.增加c(N2),v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数
16、常温,某溶液中由水电离产生的c(H+)、c(OH-)满足c(H+)·c(OH—)=10—24,则下列各组离子在该溶液中一定可以大量共存的是
A.K+、Na+、AlO2—、Cl— B.Na+、Cl—、SO42—、HCO3—
C.NH4+、Na+、NO3—、SO42— D.Ba2+、Na+、Cl—、NO3—
17、用0.01mol/L的NaOH溶液完全中和pH=3的下列溶液各100mL。需要NaOH溶液的体积最大的是
A、盐酸 B、硫酸 C、高氯酸 D、醋酸
18、汽车的启动电源常用铅蓄电池,电池反应如下:
![]() PbO2 + Pb + 2H2SO4 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是
PbO2 + Pb + 2H2SO4 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是
A.PbO2放电时是电池的负极,充电时是电池的阳极。
B.负极的电极反应式为:Pb + SO![]() – 2e – = PbSO4
– 2e – = PbSO4
C.放电时,PbO2得电子,被氧化
D.电池放电时,溶液酸性增强
19、已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1 mol/L-1的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中一定正确的是
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C.c(RO32-)+c(HRO3-)+c(H2RO3)=c(Na+)
D.两溶液中c(Na+)、c(HRO3-)、c(RO32-)分别相等
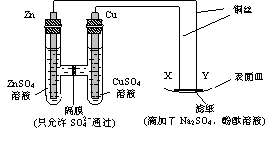 20、如图所示,下列叙述正确的是
20、如图所示,下列叙述正确的是
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X与滤纸接触处变红
21、常温下,现有PH=2的某酸HX溶液和PH=12某碱YOH溶液,两溶液混合后,溶液的pH小于7。下表中判断合理的是
| 编号 | HX | YOH | 溶液的体积关系 |
| A | 强酸 | 强碱 | V(HX)=V(YOH) |
| B | 强酸 | 强碱 | V(HX)<V(YOH) |
| C | 强酸 | 弱碱 | V(HX)=V(YOH) |
| D | 弱酸 | 强碱 | V(HX)=V(YOH) |
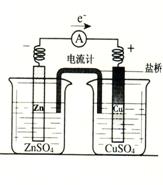
22、有关如右图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)
A.反应中,盐桥中的K+会移向CuSO4溶液
B.取出盐桥后,电流计依然发生偏转
C.铜片上有气泡逸出
D.反应前后铜片质量不改变
23、金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍。(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是
A.阳极发生还原反应,其电极反应式:Ni2++2e-===Ni
B.电解过程中,阳极质量减少与阴极质量增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
24、一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的容器中,发生反应:2SO2+O2 ![]() 2SO3,平衡时SO3为n
mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
2SO3,平衡时SO3为n
mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
A.2 mol SO2 + 1 mol O2
B.1mol SO2 + 1 mol O2
C.2 mol SO2 + 1 mol O2 + 2 mol SO3
D.1 mol SO2 + 1 mol SO3
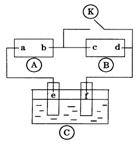 25、下图
25、下图![]() 为直流电源,
为直流电源,![]() 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,![]() 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现![]() 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通![]() 后,使c、d两点短路.下列叙述正确的是
后,使c、d两点短路.下列叙述正确的是
A.a为直流电源的负极
B.c极发生的反应为2H++2e-=H2↑
C.f电极为锌板
D.e极发生还原反应
第Ⅱ部分 非选择题 (共50分)
二、填空题:
26、(1)(3分)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
_________________
(2)、(3分)已知:AgCl+Br-=AgBr↓+Cl-,2AgI+S2-=Ag2S↓+2I-,AgBr+I-=AgI↓+Br-。由以上实验事实可知4种难溶银盐溶解度减小的顺序是 。
(3)、(4分)用碳棒作电极,电解下列水溶液:
①Na2SO4溶液 ②AgNO3溶液 ③KCl溶液 ④CuCl2溶液。(填编号)
A、通过相同电量时,阴极产生的气体的物质的量相同的是___________ __。
B、通过相同电量时,产生的气体总的物质的量由多到少排列顺序是___ ___。
27、(8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
28、(12分)某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL稀H2SO4溶液;以0.14mol/L的NaOH溶液滴定上述稀H2SO425mL,滴定终止时消耗NaOH溶液15mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写): 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终点? 。
(2)分析下列操作的结果:(填“偏小”、“偏大”或“恰好合适”)
碱式滴定管用蒸馏水润洗后,未用标准液润洗,导致滴定结果 。
碱式滴定管滴定前读数时仰视,结束时读数平视,导致滴定结果 。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度 mol/L。
(计算出结果到小数点后二位)
29、(6分)现有0.1mol/L的纯碱溶液,回答下列问题:
(1)常温下,甲同学用pH试纸检验该溶液,发现其pH﹥7,你认为原因是什么?(用离子方程式表示)
(2)常温下,乙同学向该溶液中滴入几滴酚酞溶液,发现该溶液遇到酚酞呈红色。对该现象的分析,你认为能得到的结论是:该溶液呈 性。
对为什么遇到酚酞该溶液呈现出红色的原因问题,同学们展开了讨论,乙同学认为,是在配制标准碳酸钠溶液时混入了NaOH所致,而丙同学则认为,是碳酸钠溶液水解所致。
请你设计一个简单的实验方案,来评判上述观点。(要求必须写出操作、现象和结论)
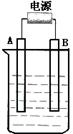 30、(14分)在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成。请回答下列问题:
30、(14分)在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成。请回答下列问题:
(1)请写出B极板的名称及反应式: 。
(2)写出电解时反应的总离子方程式
。
(3)若当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。电解后溶液的pH为 ;要使电解后溶液恢复到电解前的状态,则需加入 ,其质量为 g。(假设电解前后溶液的体积不变)
(4)若原溶液为1L K2SO4、CuSO4的混合溶液,且c(SO42-)= 2.0mol/L ;如图装置电解,当两极都收集到22.4L气体(标准状况)时,停止电解。
则原溶液中的c(K+)为 多少?(请简单表示计算过程,4分)