高二年级化学学业水平测试第一次模拟考试
试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷第1至第2页,第Ⅱ卷第2至第3页,满分100分。考试用时75分钟。
可能用到的原子量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 Ba 137
第Ⅰ卷(选择题 共69分)
一、第1-16小题所有考生必做,每小题3分,共48分。
1.下列关于2311Na的叙述,错误的是 ( C )
A.质子数是11 B.电子数为11 C.中子数是11 D.质量数是23
2.能够将溶液和胶体区分开的方法是 ( C )
A.过滤 B.观察颜色、状态 C.利用丁达尔效应 D.闻气味
3.某元素最高价氧化物对应水化物的化学式是H2XO4,这种元素的气态氢化物的化学式为
(B)
A.HX B.H2X C.XH3 D.XH4
4.能够用于鉴别SO2和CO2的溶液是 ( B )
A.石蕊试液 B.品红溶液 C.澄清石灰水 D.氯化钡溶液
5.在下列说法中,正确的是 ( A )
A.Cl2有毒而Cl—无毒 B.Cl2的液化属于化学变化
C.Cl比Cl—的结构稳定 D.氯水中没有含氧化合物
6.在下列物质中,化学键类型相同的一组是 ( A )
A.CO2和H2O B.NaCl和HCl C.CCl4和KCl D.MgCl2和SO2
7.在元素周期表中,非金属性最强的元素是 ( D )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
8.在强酸性溶液中能大量共存的无色透明的离子组是 ( C )
A.Al3+、Cu2+、NO3—、Cl— B.Na+、NO3—、SO42—、CO32—
C.Mg2+、NH4+、SO42—、Cl— D.Ba2+、K+、OH—、Cl—
9.下列说法正确的是 ( C )
A.1H、2H、3H互为同素异形体 B.O2、O3互为同位素
C.正丁烷和异丁烷互为同分异构体 D.乙烷、乙烯互为同系物
10.在下列有关实验的叙述中,正确的是 ( B )
A.用烧杯或烧瓶给液态物质加热时,不用垫石棉网
B.用乙醇和乙酸做原料可以制得乙酸乙酯
C.在用托盘天平称量固体药品时,药品直接放在右盘上
D.如果未知溶液中滴加BaCl2溶液有白色沉淀生成,证明原溶液中一定含有SO42—离子
11.在下列溶液中,c(Cl—)与150mL 1mol/LAlCl3溶液中的c(Cl—)相等的是 ( B )
A.150mL 3mol/L的CaCl2溶液 B.75mL l.5mol/L的MgCl2溶液
C.50mL l mol/L的FeCl2溶液 D.225mL 2mol/L的NH4Cl溶液
12.能正确表示下列化学反应的离子方程式是 ( A )
A.碳酸钙与盐酸反应:CaCO3+2H+==Ca2++CO2↑+H2O
![]() B.铜片与浓硝酸反应:Cu+NO3—+4H+==Cu2++NO↑+2H2O
B.铜片与浓硝酸反应:Cu+NO3—+4H+==Cu2++NO↑+2H2O
C.二氧化锰与浓盐酸反应:MnO2+4HCl==Mn2++2Cl—+Cl2↑+2H2O
D.硫酸铜与氢氧化钡反应:Ba2++SO42—==BaSO4↓
13.在下列三个反应中,过氧化氢(H2O2)所起的作用是 ( D )
|
A.均起氧化剂作用 B.均起还原剂作用 C.相同作用 D.起不同作用
14.下列事实可以说明甲烷分子具有正四面体结构的是 ( C )
A.CH4 没有同分异构体 B.CH3Cl没有同分异构体
C.CH2Cl2没有同分异构体 D.CCl4 没有同分异构体
15. 下列关于烃的说法中,正确的是 ( D )
A.烃是指分子里含有碳、氢元素的化合物 B.烃是指分子里含碳元素的化合物
C.烃是指燃烧反应后生成二氧化碳和水的有机物 D.烃是指仅由碳和氢两种元素组成的化合物
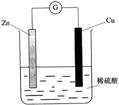 16.下列关于如右图所示的原电池的有关说法中,正确的是
( D )
16.下列关于如右图所示的原电池的有关说法中,正确的是
( D )
A.![]() 是负极,发生还原反应 B.
是负极,发生还原反应 B.![]() 是负极,发生氧化反应
是负极,发生氧化反应
C.锌片上有气体逸出 D.电子由锌片通过导线流向铜片
二、第17-23小题,选修《化学与生活》的考生必做,每小题3分,共21分。
17.下列食物属碱性食物的是 ( D )
A.面包 B.葡萄 C.大米 D.鸡蛋
18.下列关于合金的说法,正确的是 ( D )
A.合金不能导电、传热 B.合金属于纯净物
C.合金没有延展性 D.合金的很多性能与组成它们的纯金属不同
19.下列关于药物的使用说法正确的是 ( A )
A.虽然药物能治病,但大部份药物有毒副作用 B.青霉素有解热镇痛的作用
C.阿司匹林是最重要的抗生素
D.随着药物的普及,生病了都可以到药店自己买药吃,不用到医院
20.人体中因缺少或过多会患甲状腺疾病的元素是 ( D )
A.Na B.Cl C.F e D.I
21.小明家里收藏了一件清代的铝制佛像,该佛像至今仍保存十分完好.该佛像未锈蚀的主要原因是( D )
A.铝不易发生化学反应 B.铝的氧化物容易发生还原反应
C.铝不易被氧化 D.铝易氧化,但氧化铝具有保护内部铝的作用
22. 误食重金属盐而引起的中毒,急救方法是 ( C )
A、服用大量生理盐水 B、服用大量冷开水 C、服用大量的豆浆或牛奶 D、服用大量小苏打溶液
23.废电池必须集中处理的首要原因是 ( C )
A.不使电池渗泄的电解液腐蚀其他物品 B.回收其中的石墨电极
C.防止电池中汞、镉、铬、铅等重金属元素形成的有毒化合物对土壤和水源的污染
D.回收其中的各种金属及塑料包装等
三、第24-30小题,选修《有机化学》的考生必做,每小题3分,共21分。
24.下列物质中属于天然高分子化合物的是 ( C )
A.油脂 B.蔗糖 C.纤维素 D.麦芽糖
25.居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料会释放出一种刺激性气味的气体,该气体是 ( C )
A.甲烷 B.氨气 C.甲醛 D.二氧化硫
26. 下列有机物分子中,所有原子均在同一平面上的是 ( B )
A.环丙烷 B.苯 C.甲烷 D.甲苯
27.已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如下图苯的二氯取代物C6H4Cl2有三种,则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为 (C )
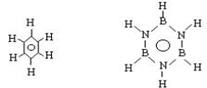
A.2 B.3 C.4 D.6
28 .下列有机物中刚滴入NaOH溶液会出现分层现象,然后用水浴加热分层现象逐渐消失的是 ( A )
A.油脂 B.苯 C.己烯 D.乙酸
29 .阿司匹林是一种常见药物,它的相对分子质量为180,含C、H、O三种元素,其中含C、H的质量分数分别为60℅、4.5℅,所以阿司匹林的分子式 ( A )
A、C10H9O4 B、C10H22O3 C、C9H10O4 D、C9H8O4
30.丙烯醛的结构简式为CH2=CH-CHO,结合所学知识推测该物质不能发生的反应是 ( C )
A.加成反应 B.聚合反应 C.酯化反应 D.氧化反应
第Ⅱ卷(非选择题 共31分)
注意事项:
1.第Ⅱ卷共2页,用钢笔或圆珠笔直接答在试卷上。 2.答卷前将密封线内的项目填写清楚。
四、第31-32小题,选修《化学与生活》的考生必做,每空1分,共9分。
|
|
|
A B C
32.⑴下表是某食品包装袋上的说明,从表中的配料中分别选出一种物质填在相应的横线上
| 品 名 | ××× |
| 配 料 | 鲜鸡蛋、精面粉、白砂糖、精炼植物油、奶油、奶粉、食盐、柠檬汁等 |
| 保 质 期 | 240天 |
| 生产日期 | 标于包装袋封口上 |
①富含蛋白质的物质是_________________;②富含糖类的物质是__________________;
③富含油脂的物质是___________________;④富含维生素的物质是________________。
⑵阅读下列材料后回答问题:
|
① 在人体中进行Fe2+![]() Fe3+的转化时,①中的Fe2+作 剂,②中的Fe3+作 剂;
Fe3+的转化时,①中的Fe2+作 剂,②中的Fe3+作 剂;
②“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作 剂
③市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐。此反应的化学方程式为 。
五、第33-34题,选修《有机化学》的考生必做,每空1分,共9分。
33.(4分)化合物A是一种酯,它的分子式为C4H8O2,有下图转化关系。试回答下列问题。
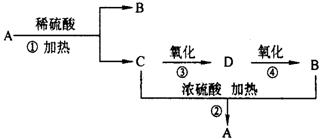
(1)A的名称是 (2)B的结构简式是 。
(3)D中含有的官能团(填名称)是 。
(4)在图中①~④的反应中,属于取代反应的有 。
34.(5分)根据以下所示有机物的结构特点判断以下各项是否正确(对的画√,错的画×)。
![]()
(1)该有机物属于烃的衍生物: ; (2)该有机物不能发生酯化反应: ;
(3)该有机物不能跟NaOH反应: ; (4)该有机物能发生银镜反应: ;
(5)该有机物可以和Cl2反应: 。
六、第35-37题,所有考生必做,共22分。
35.(5分)下图是铜与浓硫酸反应的实验装置图,请回答下列问题。
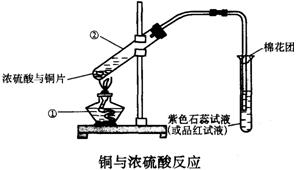
(1)写出有标号仪器的名称:① ;② 。
(2)写出铜与浓硫酸反应的化学方程式: 。
(3)SO2通入品红试液中的现象为 。
(4) SO2和NO2都是大气污染物,它们会引起雨水呈 (填“酸性”、“碱性”、“中性”)。
36.(8分)A、B、C三种元素的原子具有相同的电子层数,且都是短周期元素。已知A是一种金属元素,A原子的最外层电子数为1,它跟酸反应后转化成的A+具有跟Ne相同的电子层结构。B的质子数比A多2个,C的质子数比B多4个。
根据以上条件,填空回答:
(1)C是 元素(写元素名称),画出C原子结构示意图: 。
(2)B元素在周期表中的位置是第 周期,第 族。
(3)C元素的气态氢化物的水溶液呈 (填“酸性”、“碱性”、“中性”)。
(4) A与C形成的化合物的电子式: 。
(5)B元素的最高价氧化物对应的水化物与C元素的气态氢化物的水溶液之间发生的化学反应方程式: 。
37.(9分) 取100mLNa2CO3和Na2SO4的混合液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀硝酸处理后沉淀质量减少到4.66g,并有气体放出。试计算:
求:①原混合物中Na2CO3和Na2SO4的物质的量浓度。 ②产生的气体在标准状况下的体积。
客观题参考答案:
31.鲜鸡蛋、奶油、奶粉 精面粉、白砂糖
精炼植物油 柠檬汁
32.① 还原剂 氧化剂
② 还原剂
③ Fe+2H+=Fe2++H2↑
33.(1)乙酸已酯 (2) CH3COOH
(3) 醛基 (4)①②
34.⑴√ ⑵× ⑶× ⑷√ ⑸√
35.⑴①酒精灯 ②试管 ⑵Cu+2H2SO4==CuSO4+SO2↑+2H2O(加热条件)
⑶品红试液褪色
⑷酸性