高中会考化学模拟卷(4)
蔡肖雄 三门二高
可能要用到的相对原子质量:H—1 C—12 N—14 O—16 A1—27 Fe—56
试 卷 I
一、选择题 (每小题2分,共56分)每小题只有1个选项符合题意.
1、日常生活中的问题常常与化学有关,下列说法正确的是 ( )
A.绿色食品是指不含任何化学物质的食品
B.喝纯净水肯定比喝白开水更有利于人体健康
C.棉花、蚕丝、羊毛主要成分都是纤维素
D.室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染空气
2、下列物质中,属于强电解质的是 ( )
A.NaOH B.CH3COOH C.H2O D.CO2
3、下列物质的物质的量最大的是 ( )
A.1 gH2 B.11 gCO2 C.8 gO2 D.4.5 gH2O
4、下列物质中,属于纯净物的是 ( )
A.汽油 B.福尔马林 C.乙酸乙酯 D.食醋
5、既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是 ( )
A.Fe B.Mg C.Al D.Cu
6、既有氧化性又有还原性的微粒是 ( )
A.H+ B.Fe C.Cu2+ D.N2
7、下列溶液呈碱性的是 ( )
A.NH4Cl B.CH3COONa C.NaCl D.FeCl3
8、下列各仪器中,有零刻度的仪器的是 ( )
A.容量瓶 B.量筒 C.滴定管 D.烧杯
9、氯化钠的电子式正确的是 ( )
A.NaCl B.![]() C.
C.![]() D.Na+[Cl-]
D.Na+[Cl-]
10、某元素原子核外M电子层上的电子数比K层上的电子数多1,则此元素位于元素周期表中的位置 ( )
A、第二周期 第ⅢA族 B、第三周期 第ⅡA族
C、第三周期 第ⅢA族 D、第二周期 第ⅤA族
11、我国将启动定名为“嫦娥工程”的探月工程,登月的重要意义在于探索月球为人类造福。已知月球上深度3米以内的3He有70多万吨,如果用于核反应发电,可供地球上的人类使用7千年。3He与4He的关系是 ( )
A.同分异构体 B.同素异形体 C.同位素 D.同一种原子
12、硝酸应避光保存是因为它具有 ( )
A.强氧化性 B.挥发性 C.强酸性 D.不稳定性
13、下列物质中不能使酸性高锰酸钾溶液褪色的是 ( )
A.乙烷 B.乙烯 C.乙炔 D.乙醛
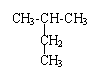 14、结构简式为 的烃,其正确的命名是
( )
14、结构简式为 的烃,其正确的命名是
( )
A.1,1一二甲基丙烷 B.2一乙基丙烷 C.3一甲基丁烷 D.2一甲基丁烷
15、实验室收集下列气体不能用排水法收集的是 ( )
A.NO B.H2 C.NO2 D.CH4
16、下列元素中金属性最强的是 ( )
A.钠 B.镁 C.铝 D.铁
17、常温常压下,燃烧相同物质的量的下列烃,消耗O2物质的量最多的是 ( )
A.CH4 B.C2H2 C.C2H4 D.C6H6
18、下列物质中,既含有离子键又含有共价键的是 ( )
A.H2O B.NH4Cl C.NaCl D.C2H4
19、下列过程中,需要加快化学反应速率的是 ( )
A.钢铁腐蚀 B.食物变质 C.金属冶炼 D.塑料老化
20、淀粉水解最终的产物是 ( )
A.蔗糖 B.葡萄糖 C.氨基酸 D.甘油
21、在强酸性溶液中能大量共存的离子是 ( )
A.OH- B.AlO2- C.HCO3- D.NH4+
![]() 22、合成氨反应为:N2(g)+3H2(g) 2NH3(g)(正反应为放热反应),为了使平衡向生
22、合成氨反应为:N2(g)+3H2(g) 2NH3(g)(正反应为放热反应),为了使平衡向生
成氨的方向移动,可采用的方法是 ( )
A.增大压强 B.减小压强 C.升高温度 D.使用催化剂
23、下列反应的离子方程式书写错误的是 ( )
A.盐酸跟氢氧化钠溶液反应: H+ + OH -= H2O
B.硝酸跟碳酸钠溶液反应: 2H+ + CO32- = CO2↑ + H2O
C.氯化钠溶液跟硝酸银溶液反应: Ag+ + Cl - = AgCl↓
D.盐酸跟氢氧化铜反应: H+ + OH- = H2O
24、只用一种试剂鉴别氯化铵、氯化铝、氯化铁、氯化镁四种溶液,这种试剂是( )
A.酚酞 B.氨水 C.硝酸银溶液 D.氢氧化钠溶液
25、下列各组物质互为同系物的是 ( )
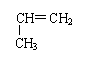 A.C6H5CH2OH和C6H5OH B.CH2=CHCH3 和
A.C6H5CH2OH和C6H5OH B.CH2=CHCH3 和
C.C6H6和C2H2 D.CH3OH和CH3CH2OH
26、只用一种试剂鉴别乙醇、乙醛、乙酸,此试剂是 ( )
A.溴水 B.新制Cu(OH)2 C.酸化的高锰酸钾溶液 D.饱和碳酸钠溶液
27、火星探测器发回的信息表明,火星上存在针铁矿[Goethite,化学式:FeO(OH)]和黄钾铁矾[Jarosite],从而证明火星表面曾经存在过水。这一发现被《人民日报》评为2004世界十大新闻之首。已知两种矿物中铁的价态相同,则黄钾铁矾{化学式记为:KFe3(SO4)2(OH)n}中n值为: ( )
A.4 B.5 C.6 D.7
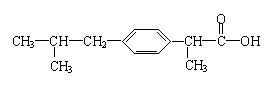 28、芬必得是一种性能优良、使用广泛的解热、镇痛、抗炎的长效缓释药物,其主要成分的结构简式如下:.
28、芬必得是一种性能优良、使用广泛的解热、镇痛、抗炎的长效缓释药物,其主要成分的结构简式如下:.
下列对芬必得的叙述不正确的是 ( )
A.芬必得具有酸性
B.1mol芬必得在一定条件下最多能与4molH2加成
C.芬必得虽含有苯环结构,但不属于苯的同系物
D.芬必得在一定条件下可以跟乙醇发生酯化反应
试 卷 Ⅱ
二、填空题(本题有3小题,共20分)
29、(10分)写出下列化学方程式或离子方程式:
(1)乙醛与氢气在一定条件下反应的化学方程式: ;反应类型为 。
(2)苯与液溴在一定条件下反应的化学方程式: ;反应类型为 。
(3)明矾净水时发生反应的离子方程式: 。
30、(6分)[本题包括2小题,每位同学只需选做一小题,若都做,则按第(1)小题记分]
(1)以乙烯为原料制取乙酸乙酯的过程为:
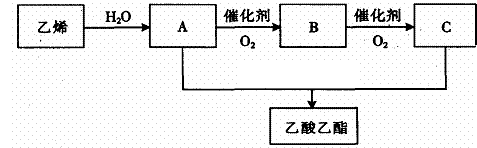 |
则A的结构简式为____________,B的名称为____________,C的官能团名称为 。
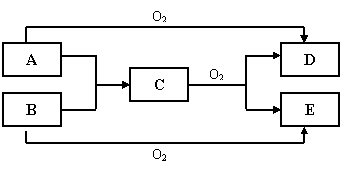 (2)已知常温下A、B、C、D为四种无色气体,E为无色液体。它们在一定条件下有如下的转化关系:
(2)已知常温下A、B、C、D为四种无色气体,E为无色液体。它们在一定条件下有如下的转化关系:
写出B、C、D各物质的化学式:B: C: D:
31、(4分)运用学过的化学知识,解释下列事实(用必要的文字或方程式说明)
(1)实验室里为了配置澄清的CuSO4溶液,配置时常在溶液中加入少量的稀硫酸,试解释原因: 。
(2)电工操作时规定不能把铜线与铝线拧在一起进行线路的连接,原因: 。
三、简答题(本题有两小题,共12分)
32(4分)、下列实验操作或叙述不正确的是 (填序号)
① 用燃烧方法可以鉴别聚乙烯塑料和聚氯乙烯塑料
② 把氢氧化钠固体放入容量瓶中加水配置0.1mol/L的氢氧化钠溶液
③ 用量筒准确量取20.25mL的食盐溶液
④ 用分液漏斗将乙醇和水的混合物分离
⑤ 用PH试纸直接浸入盐酸溶液中测其PH值
⑥ 用酒精洗涤沾在手上的苯酚
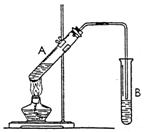 33、(8分)右图为实验室制取乙酸乙酯的装置图。试回答:
33、(8分)右图为实验室制取乙酸乙酯的装置图。试回答:
(1)A中加入试剂的顺序依次为: 。(2)B中所盛试剂是 ,其作用是 。 (3)从B中提取乙酸乙酯,宜采用的简便分离方法是
四、计算题(本题有两小题,共12分)
34、(5分)2006年,我国内地发生亮菌甲素假药中毒事件,事件发生后,有关部门立即对齐齐哈尔第二制药厂生产的亮菌甲素假药进行查封。已知亮菌甲素的相对分子质量为234,其中含碳的质量分数为61.5%,含氢的质量分数为4.3%,其余为氧,通过计算写出亮菌甲素的分子式。
35、(7分)现有一包铁铝混合样品,某研究性学习小组欲测定该样品各成分的含量,进行下列实验:
甲、乙、丙各取300mL同浓度的盐酸,加入不同质量的同一混合样品,有关数据如下表(气体体积均在标准状况下测定):
| 实验序号 | 甲 | 乙 | 丙 |
| 混合样品质量(mg) | 830 | 1098 | 1258 |
| 气体体积(mL) | 560 | 672 | 672 |
求:(1)盐酸的物质的量浓度是多少?
(2)样品中各成分的质量分数。
参考答案
一、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 答案 | D | A | A | C | C | D | B | C | B | C | C | D | A | D |
| 题号 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 |
| 答案 | C | A | D | B | C | B | D | A | D | D | D | B | C | B |
 二、填空题
二、填空题
![]()
![]() 29、(1)CH3CHO
+ H2
CH3CH2OH
加成反应
29、(1)CH3CHO
+ H2
CH3CH2OH
加成反应
![]() (2)
+ Br2
+ HBr 取代反应
(2)
+ Br2
+ HBr 取代反应
![]() (3)Al3++3H2O Al(OH)3 +
3H+
(3)Al3++3H2O Al(OH)3 +
3H+
30、(1)A的结构简式:CH2CH2OH ; B的名称:乙醛 ; C的官能团名称:羧基
(2)B:H2;C:NH2;D:NO
![]() 31、(1)因为铜离子水解,Cu2++H2O Cu(OH)2+H+,加入稀硫酸抑制铜离子的水解,使溶液澄清。
31、(1)因为铜离子水解,Cu2++H2O Cu(OH)2+H+,加入稀硫酸抑制铜离子的水解,使溶液澄清。
(2)铜与铝在潮湿的环境下形成了原电池,加快了铝的腐蚀,长时间后会使线路发生短路。
32、②③④⑤
33、(1)乙醇、浓硫酸、冰醋酸
(2)饱和碳酸钠溶液;中和乙酸,溶解乙醇,分层乙酸乙酯
(3)分液
34、C12H10O5
35、(1)C(HCl)=0.2mol/l
(2) 铁的质量分数:67.5%
铝的质量分数:32.5%