�߶���ѧ��ѧ�����п����Ծ�(X��)
���������������� ��I����ѡ���⣬��74�֣�
�����õ������ԭ��������H 1��C 12��Cu 64��O 16��
һ��ѡ���⣨���14С�⣬ÿС��3�֣���42�֡�ÿС��ֻ��һ��ѡ��������⡣��
1��������Һ�����ԡ�����ǿ����˵���У���ȷ����
A.������ֻҪ��Һ����H+,��Һ��������
B.������H+Ũ��������Һ������һ����ǿ
C.������H+Ũ�ȴ���OH-��Ũ�ȣ���Һһ��������
D.���� ǿ����Һ������һ����������Һ������ǿ
2��
E.��������
F.��������
G.��������
2.�������� ����ˮ�����ص��������������ԣ������йص�˵������ȷ���ǣ���������� �ڰ�ˮ���� �� ǡ����ȫ��Ӧ �� c (NH4+) = c(Cl��) ��c (NH4+) �� c(Cl��)
A. �٢ݡ���������������B. �ۢܡ���������������C. �ڢݡ���������������D. �ڢܡ�
3. ��һ�����¶��£���0.2mol/LCH3COOH����Һ���ˮϡ�ͣ����и������ı仯�У������Ǣ�c(H+)�����ʵ���Ũ�� ��c(OH-��)�����ʵ���Ũ�� ��c (CH3COO-��)/c(CH3COOH) ��c(H+)��c(OH-��)
A .�� �ܡ��������� B. ���ڢۡ�������������C. �ۢܡ���������������D. �ڢ�
4. ���ܱ������н��л�ѧ��Ӧ��2SO2 + O2![]() 2SO3����֪��Ӧ������ijһʱ��SO2��O2��SO3Ũ�ȷֱ�Ϊ0.2mol/L��0.1mol/L��0.2mol/L������Ӧ�ﵽƽ��ʱ���ܴ��ڵ�������
2SO3����֪��Ӧ������ijһʱ��SO2��O2��SO3Ũ�ȷֱ�Ϊ0.2mol/L��0.1mol/L��0.2mol/L������Ӧ�ﵽƽ��ʱ���ܴ��ڵ�������
A��SO2Ϊ0.4mol/L��O2Ϊ0.2mol/L���� B��SO2Ϊ0.25mol/L
C��SO2��SO3��Ϊ0.15mol/L���������� D��SO2Ϊ0.4mol/L
5. �¶�һ��ʱ, ���ܱ������з������淴Ӧ: mA(��)
+ nB(��) ![]() ����pC(��), �ﵽƽ���, ���������������ѹ����ԭ���� 1/2, ���ٴδﵽƽ��ʱ, C��Ũ��Ϊԭƽ��ʱC��Ũ�ȵ� 1 .9 ��, ��������������ȷ����
����pC(��), �ﵽƽ���, ���������������ѹ����ԭ���� 1/2, ���ٴδﵽƽ��ʱ, C��Ũ��Ϊԭƽ��ʱC��Ũ�ȵ� 1 .9 ��, ��������������ȷ����
A. ƽ�����淴Ӧ�����ƶ����������� B. C����������������
C. ����A��ת�������ߡ����������� D. m + n > p������
6.���ܱ������н������з�Ӧ��M(g)��N(g)![]() R(g)��2L���˷�Ӧ��������ͼ������
R(g)��2L���˷�Ӧ��������ͼ������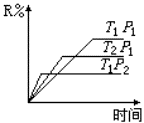 ������ȷ���ǡ���
������ȷ���ǡ���
A. ����Ӧ���ȣ�L������
B. ����Ӧ���ȣ�L�ǹ���
C. ����Ӧ���ȣ�L������
D. ����Ӧ���ȣ�L�ǹ����Һ��
7. 25������ˮ��Һ��HCl����FeCl3����KOH����Na2CO3�� PHֵ����Ϊ4��4��10��10������Һ��ˮ�ĵ���̶ȴ�С��ϵ��ȷ���ǡ�
A����=��=��=�ܡ������������������� B���٣��ۣ��ڣ���
C����=�ڣ���=�١������������������� D����=�ۣ��ڣ���
8. ��1molSO2��1molO2ͨ��һ���������ܱ������У���һ���¶Ⱥʹ��������£���Ӧ�ﵽƽ�⣬SO3Ϊ0.3mol����ʱ������0.5molO2��0.5molSO2����Ӧ�ﵽ�µ�ƽ��ʱ��SO3�����ʵ���Ϊ��
A��0.3mol�������������������� B��0.15mol��������
C����0.15mol�������������� D������0.15mol,��0.3mol
9. ��20.0��NaOH��ϡ��Һ��ϡ���ᷴӦ���ų�28.7kJ����������ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽ��ȷ���ǡ������� ����������������������������������������������������������������������������������������
A��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)����H=+28.7kJ/mol
B��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)����H=-28.7kJ/mol
C��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)����H=+57.4kJ/mol
D��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)����H=-57.4kJ/mol
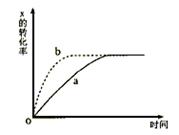
10. ��ͼ����a��ʾ���ȷ�ӦX(g)+Y(g)��![]() �� Z(g)+M(g)+N(s)���й�����X��ת������ʱ��
�� Z(g)+M(g)+N(s)���й�����X��ת������ʱ��
|
���߽��У��ɲ�ȡ�Ĵ�ʩ��
������A�������¶ȡ����� B���Ӵ�X��Ͷ����
������C���Ӵ�����������D���������
11. �����º�ѹ�£����ݻ��ɱ�������У���Ӧ2NO2��g��![]() N2O4��g���ﵽƽ�������������ͨ��һ����NO2���ִﵽƽ��ʱ��N2O4���������
N2O4��g���ﵽƽ�������������ͨ��һ����NO2���ִﵽƽ��ʱ��N2O4���������
A. ���� ��������B. ���������� C. ���� ������������D. ���ж�
12. ���ʵ���Ũ����ͬ�����и����ʵ���Һ�У�NH4+Ũ���ɴ�С����
�� ��NH4Al(SO4)2 ��NH4HCO3�� ��NH4HSO4�� ��NH4NO3
A���٢ۢܢڡ� B���ۢ٢ܢڡ� C���ڢܢ٢ۡ� D���٢ۢڢ�
13. ����˵���п��Գ��˵����ӦP(g)��Q(g)�� ![]() ��R(g)��S(g)�ں����������Ѵﵽƽ��״̬����
��R(g)��S(g)�ں����������Ѵﵽƽ��״̬����
A�������ڵ�ѹǿ����ʱ��ı仯���ı䡡�� B��P��R�������������
C�����������ܶȲ�����ʱ����仯������ D��������P��Q��R��S����
14.���ȷ�Ӧһ����
���ͷ��������� �������������� �۷�Ӧ��������������������������
������������������ڷ�Ӧ���������
A���٢ۡ�����B���٢ܡ���C���ڢۡ� D���ڢ�
����ѡ���⣨���8С�⣬ÿ��4�֣���32�֡�ÿС����һ��������ѡ��������⡣��
15. ����ͬ���ʵ���Ũ�ȵ�ij����HX��Һ��NaX��Һ�������ϣ���û�Ϻ���Һ��c(Na+)>c(X��)�������й�ϵ�������ǡ�������
����A��c(OH-)>c(H+)����������������B��c(HX)<c(X-)
C��c(X-)+c(HX)=2c(Na+)�� ������D��c(HX)+c(H+)=c(Na+)+c(OH-)
16.pHֵ��ȵ����ᣨ�ף��ʹ��ᣨ�ң����ֱ���п��Ӧ�������п��ȫ���ܽ��ҷų�����һ���࣬Ϊ������˵����ȷ����
A����Ӧ��ʼʱ�����ʣ��ף��ҡ������������� B����Ӧ����ʱ�䣺�ף���
C����Ӧ��ʼʱ��������ʵ���Ũ�ȣ��ף��ҡ� D����Ӧ�����Һ��pHֵ���ף���
17����������a����Ba(OH)2��b����NaOH��Һ��c����NH3��H2O��Һ������˵����ȷ����
A��ͬ���ʵ���Ũ�ȵ�������Һ��pH��a��b��c��
B��ͬpHʱ��������Һϡ����ͬ������pH��a=b��c
C��ͬpH��ͬ�����������Һ����ͬŨ������������a=b=c
D��ͬpHʱ��ϡ�Ͳ�ͬ������pH����ͬ��������Һϡ�͵ı�����a��b��c
18. �ڳ����£���PH=11��ij����Һ��PH=3��ij����Һ�������ϣ��Դ�����˵����ȷ���ǡ��� A
��A.��������Һ�����ԣ������ɵ��ο���Ϊǿ��ǿ����
��B.�����õ���Һ�ʼ��ԣ��������ǿ����������Һ��Ӧ
��C.��������Һ�����ԣ��������ǿ����������Һ��Ӧ
��D.��������Һ��PH=5�������ǿ����������Һ��Ӧ ��
19����Ca(OH)2�������һ����������ˮ�У�һ���¶��´ﵽƽ�⣺Ca(OH)2��s��![]() Ca2+(aq)+2OH-(aq)����������Һ�м�������ʯ�Һ����¶ȱ��ֲ��䣬�����ж���ȷ����
Ca2+(aq)+2OH-(aq)����������Һ�м�������ʯ�Һ����¶ȱ��ֲ��䣬�����ж���ȷ����
A����Һ��Ca2+��Ŀ���١������� B����Һ��c(Ca2+)����
C����ҺpHֵ���䡡������������ D����ҺpHֵ����
20. ��֪ij��Һ��ֻ����OH-����H+��NH4+��Cl-���������ӣ�ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ����������������
A��c(Cl-��)��c(NH4+)��c(H+)��c(OH-��)������B��c(Cl-��)��c(NH4+)��c(OH-��)��c(H+)
C��c(Cl-)��c(H+)��c(NH4+)��c(OH-)����������D��c(NH4+)��c(Cl-)��c(OH-)��c(H+)
21. ���ݻ�һ�����ܱ������У���Ӧ2A![]() B��g����C��g���ﵽƽ��������¶�������������ܶ�����������������ȷ����
B��g����C��g���ﵽƽ��������¶�������������ܶ�����������������ȷ����
A.����Ӧ�����ȷ�Ӧ����A������̬��������
B.����Ӧ�Ƿ��ȷ�Ӧ����A����̬
C.�����������䣬��������A����ƽ��������Ӧ�����ƶ�
D. �ı�ѹǿ�Ը�ƽ����ƶ���Ӱ��
22. ��100��ʱ����0.50 mol N2O4����ͨ�뵽���Ϊ5.0 L������ܱ��������������ֺ���ɫ����Ӧ���е�2��ʱ��NO2��Ũ��Ϊ0.02 mol/L��60��ʱ��ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼ��1.6��������˵����ȷ����
A��ǰ2����N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.010 mol/(L��s)
B����2��ʱ��ϵ��ѹǿΪ��ʼʱ��1.1��
C��ƽ��ʱ��ϵ�ں�N2O4 Ϊ0.25mol
D��ƽ��ʱ���ѹ�������������������N2O4��ת����
��II������ѡ���⣬��76�֣�
�������������2С�⣬��20�֣�
23����9�֣�����0.1mol•L-1�Ĵ�����Һ,����PH��ֽ�ⶨ��Һ��PH,����ȷ�IJ����������������� ��������Һ�ʼ��Ե�ԭ�������ӷ���ʽ��ʾ������������ -��������Ϊ����ҺPH�ķ�Χһ������������ ��
Ϊ̽��������Һ�ʼ�������CO32-����ģ��������һ����ʵ�鷽����
�� ���������������������������������������������������������� ��
24����11����ͼij��ѧʵ��С����̵���ص�Ũ�����Լ���ǩ�IJ������ݣ���С���ڿ��������л��������Ϣ��Ũ���ḯʴ�Ժ�ǿ������ˮʱ�ͷŴ������ȣ�Ũ���������ֲ����롣
|
��HSO4- ![]() SO42-��+
H+������������������
SO42-��+
H+������������������
�����Լ�ƿ���ܷ�ǩ������,���ǻ��ɸ����������������ǩ����,ȷ����չ�о�.
��������Ϊ������һ�־���������������Һ��C(H+),��C(H+) =36.8 mol•L-1,����Һ����������Ϊ0.98;
�� ����Ϊ����ʹ�о��ܵ�����������Ҳ���У��������������������⡣�������룺ȡһ����������������BaCl2��Ӧ�����ˡ�ϴ�ӡ������������������������
�� �������á��к͵ζ������в������������£�A��ȷ��ȡһ����������ᣬ����������ˮϡ�ͣ�B����ϡ�ͺ���Һ�е���2-3�η�̪��C����һ��Ũ�ȵ�NaOH��Һ�ζ���ֱ�����ֵζ��յ�Ϊֹ��D����¼���ĵ�NaOH��Һ�������
�ش��������⣺��
��1�����ƶϡ���ͬѧ���������С��������ǣ��������� ��
��2���ҷ����Ĺؼ����������㣺��ȷ��SO42-��ȫ��Ӧ����ϴ�ӳ�����ȷ�������������ʡ���ʵ��������϶�SO42-��ȫ��Ӧ��
�������������������������������� ��
��3�����ϡ��Ũ������Һ��
���������������������������������� ��
��4�����������в�����ʹ�ⶨ���ƫ���������� ��
���ڵζ�ǰδ��NaOH����Һ��ϴ�ζ���
���ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���ζ��ܼ��첿��������ʧ
����ƿ��ˮϴ�ɾ���δ�ô���Һ��ϴ
����ʼʱƽ�Ӷ������ζ����ʱ���Ӷ���
��5������ʵ���У��ֱ�ȡ����5.00mL,��5.00mol/L NaOH�ζ�����,�յ�ʱ,�õ���NaOH���������Ϊ35.65mL��40.62mL��35.55mL,��ͨ������������Ƿ�ϸ�.��Ҫ������̣�
�ġ����������5С�⣬��43�֣�
25��(10��)
��1����FeCl3��Һ�����������IJ��������������� ��
�� ��2����ҵ���Ʊ��������Ȼ�пʱ���������ʵ��Ȼ�п���ڹ��������У�Ϊ�˳�ȥ�����������Һ��PH��4��Ӧ������Լ��������������� ��
�� ��3��3mol/L 100mL��H2SO4��Һ��������Zn��Ӧ��Ϊʹ������H2���ʼ�����������H2���������䣬�ɲ�ȡ�Ĵ�ʩ�������� ������������ѡ�����ţ�
�ټӹ���CH3COONa�� ��BaCl2��Һ�� ��NH4Cl��Һ���� �ܼӰ�ˮ��
��4����1�������ǡ����10���PH=11���������Ƶ���Һ��ȫ��Ӧ����������ʵ���Ũ��֮������������ ��
26����4�֣���֪��2H2(g)
+ O2(g) == 2H2O(g)����H= �C483.6
kJ��![]() , H2(g) + 1/2O2(g) == H2O(l)����H=�C285.8 kJ��
, H2(g) + 1/2O2(g) == H2O(l)����H=�C285.8 kJ��![]() ,�ɴ˿�֪���ڵ���������45gҺ̬ˮ������_____������kJ��������27����3�֣���ͬѧ�����Ƶ�����Mg(OH)2�����м���Ũ��CH3COONH4��Һ�����������ȫ�ܽ⣬��֪CH3COONH4��Һ�����ԣ������й����۽�����һ��ʵ����������������������������������������������������������������
,�ɴ˿�֪���ڵ���������45gҺ̬ˮ������_____������kJ��������27����3�֣���ͬѧ�����Ƶ�����Mg(OH)2�����м���Ũ��CH3COONH4��Һ�����������ȫ�ܽ⣬��֪CH3COONH4��Һ�����ԣ������й����۽�����һ��ʵ����������������������������������������������������������������
�������������������������������������������������� ����������������������������
28����12�֣�ij��Ԫ�ᣨ��ѧʽ��H2A��ʾ����ˮ�еĵ��뷽��ʽ�ǣ�
H2A=H++HA������
HA-����![]() ���� H++A2��
���� H++A2��
�ش��������⣺
��1�������� Na2A��Һ��____________������ԡ��������ԡ������ԡ�����
������____________________________________________�������ӷ���ʽ��ʾ��
��2�������� ��0.1mol.L-1��Na2A��Һ�У�������Ũ�ȹ�ϵʽ��ȷ����__________
A��c(A2��) +c( HA��)+c( H2A) =0.1mol��L-1 ������ B��c(OH��)=c(H+) +c( HA��)��������������
C��c(Na+ )+ c(H+) =c(OH��)+ c( HA��)+2c(A2��)�� D��c(Na+ )= 2c(A2��) +2c( HA��)����������
��3�������� ��֪0.1mol��L��1NaHA��Һ��pH=2����0.1mol��L-1 H2A��Һ�������ӵ����ʵ���Ũ�ȿ�����_______ 0.11 mol��L��1�������������������=�����������ǣ�
____________________________________________________________
��4�������� 0.1mol��L��1 NaHA��Һ�и�������Ũ���ɴ�С��˳���ǣ�____________________
29����14�֣�t��ʱ����3mol A��1molB����ͨ�����Ϊ2L���ܱ������У��ݻ����䣩���������·�Ӧ��3A��g�� + B(g) ![]() xC(g)
xC(g)
2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩��ʣ����0.8molB,�����C��Ũ��Ϊ0.4mol/L,����д���пհ�:
(1)�����ӿ�ʼ��Ӧ���ﵽƽ���״̬,����Cƽ����Ӧ����Ϊ�������� .
(2)����x=������ ;ƽ�ⳣ��K=�������� .
(3)������������ԭ������������ͨ����������(�躤����A��B��C������Ӧ)��ѧƽ�⣨����ĸ������������ ��
A��������Ӧ�����ƶ����� B�����淴Ӧ�����ƶ������� C��ƽ�ⲻ�ƶ�
��4������ԭƽ��������������ٳ���amolC����t��ʱ�ﵽ��ƽ�⣬��ʱB�����ʵ���Ϊn��B��=��������mol��
��5�����������Ӧ����ͬ�¶Ⱥ������н��У���ʹ��Ӧ�ﵽC�����ʵ���������ԭƽ����ȣ���ʼ������������ʵ����ʵ���n��A����n��B����n��C��֮��Ӧ������Ĺ�ϵʽΪ����
�������������� ��
�塢���������С�⣬��13�֣�
30. ������ܱ������ڼ���amolPH4I���壬��һ���¶��·������·�Ӧ��
��������
PH4I��s��![]() PH3��g��
+ HI��g��
PH3��g��
+ HI��g��
��������
4PH3��g��![]() P4��g��
+ 6H2��g��
P4��g��
+ 6H2��g��
������������
2HI��g��![]() ��H2��g����+ I2��g��
��H2��g����+ I2��g��
��������Ӧ����ƽ����HIΪbmol��I2��g��Ϊcmol��H2Ϊdmol��
��
��1�������� ƽ���������P4��g����PH3�����ʵ������ô���ʽ��ʾ����
����n��P4����=����������n��PH3��= ����������
��2��a��b��c���߷���a>������ (��b��c�Ĵ���ʽ)��
b��c��d���ߵĹ�ϵ����b>�� (��c��d�Ĵ���ʽ)
��3��ƽ�������ѹǿ��������n��I2������ ��n��PH4I�������� ��������С�����䣩
��ѧ�Ծ����ֱ�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| �� | C | D | B | B | A | C | C | C | D | C | A |
| ��� | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| �� | B | B | C | B | AC | AB | AD | AC | B | A | B |
�������������2С�⣬��20�֣�
![]() 23����9�֣���һС����ֽ���ڱ�����(����Ƭ)��,��պ�д�����Һ�IJ�����������ֽ���в�,��ֽ��ɫ��,�����ɫ���Ƚ���ȷ����Һ��PH����2�֣�CO32-
+H2O��������H CO3-
+ OH-������2�֣���7-13������2�֣���
23����9�֣���һС����ֽ���ڱ�����(����Ƭ)��,��պ�д�����Һ�IJ�����������ֽ���в�,��ֽ��ɫ��,�����ɫ���Ƚ���ȷ����Һ��PH����2�֣�CO32-
+H2O��������H CO3-
+ OH-������2�֣���7-13������2�֣���
��2����3�֣�����Һ�еμӷ�̪��Һ����Һ�Ժ�ɫ�����������Һ�е�������Ȼ�����Һ��������ɫ����������Һ��ɫ��ȥ��˵��������Һ�ʼ�������CO32-����ġ�
24����11��
����:(1)Ũ���������������,������ȫ����.��2�֣�
�� (2)���ϲ���ҹ (��ȡ�����ϲ���ҹ����С�Թ�) ��,�μ�BaCl2��Һ,�������������,˵�������Ѿ���ȫ.��2�֣�
�� (3)ȡһ�������ˮ�����ձ���,��Ũ���Ỻ������ˮ��,�ӱ߽���.��2�֣�
�� (4) �� �� ��2�֣�
�� (5)17.8mol/L<18.4mol/L��3�֣����,������ϸ�.
�ġ����������4С�⣬��41�֣�
25��(10��)
��1��Fe2O3���� ��2��ZnO��Zn��OH��2�� ��3���٢ڡ� ��4��5��1��4�֣�
26����4�֣�110
27����3�֣�Mg(OH)2��s��![]() Mg2++2OH-,������κ�,NH4++OH-
Mg2++2OH-,������κ�,NH4++OH-![]() NH3��H2O��Һ��OH-����Ũ�ȼ�С,�ܽ�ƽ�������ƶ�,������ȫ�ܽ�.��������
NH3��H2O��Һ��OH-����Ũ�ȼ�С,�ܽ�ƽ�������ƶ�,������ȫ�ܽ�.��������
28������12�֣�
��1�����ԣ� A2- + H2O��![]() HA-��+ OH-����1�֣�
HA-��+ OH-����1�֣�
��2��BCD��(��ѡ0�֣�3��) ��
��3��<������H2A��һ�����������H+��������HA-�ĵ��롣����2�֣�
��4��c(Na+ )> c(HA-)> c(H+)> c(A2-)> c(OH- )����3�֣���
29����14�֣���������2�֣�
��1��0.2 mol•L-1•min-1(˵��:��д��λ�۷�)
(2)4;1/27
(3)C
(4)(0.8+0.2a)��3�֣�
(5)n��A��=3n��B����n��C����0[��n��A��=n��B��=0��n��C����0]
�塢
30. ��13�֣�
�𰸣���������2�֣�
��1�������� n��P4�� = ��d-c��/6��n��PH3��=b+8 c /3 -2 d /3 ��3�֣�
��2�������� a>b +2c;b>2d/3 -8c/3
��3�������� ��С;����.