高二化学第一学期中考试卷
时间:90分钟 2 :40 ~ 4 :10
可能用到的有关原子的相对质量:H 1 N 14 O 16
第I卷 选择题(45分)
一、选择题 (每小题只有1个选项最符合题意,每题3分,共45分)
1. 下列气体能造成空气中光化学烟雾污染的是-------------------------------------------------( )
A. CO B. SO2 C. NO2 D. Cl2
2. 在NO2与水的反应中,NO2所表现的性质是------------------------------------------------( )
A. 只是氧化剂 B. 只是还原剂
C. 既是氧化剂,又是还原剂 D. 既不是氧化剂,又不是还原剂
3. 可用以干燥氨气的物质是-------------------------------------------------------------------------( )
A. 浓硫酸 B. 五氧化二磷 C. 无水硫酸铜 D. 生石灰
4. 氮的某氧化物中,氮元素与氧元素的质量比为7 :20,此氧化物中氮的化合价为--( )
A. +1 B. +2 C. +4 D. +5
5. 某一个反应物的浓度是1.0 mol/L,经过20 s后,它的浓度变成了0.2 mol/L,在这20 s内
它的反应速率为--------------------------------------------------------------------------------------( )
A. 0.04 B. 0.04 mol・(L・s)-1 C. 0.8 mol・(L・s)-1 D. 0.04 mol/L
6. 可逆反应N2+3H2![]() 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。
下列各关系中能说明反应已达到平衡状态的是( )
A 3v正(N2)=v正(H2) B v正(N2)=v逆(NH3)
C 2v正(H2)=3v逆(NH3) D v正(N2)=3v逆(H2)
7. 下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是---( )
A. 2NO2![]() N2O4(正反应为放热反应) B. C(s)+ CO2
N2O4(正反应为放热反应) B. C(s)+ CO2![]() 2CO(正反应为吸热反应)
2CO(正反应为吸热反应)
C. N2 + 3H2 ![]() 2NH3(正反应为放热反应) D. H2S
2NH3(正反应为放热反应) D. H2S ![]() H2
+ S(s)(正反应为吸热反应)
H2
+ S(s)(正反应为吸热反应)
8. 下列离子反应方程式属于水解反应的是-------------------------------------------------------( )
A. NH3・H2O ![]() NH4+ + OH- B. HCO3- + H3O+
NH4+ + OH- B. HCO3- + H3O+
![]() H2CO3 + H2O
H2CO3 + H2O
C. HS- + H2O
![]() H2S + OH-
D. H2SO3
H2S + OH-
D. H2SO3
![]() HSO3- + H+
HSO3- + H+
9. 下列物质的水溶液,其pH小于7的是------------------------------------------------------( )
A. Na2CO3 B. NH4NO3 C. Na2SO4 D. KNO3
10. 0.1 mol/L K2CO3溶液中,由于CO32- 的水解,使c(CO32-)< 0.1 mol/L 。若要使c(CO32-)
更接近于0.1 mol/L,可以采取的措施是------------------------------------------------------( )
A. 加入少量盐酸 B. 加入适当KOH C. 加入适量水 D. 加热
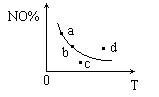 11. 如图曲线是表示其他条件一定时,
11. 如图曲线是表示其他条件一定时,
2NO+O2 ![]() 2NO2+Q(Q>0)反应中NO的转化率与温
2NO2+Q(Q>0)反应中NO的转化率与温
度的关系曲线,图中标有a、b、c、d四点,其中表示未达
到平衡状态,且v(正)>v(逆)的点是( )
A. a B. b C. c D. d
12. 在容积为4L的刚性密闭容器中,进行可逆反应:
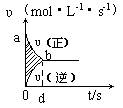 X(g)+2Y(g)
X(g)+2Y(g)![]() 2Z(g)并达到平衡,在此过程中,以Y
2Z(g)并达到平衡,在此过程中,以Y
的浓度改变表示的反应速率 v(正)、v(逆)与时间t的关系如
图。则图中阴影部分的面积表示( )
A. X的浓度的变化 B. Z的浓度的变化
C. Y的物质的量的减少. D. 无法判断。
13. 若常温时,某溶液由水电离出来的c(H+)=1×10-13mol/L,满足此条件的溶液中一定可以大量共存的离子组是( )
A.K+、Na+、Cl-、SO![]() B.K+、NH4+、Cl-、NO3-
B.K+、NH4+、Cl-、NO3-
C.Na+、Fe2+、Cl-、NO3- D.K+、Na+、Cl-、HCO3-
14. 100ml0.1 mol.L-1醋酸 与50mL0.2mol.L-1氢氧化钠溶液混合,在所得溶液中----( )
A [Na+]>[CH3COO+]>[OH-]>[H+] B [Na+]>[CH3COO+]>[H+]>[OH-]
C [Na+]>[CH3COO+]>[H+]=[OH-] D [Na+]=[CH3COO+]>[OH-]>[H+]
15、锌与某浓度的硝酸完全反应,消耗的锌与HNO3的物质的量之比为 5 :12,则还原产物可能是( )
A. NO2 B. NO C. N2O D. N2
第II卷 非选择题 (55分)
二、填空题 (有4小题 共32)
16. (2分)(1)碳酸氢钠溶液不为中性,为什么?(用离子方程式表示)
(3分)(2)实验室配制的氯化铁溶液,时间久常发现有浑浊出现,为什么?
出现浑浊的离子方程式 应加 试剂
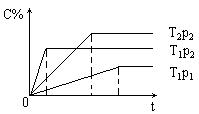 17. (8分)对于mA(g)+nB(g)
17. (8分)对于mA(g)+nB(g)![]() pC(g) + Q有如图所示的关系,
pC(g) + Q有如图所示的关系,
(图中C%为C的质量分数)则
(1)P1与P2 的关系:
(2)m+n与p的关系:
(3) T1与T2的关系:
(4)Q与0的关系:
(请用“>”“<”或“=”回答)
18. (10分)化学平衡移动原理,同样也适用于其它平衡,已知在氨水中存在下列平衡:
NH3 + H2O![]() NH3・H2O
NH3・H2O![]() NH4+ + OH-
NH4+ + OH-
(1)(3分)向氨水中加入CuSO4固体时平衡向 移动,OH-离子的浓度 ,
NH4+ 的浓度 。
(2)(4分)向氨水中加入浓盐酸,平衡向 移动,此时溶液中浓度减小的
粒子有 、 、 。
(3)(3分)向浓氨水中加入少量的NaOH 固体,平衡向 移动,此时发生的现
象是 。
19. (9分)下图![]() 分别代表有关反应中的一种物质,请填下以下空白。
分别代表有关反应中的一种物质,请填下以下空白。
(已知二氧化碳能与镁反应生成氧化镁和另一种单质)
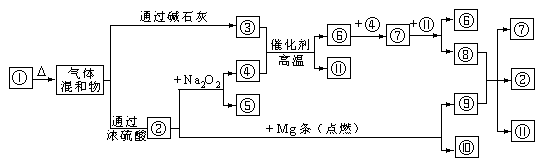
(1)(6分)①、③、④的化学式分别是
、
、 。
(2)(3分)⑧与⑨反应的化学方程式是
。
三、实验题 (有2题 共15分)
20. (4分) 用 pH 试纸测定溶液的 pH 时,为什么不能先用蒸馏水润湿试纸 ?
答:
21(11分)实验室用氨气还原氧化铜方法测定铜的近似相对原子质量, 反应的化学方程式为:
![]()
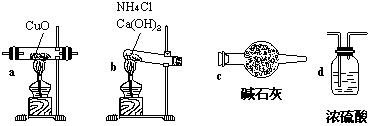 |
试回答:(1)如果选用测定反应物CuO和生成物H2O的质量(mCuo、
① (5分)仪器连接的顺序(用字母编号表示,仪器可重复使用) ;
d中浓硫酸的作用是 , ;
实验完毕时观察到a中的现象是 ;
② (2分)列出计算Cu的相对原子质量的表达式 ;
③ (2分)下列情况将使测定结果偏大的是 .
(以下选择填空不限1个正确答案,均用字母编号填写)
(a) CuO未全部还原为Cu (b)CuO受潮 (c)CuO中混有Cu
(2)(2分)如果仍采用上述仪器装置,其他方案可选用测定的物理量有
![]()
![]()
四、计算题(只有1小题 共8分)
22. (8分)将 等 物 质 的 量 的 A,B 混 合 于2 L 的 密 闭 容 器 中,发 生 反 应
3A(g)+ B(g)![]() xC(g) + 2D(g)。经5min分钟后达到平衡时,测知D的浓
xC(g) + 2D(g)。经5min分钟后达到平衡时,测知D的浓
度为0.5mol/L,[ A] :[ B] = 3 :5,C的平均反应速率为0.1mol・(L・min)-1 试求
(1)A的平衡浓度是多少?(2)B的平均反应速率?(3)x = ?
高二化学答案
一、1.C 2.C 3.D 4.D 5.B 6.C 7.B 8.C 9.B 10.B 11.C 12.B 13.A 14.A 15.D
二、16. (1)HCO3- +
H2O ![]() H2CO3 +OH-
H2CO3 +OH-
(2)Fe3+ + 3H2O
![]() Fe(OH)3 +
3H+ HCl
Fe(OH)3 +
3H+ HCl
17. p2>p1 m+n>p T1>T2 Q>0
18.(1)右 减小 增大 (2)右 OH- NH3・H2O NH3
(3)左 NaOH 固体溶解,溶液中产生气泡。
19. (1)NH4HCO3或(NH4)2CO3, NH3, O2 (2)C+4HNO3 = 2H2O+4NO2+CO2
20. 答到 “ 降低溶液的浓度 ” 给满分.
21. (1)①b c a c d 吸收未反应的氨 防止空气中水分进入 固体由黑色转变
![]()
(2)a、c
22. (1)0.75mol/L (2)0.05 mol・(L・min)-1 (3)x = 2
曲仁中学2004---2005学年度第一学期中考
高二化学答案 2004年11月
一、1.C 2.C 3.D 4.D 5.B 6.C 7.B 8.C 9.B 10.B 11.C 12.B 13.A 14.A 15.D
二、16. (1)HCO3- +
H2O ![]() H2CO3 +OH-
H2CO3 +OH-
(2)Fe3+ + 3H2O
![]() Fe(OH)3 + 3H+ HCl
Fe(OH)3 + 3H+ HCl
17. p2>p1 m+n>p T1>T2 Q>0
18.(1)右 减小 增大 (2)右 OH- NH3・H2O NH3
(3)左 NaOH 固体溶解,溶液中产生气泡。
19. (1)NH4HCO3,NH3,O2 (2)C+4HNO3 = 2H2O+4NO2+CO2
20. 答到 “ 降低溶液的浓度 ” 给满分.
21. (1)①b c a c d 吸收未反应的氨 防止空气中水分进入 固体由黑色转变
![]()
(2)a、c
22. (1)0.75mol/L (2)0.05 mol・(L・min)-1 (3)x = 2
曲仁中学2004---2005学年度第一学期中考
高二化学答案 2004年11月
一、1.C 2.C 3.D 4.D 5.B 6.C 7.B 8.C 9.B 10.B 11.C 12.B 13.A 14.A 15.D
二、16. (1)HCO3- +
H2O ![]() H2CO3 +OH-
H2CO3 +OH-
(2)Fe3+ + 3H2O
![]() Fe(OH)3 + 3H+ HCl
Fe(OH)3 + 3H+ HCl
17. p2>p1 m+n>p T1>T2 Q>0
18.(1)右 减小 增大 (2)右 OH- NH3・H2O NH3
(3)左 NaOH 固体溶解,溶液中产生气泡。
19. (1)NH4HCO3,NH3,O2 (2)C+4HNO3 = 2H2O+4NO2+CO2
20. 答到 “ 降低溶液的浓度 ” 给满分.
21. (1)①b c a c d 吸收未反应的氨 防止空气中水分进入 固体由黑色转变
![]()
(2)a、c
22. (1)0.75mol/L (2)0.05 mol・(L・min)-1 (3)x = 2