高中证书化学会考
相对原子质量:H-1,C-12,N-14,O-16,Na-23,Mg-24,Al-27,S-32,Fe-56,Ag-108。
一、选择题(本题有32小题,每小题2分,共64分。每小题只有1个选项符合题意。)
1、下列物质中,属于有机物的是:A、CO2;B、KCl;C、C2H4;D、Na2CO3。
2、饱和链烃的通式为:A、CnH2n+2;B、CnH2n;C、CnH2n-2;D、CnH2n-6。
*3、对某一可逆反应来说,使用催化剂的作用是:A、提高反应物的转化率;B、以同等程度地改变正逆反应的速率;C、增大正反应速率,减小逆反应速率;D、改变平衡混合物的组成。
*4、加入下列哪一种试剂后,可促进水的电离:
A、H2S;B、KCl;C、NaOH;D、AgNO3。
5、下列物质属于纯净物的是:A、液氯;B、碘酒;C、漂白粉;D、盐酸。
6、属于氧化还原反应的是:A、MnO2 + 4HCl(浓)=MnCl2 + Cl2↑+2H2O;
B、Al2O3+6HCl=2AlCl3+3H2O;C、2NaHCO3= Na2CO3+CO2↑+H2O;
D、NaOH+HCl=NaCl+H2O。
7、下列叙述正确的是:A、H+的摩尔质量是1g;B、H+的摩尔质量是1 g/mol;
C、H+的摩尔质量是1;D、H+的摩尔质量是1 mol。
8、属于共价化合物的是:A、NH4NO3;B、H2SO4;C、Cl2;D、Mg(NO3)2。
*9、银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
![]()
在此电池放电时,负极上发生反应的物质是:
(A)Ag;(B)Zn(OH)2;(C)Ag2O;(D)Zn。
![]() 10、与CH3CH2CH=CH2互为同分异构体的是:
10、与CH3CH2CH=CH2互为同分异构体的是:
![]() A、 B、
A、 B、
![]()
![]() C、
D、
C、
D、
11、下列各组中的物质,一定互为同系物的是:
A、CH4和C3H8;B、C4H6和C5H8;C、C6H6和C2H2;D、C2H4和C5H10。
12、为了除去FeSO4溶液中的CuSO4杂质,应加入:A、铁粉;B、铝粉;C、镁粉;D、锌粉。
13、下列物质在常温下能与二氧化硅反应的是:
A、水;B、盐酸;C、氢氧化钠溶液;D、氧化钙。
14、下列物质置于空气中,颜色会发生变化的是:A、Al2O3;B、MgO;C、Fe2O3;D、Fe(OH)2。
15、下列有机物的命名正确的是:
A、3,3-二甲基丁烷;B、2-甲基丁烷;C、2,3-二乙基戊烷;D、2,5-二甲基戊烷。
16、用一种试剂区别MgCl2、Al2(SO4)3、NaCl、(NH4)2SO4四种溶液,这种试剂可以是
A、氨水;B、BaCl2溶液;C、AgNO3溶液;D、NaOH溶液。
17、下列变化,可通过消去反应实现的是:
A、CH3CH2OH→CH3CHO;B、CH3CH2OH→CH3CH2OCH2CH3;
C、CH3CH2OH→CH2=CH2;D、CH3CH2OH→CH3CH2Cl。
*18、利用家庭生活用品可以进行某些科学实验,下列哪一实验只需厨房用品就可简便地完成:
A、检验食盐中是否含碘元素;B、检验自来水中是否含有Cl-;
C、蛋白质的盐析和溶解;D、检验白酒中是否含有甲醇。
19、在实验室进行下列实验时,需用水浴加热的是:
A、由酒精制乙烯;B、由苯制硝基苯;C、由苯制溴苯;D、蒸馏石油。
20、下列各组离子中,在水溶液中能大量共存的是:A、Al3+、Mg2+、OH-、Cl-;B、Fe3+、Cu2+、SCN- 、SO42-;C、C6H5O-、Cl-、Na+、H+;D、AlO2-、OH-、K+、Na+。
21、下列叙述正确的是:A、通常把铝粉和氧化铁的混合物叫铝热剂;B、某物质中只含有一种元素,该物质一定是纯净物;C、40K和40Ca的中子数相等、质子数不相等;
D、乙烯分子中碳碳双键的键能是乙烷分子中碳碳单键键能的两倍。
22、下列物质不能与氢氧化钠溶液反应的是:A、苯酚;B、乙醇;C、乙酸;D、乙酸甲酯。
23、下列性质的比较,错误的是:
A、稳定性:HI<HBr<HCl<HF; B、酸性:H2SiO3<H3PO4<H2SO4<HClO4;
C、原子半径:O<F<Na<Mg; D、氧化性:K+<Fe2+<Cu2+<Ag+。
24、某元素的一价阴离子,核外有10个电子,质量数为19,则中子数为:
A、9;B、10;C、11;D、12。
25、X、Y两元素能形成多种化合物,已知化合物X2Y中,X和Y的质量比为7:5,则X和Y质量比符合7:15的化合物是:A、XY2;B、X2Y3;C、X3Y2;D、X2Y5。
26、根据下列反应:(1)2Fe3++2I-=2Fe2++I2;(2)Br2+2Fe2+=2Br-+2Fe3+,判断离子的还原性由强到弱的顺序是:A、Br->I->Fe2+;B、I->Fe2+>Br-;C、Fe2+>I->Br-;D、Br->Fe2+>I-。
*27、下列化学反应的实验现象描述错误的是:
A、淀粉、纤维素、蛋白质都是天然高分子化合物;B、红磷在氯气中燃烧产生白色烟雾;
C、醋酸溶液中加入稀硫酸,溶液的pH值减小;D、氢气在氯气中燃烧产生淡蓝色火焰。
28、加热碳酸镁和氧化镁的混合物m g,使之完全反应,得到剩余物ng。则原混合物中氧化镁的质量分数为:A、![]() ;B、
;B、![]() ;
;
C、![]() ;D、
;D、![]() 。
。
29、下列离子方程式正确的是:
A、碳酸氢铵溶液中加入足量氢氧化钠溶液:NH4+ +OH-=NH3↑+H2O;
B、乙酸乙酯与氢氧化钠溶液共热:CH3COOCH2CH3+OH-![]() CH3COO- +CH3CH2OH;
CH3COO- +CH3CH2OH;
C、盐酸溶液中加入碳酸镁:CO32-+2H+=CO2↑+H2O;
![]() D、氯化亚铁溶液中通入足量氯气:Fe2++Cl2=Fe3++2Cl-;
D、氯化亚铁溶液中通入足量氯气:Fe2++Cl2=Fe3++2Cl-;
![]() 30、某有机物的分子式为C5H11Cl,其分子结构中含有2个—CH3、2个—CH2—、1个
。具有这种结构的同分异构体共有:A、2个;B、3个;C、4个;D、5个。
30、某有机物的分子式为C5H11Cl,其分子结构中含有2个—CH3、2个—CH2—、1个
。具有这种结构的同分异构体共有:A、2个;B、3个;C、4个;D、5个。
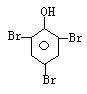
31、某草药中有一种色素,它的结构简式为 ,用它制成的试剂可以检验物质的酸碱性。能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是:
A、3mol、5mol;B、6mol、8mol;C、10mol、8mol;D、6mol、10mol;
32、某烃与乙烷的混合气体1.344L(标准状况下)在足量的O2中完全燃烧,所得气体通入300mL0.4mol/LNaOH溶液中完全吸收,将吸收液低温蒸干得到固体7.6g。该烃为:
A、甲烷;B、乙烯;C、乙炔;D、丙烷。
二、填空题(本题有4小题,共16分。)
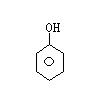
33.写出下列反应的化学方程式:*(1)金属铜溶解在稀硝酸中_______________________。
(2)苯酚溶液中加入过量浓溴水 ▲ 。
(3)氯化铝溶液中滴加过量氨水(写离子方程式) ▲ 。
34、某冶炼厂的废渣经处理后含有铁、银、氧化铝三种物质,经加工后可制得多种化工产品。加工的主要流程如下:试写出产品的化学式:A ▲ 、B ▲ 、C ▲ 。
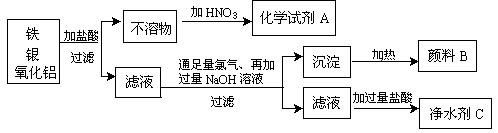
35.A是一种对位二取代苯,相对分子质量为180,A水解生成B和C两种酸性化合物。B的相对分子质量为60;C能与NaHCO3溶液反应,并能使FeCl3溶液显色。试写出A的结构简式 ▲ 。
36.一定质量Fe和Fe2O3的混合物投入250mL2.0mol/L的HNO3溶液中,固体完全溶解后,在标准状况时得到1.12LNO(假设HNO3的还原产物仅此一种)。要使反应后溶液中的铁元素全部沉淀下来,最少需加入1、0 mol/L 的NaOH溶液 ▲ mL。
三、简答题(本题有2小题,共8分。)
37.下列操作正确的是 ▲ 。A、实验室蒸馏石油时,将温度计的水银球插入液面下;
B、稀释浓硫酸时,将浓硫酸慢慢注入盛有水的量筒内并不断用玻璃棒搅拌;
C、用蒸发皿蒸发液体时,未垫上石棉网直接加热蒸发皿;
D、配制一定物质的量浓度的溶液时,清洗后未经干燥的容量瓶直接用于实验。
38.某同学在学习乙醇的知识后,设计了如下的实验。
操作步骤为:①在试管里加入2mL乙醇;②把一端弯成螺旋状的铜丝放在酒精灯外焰中加热;
③立即将铜丝插入盛有乙醇的试管里(如图),反复操作几次;④闻生成物的气味,观察铜丝表面的变化。试回答下列问题:⑴该实验的目的是 ▲ ;⑵第④步操作中,能闻到 ▲ 气味;
⑶写出反应的化学方程式 ▲ 。
四.计算题(本题有2小题,共12分。)
39.将足量的铝粉投入到100mL 1.0mol/L的硫酸中,充分反应后能得到标准状况下的氢气多少升?
40.两种烃的衍生物A和B,所含碳、氢、氧三种元素的质量比均为6:1:4。完全燃烧0.1molA,可生成3.6g水。B只含一个醛基,1.1gB与足量银氨溶液反应,可析出2.7g银。
(1)求A、B的分子式。
(2)若B能与酸发生酯化反应,且主链含3个碳原子,写出其可能的结构简式。
说明:打有*号的题为编者改动的。
浙 江 省 2002年 高 中 证 书 会 考
化学参考答案和评分标准
说明:本卷最小采分点为1分,没有0、5分。
一、 选择题(每小题2分,共64分,不选、多选、错选均不给分。)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | C | A | C | B | A | A | B | B | D | A | A | A | C | D | B | D |
| 题号 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | 32 |
| 答案 | C | C | B | D | A | B | C | B | B | B | D | B | B | C | D | A |
二、填空题(本大题共16分。)
| 题 号 | 参 考 答 案 | 分数 | 评分意见 |
|
| ⑴CH3COONa + NaOH | 2 |
化学符号写错不给分,条件错或未配平给1分。
⑶中写化学方程式不给分。 |
| ⑵ + 3Br2 | 2 | ||
| ⑶ Al3+ + 3NH3·H2O = Al(OH)3↓ + 3NH4+ | 2 | ||
| 34 | A:AgNO3 B:Fe2O3 C:AlCl3 | 6 | 每空2分。C填AlCl3和NaCl同样给分。(只填NaCl不给分) |
|
|
| 2 | |
| 36 | 450 | 2 |
三、简答题(本大题共8分)
| 题号 | 参 考 答 案 | 分数 | 评分意见 | |
| 37 | C D | 2 | 只选1个且正确的给1分,错选、多选均不给分。 | |
|
| ⑴ | 验证乙醇在加热和铜作催化剂条件下,能被空气氧化成乙醛。 | 2 | 该题属于“开放题”,其他表述只要合理也给分。 合理的也给分。 |
| ⑵ | 刺激性 | 2 | ||
| ⑶ | 2CH3CH2OH + O2 | 2 | 分步写出方程式同样给分。 | |
四、计算题(本大题共12分。第39小题5分,第40小题7分)
| 题号 | 参 考 答 案 | 分数 | 评分意见 | ||||||
|
| 解:n(H2SO4) = 0、1L×1、0mol/L = 0、1 mol 2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑ 3mol 3×22、4L 0、1mol V (H2) 答:能得到标准状况下的氢气2、24L。 | 1 2 2 | 计算过程不带单位不扣分。 用其他方法计算,只要步骤合理、结果正确,可参考分步计分给分。 | ||||||
|
| 解:⑴ N (C) : N (H) : N (O) = A、 B的最简式为C2H4O 设A、B的分子式分别为(C2H4O)m、(C2H4O)n 则 (C2H4O)m ~ 2m H2O 1 2m 0、1mol m = A的分子式为C2H4O。 因为B只含1个醛基, 则(C2H4O)n ~ 2 Ag 44n 2 1、1g 2、7g n = B的分子式为C4H8O2 ⑵ B能与酸发生酯化反应,说明含有羟基,B可 能的结构简式: OH HO—CH2—CH—CHO CH3—C—CHO CH3 CH3 | 1 1 1 1 1 2 | 求分子式没有计算过程不给分。 计算过程不带单位不扣分。 用其他方法计算,只要步骤合理、结果正确,可参考分步计分给分。 |
 33
33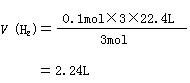 39
39