高中证书会考化学试题(春季)
相对原子质量:H-1;C-12;O-16;Al-27;Fe-56;Cu-64。
一、 选择题(本题有32小题,共64分。每小题只有一个选项符合题意。)
1.( )下列变化属于物理变化的是:A.石油分馏;B.煤的干馏;C.油脂硬化;D.石油裂化。
2.( )下列单质中,通常用于制造半导体材料的是:A.金刚石;B.晶体硅;C.铁;D.铝。
3.( )下列物质中,属于有机物的是:A.CO;B.NH4HCO3;C.H2CO3;D.CH3CH2OH。
4.( )下列分子的空间结构为正四面体的是:A.甲烷; B.乙烯; C.乙炔; D.苯。
5.( )下列物质中不属于高炉炼铁原料的是:A.铁矿石; B.焦炭; C.水; D.空气。
6.( )既能跟强酸溶液反应,又能与强碱溶液反应,且生成的产物都是盐和水的物质是:
A. Na2CO3;B.MgO;C.Al;D.Al2O3。
7.( )下列物质属于羧酸的是:A.CH3COOH;B.CH3CHO;C.HCOOCH3;D.HOCOOH。
8.( )下列物质中能跟氢氧化钠溶液起反应的是:A.苯酚;B.乙醇;C.乙烷;D.苯。
9.( )烯烃的通式为:A.CnH2n+2; B.CnH2n; C.CnH2n-2; D.CnH2n-6。
10.( )下列物质中滴入氯化铁溶液显紫色的是:
A.氯水; B、苯酚溶液; C、KSCN溶液; D、NaOH溶液。
11.( )下列关于有机物的命名,不正确的是:
A、2-甲基戊烷; B、2,2-二甲基丁烷;C、3,4-二甲基戊烷; D、3-乙基戊烷。
12.( )铝不易被腐蚀,其主要原因是因为铝:A、是一种轻金属;B、金属活动性比镁弱;
C、具有高熔点; D、易形成致密的氧化物薄膜。
13.( )苯的硝化属于:A、取代反应;B、加成反应;C、加聚反应;D、消去反应。
14.( )能将苯、甲苯区别出来的试剂是:
A、水;B、溴水;C、KMnO4酸性溶液;D、氢氧化钠溶液。
15.( )将铁粉投入稀硝酸中,充分反应后还剩余少量铁粉,反应后溶液中含量较多的阳离子是:A.Fe3+;B.Fe2+;C.Fe2+、H+;D.Fe2+、Fe3+。
16.( )常温下,既能使高锰酸钾酸性溶液褪色,又能使溴水褪色的是:
A、 乙烷;B、乙醇;C、苯;D、乙烯。
17.( )下列物质属于酸性氧化物的是:A.Al2O3;B.MgO;C.Fe2O3;D.SiO2。
18.( )铁红是指下列物质中的:A.Fe(OH) 2;B.Fe2O3;C.Fe(OH)3;D.Fe3O4。
19.( )镁铝合金投入盐酸中,待完全溶解后,再加入过量氢氧化钠溶液,得到的沉淀是:
A. Mg(OH) 2;B.Al(OH) 3;C.NaAlO2;D.MgO。
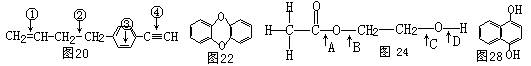
20.( )下面物质中四种碳碳键长(见附图),由长到短的次序为:
A.②>①>④>③;B.①>②>④>③;C.②>③>①>④;D.②>①>③>④。
21.( )有关油脂的说法错误的是:
A、 油脂的化学成分是高级脂肪酸的甘油酯; B、油脂的水解叫皂化反应;
C、植物油可使溴水褪色; D、油脂的硬化是加成反应。
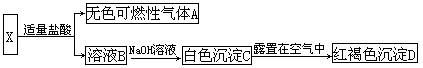
22.( )欧洲四国受“二恶英”污染的畜禽类制品、乳制品等,曾引发涉及全世界的食品安全危机。我国也发出过紧急通知,禁售上述食品。“二恶英”是二苯基1,4-二氧六环及其衍生物的通称。下列关于二苯基1,4-二氧六环(见附图)的叙述正确的是:
A. 属于芳香烃;B.相对分子质量为184;C.分子式为C12H10O; D.不能发生取代反应。
23.( )下列物质一定互为同系物的是:
A.CH4和C3H8; B.C2H4和C4H8; C.CH2O2和C2H4O2; D.C3H4和C4H6。
24.( )将下列有机物放入稀硫酸溶液中加热,发生断裂的键主要是:(见附图)
25.( )下列离子方程式正确的是:A.铝粉投入到氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑;
B. 二氧化硅与氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O;
C. 氢氧化铁与盐酸反应:OH-+H+=H2O;
D.碳酸镁与稀硫酸反应:CO32-+2H+=CO2↑+H2O。
26.( )等物质的量的下列醇完全酯化时,需醋酸最多的是:
A.乙醇; B.乙二醇; C.丙三醇; D.甲醇。
27.( )下列除杂方法中不正确的是:
A. SiO2中的CaCO3,加盐酸,过滤; B.FeCl2溶液中的CuCl2,加铁粉,过滤;
C.NaCl中的SiO2,加水溶解,过滤并将溶液蒸发结晶;D.SiO2中的CaO,通过加热熔融而除去。
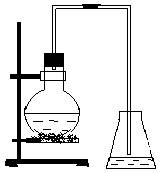
28.( )已知某有机物的结构简式为(见附图),X为该有机物苯环上的一溴代物,则X可能的结构式有:A.2种;B.种;C.4种;D.5种。
29.( )下列各组离子在水溶液中能大量共存的是:A.Ca2+、Mg2+、Cl-、NO3-;
B.Al3+、K+、SO42-、OH-; C.Fe2+、Na+、SO42-、S2-; D.Na+、H+、CO32-、SO42-。
30.( )化学式为C7H12的链烃,其结构简式中不可能:
A.只有一个“-CH3”;B.只有一个“C=C”;C.只有一个“C≡C”;D.有5个“-CH2-”。
31.( )将一定量的某醇分成两等份,取一份完全燃烧可生成0.2mol二氧化碳,另一份与足量的金属钠反应生成0.1mol氢气。则该醇可能是:A.甲醇;B.乙醇;C.丙二醇;D.丙醇。
32.( )将0.12mol某烷烃与0.78molO2混合在密闭容器中引燃,反应结束后,产物中有CO,若再向原容器中通入0.36molO2,并使之进一步反应,完全反应后,容器中还有O2剩余,则该烷烃可能是:A.丙烷;B.丁烷;C.戊烷;D.已烷。
二、 填空题(本题有4小题,共16分)
33.写出下列反应的化学方程式:
⑴有镍催化剂存在并加热到180~250℃的条件下,苯与氢气反应____________________;⑵苯酚溶液与过量的浓溴水反应_______________________________________________;
⑶氯化铝溶液与过量的氨水反应(写离子方程式)_________________________________。
34.某金属X,为了确定其成分,进行一系列实验,实验过程和发生的现象如下图所示:
⑴写出金属X的化学式__________;⑵写出溶液B中溶质的化学式_______________;
⑶写出白色沉淀C转变为红褐色沉淀D的化学方程式
__________________________________________________________________ 。
35.有机物A经过一系列反应可以转变为有机物E、F,转变的关系如下:
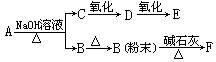
已知A与含等物质的量NaOH的水溶液反应生成等物质的量B和C;E为一元羧酸,含3.7gE的溶液50mL恰好中和0.5mol/LNaOH溶液100mL;F是气体,测得在标准状况下密度为0.717g/L。则A、D的结构简式为:A______________,D______________。
36.在托盘天平的两端各放一只盛有等量稀硫酸(均含H2SO4 n mol)的烧杯,此时天平平衡。向一只烧杯中加入ag铁,向另一只烧杯中加入bg铝,充分反应后,一只烧杯中金属有剩余,此时天平仍保持平衡。则a与b的关系是:a= ___________。
三、简答题(本题有2小题,共8分)
37.实验室可用苯和液溴反应制取少量溴苯(铁作催化剂),其装置如图所示。⑴写出制取溴苯的化学方程式________________________________________________;
⑵实验中使用的导气管较长,其中跟烧瓶口垂直的一段导管除导气外,还兼起________________作用。
38.某无色溶液中,可能含有大量的K+、H+、CO32-、Cl-中的某些离子(除上述离子外,不存在其它离子)。它能跟铝屑反应产生氢气,在反应后的溶液中加入过量的氨水,有白色沉淀生成。则上述离子中,一定存在的离子是__________________________________;
一定不存在的离子是_____________________________________;
可能存在的离子是______________________________________;
该溶液与铝屑反应的离子方程式是__________________________________________。
三、 计算题(本题有2小题,共12分)
39.已知某种链烃含碳的质量分数为85.7%,含氢的质量分数为14.3%,在标准状况下它的1.875g/L。试求该烃的分子式,并写出它的结构简式。
40.将一定量的铁粉加入500mL Fe2(SO4)3和CuSO4的混合溶液中,恰好完全反应,反应前后溶液的质量不变。要使溶液中SO42-完全沉淀,需加入2.0mol/L的BaCl2溶液500mL。求:⑴原溶液中SO42-离子的物质的量浓度。⑵加入铁粉的质量。
高中证书会考化学试题(春季)参考答案
1、A;2、B;3、D;4、A;5、C;6、D;7、A;8、A;9、B;10、B;11、C;12、D;13、A;14、C;15、B;16、D;17、D;18、B;19、A;20、C;21、B;22、B;23、A;24、A;25、B;26、C;27、D;28、B;29、A;30、B;31、A;32、C。
33、略。34、⑴Fe;⑵FeCl2;⑶4Fe(OH)2+2H2O+O2=4Fe(OH)3。
35、A、CH3COOCH2CH2CH3;D、CH3CH2CHO。36、28(b-3n)/27。
37、⑴略;⑵冷凝回流。
38、一定存在的离子是H+、Cl-;一定不存在的离子是CO32-;可能存在的离子是K+;
离子方程式:2Al+6H+=2Al3++3H2↑。
39、分子式为C3H6;结构简式为CH2=CHCH3。
40、⑴2mol/L;⑵4.48g。