高二化学第一学期期末考试5
高 二 化 学
可能用到的相对原子质量:
H―1 C―12 N―14 O―16 Na―23 Mg―24 Al―27 P―31
S―32 Cl―35.5 K―39 Ca―40 Fe―56 Cu―64 Zn―65 Br―80
Ag―108 Ba―137
一、 选择题(每小题有1个选项符合题意)
1.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中的石墨电极
2.将AlCl3溶液和NaAlO2溶液分别蒸干并灼烧,所得产物主要成分为
A.都是Al(OH)3 B.前者是Al2O3,后者是NaAlO2
C.都是Al2O3 D.前者是AlCl3,后者是NaAlO2
3.在pH=1的某溶液中,可能存在NO3-、I-、Fe3+、Na+中的一种或两种,向该溶液中滴入Br2水,单质Br2被还原,由此推断该溶液中可能存在的离子为
A.只有NO3-、Fe3+ B.只有I-、Na+
C.只有I-、Fe3+ D.只有NO3-、Na+
4.下列叙述正确的是
A.分子式相同,各元素百分含量也相同的物质是同种物质
B.通式相同的不同物质一定属于同系物
C.分子式相同的不同物质一定是同分异构体
D.相对分子质量相同的不同物质一定是同分异构体
5.把m mol C2H4和n mol H2 混合于密闭容器中,在适当的条件下生成了p mol C2H6, 若将所得的混合气体完全燃烧生成CO2和H2O,则需O2
A.3.5p mol B.(3m+n/2) mol C.(3m+n) mol D.(3m+n/2-3p) mol
6.一定量的甲烷与10 mol Cl2发生取代反应,若四种取代产物物质的量相等,则消耗甲烷的物质的量为
A.0.5mol B.2mol C.2.5mol D.4mol
7.关于制取乙烯的实验,下列说法中正确的是
A.反应物是乙醇与过量的6mol/L H2SO4溶液的混合物
B.反应容器中应加几片碎瓷片
C.温度计插入反应液液面以下,温度控制在140℃
D.实验完毕应先熄灭酒精灯火焰,再从水中取出导管。
8.A、B两种有机物的混合物,当混合物的质量一定时,无论A、B以何种比例混合,完全燃烧产生CO2的量均相等。A、B可能是①同分异构体②同系物③具有相同的最简式④含碳的质量分数相同,符合上述组合条件的是
 A.①②④ B.①③④ C.②③④ D.①②③
A.①②④ B.①③④ C.②③④ D.①②③
9.盆烯是近年合成的一种有机物,它的分子结构可简化表示为
(其中C、H原子已略去),下列关于盆烯的说法中错误的是
A. 盆烯是苯的一种同分异构体
B. 盆烯分子中所有的碳原子不可能在同一平面上
C. 盆烯是乙烯的一种同系物
D.盆烯在一定条件下可以发生加成反应
10.久置于空气中的下列物质,因被氧化而呈黄色的是
A.浓硝酸 B.氯化亚铁溶液 C.溴苯 D.溴化银
二.选择题(每小题有1至2个选项符合题意)
11.下列数据是有机物的式量,可能互为同系物的一组是
A.16、28、40、52 B.16、30、58、72
C.16、30、44、58 D.16、32、48、54
12.下列各组分子中的各个原子,或者处于同一平面,或者在一条直线上的是
![]() A.C6H6、 C2H4 、 CO2 B.CO2、HCl、 HC C CH3
A.C6H6、 C2H4 、 CO2 B.CO2、HCl、 HC C CH3
C.CH 、 HCl、 CH4 D.CO2、HCl、C2H2
13.在实验室中,下列除杂的方法正确的是
A. 溴苯中混有溴,加入Kl溶液,振荡,用汽油萃取出溴
B. 乙烷中混有乙烯,通H2在一定条件下反应,使乙烯转化为乙烷
C. 硝基苯中混有浓H2SO4和浓HNO3,将其倒入NaOH溶液中,静置,分液
D.乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶。
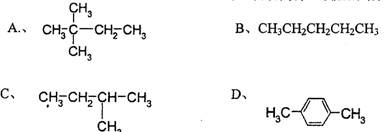
14.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下)。它在光照条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式是
15.将a g Fe2O3和Al2O3样品溶解在过量的200mL pH=1的硫酸溶液中,然后向其中加入NaOH溶液使Fe3+和Al3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度
A.0.1mol/L B.0.2mol/L C.0.4mol/L D.0.8mol/L
16.实验室中,某学生先用蒸馏水润湿pH试纸(每项使用时润湿程度相同),然后用洁净干燥的玻璃棒蘸取试液测定试液的pH,下列说法正确的是
A. 该生的测定值一定有误差产生。
B. 当溶液为中性时,该生的测定值不会有误差,一定是纯水。
C. 用此方法检测C(H+)相等的盐酸和醋酸两溶液是盐酸的pH比醋酸小
D.用此方法检测C(H+)相等的盐酸两溶液是醋酸的pH比盐酸小。
17.在120℃时,1体积甲烷和丁烯的混合物与4体积氧气在密闭容器中充分燃烧,反应后恢复到原温度,压强增加为原来的1.1倍,则混合气体中丁烯的体积分数是
A.20% B.40% C.50% D.95%
18.燃料电池是燃料氧气或空气起反应,将化学能转变为电能的装置,下列关于甲醇燃料电池(电解液为强酸溶液)的说法中,正确的是
A. 极反应为:CH3OH+H2O-6e-=CO2+6H+
B. 正极反应为:O2+2H2O+4e-=4OH-
C. 随着放电的进行,溶液中的阳离子向正极移动
D.随着放电的进行,溶液的pH不变
19.要鉴别已烯中是否混有少量甲苯,正确的实验方法是
A. 先加足量的酸性高锰酸钾溶液,然后再加入溴水
B. 先加足量溴水,然后再加入酸性高锰酸钾溶液
C. 点燃这种液体,然后再观察火焰的颜色
D.加入浓硫酸与浓硝酸后加热
20.某烃具有同一类别的两种或两种以上的同分异构体,在同分异构体中的某一种只能有一种一氯代物,这种烃可以是
①具有7个碳原子的芳香烃 ②具有4个碳原子的烷烃 ③具有5个碳原子的烷烃 ④具有6个碳原子的烷烃 ⑤具有8个碳原子的烷烃
A.①③ B.③④⑤ C.仅③⑤ D.②③④⑤
三.填空题
21.下列有机物按系统命名法命名

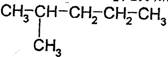 22.某炔烃与过量H2充分加成后得到的化合物的结构简式为:
22.某炔烃与过量H2充分加成后得到的化合物的结构简式为:
此炔烃的结构简式为_______________________。
23.为了除去下列物质中所含有杂质(括号内),将所加的试剂填入下表。
| 混合物 | 试剂 |
| (1)甲烷(乙烯) | |
| (2)乙炔(H2S) | |
| (3)乙烯(SO2) |
![]()
24.试由乙炔和其他无机小分子为原料合成 (聚氯乙烯),请用化学方程式表示。
25.有人提出苯的结构还可能有两种具有三维空间的立体结构。

(I) (II)
![]() (1)若苯的结构为(I),问它与 结构在下列各项中的哪些方面不同?
(1)若苯的结构为(I),问它与 结构在下列各项中的哪些方面不同?
A. 一氯代物种数 B.二氯代物种数 C.与溴水作用 D.含碳量
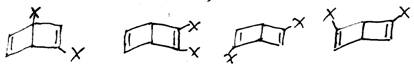
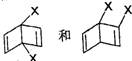 (2)在结构(II)分子中引入2个“-X”基因,可形成的同分异构体除
(2)在结构(II)分子中引入2个“-X”基因,可形成的同分异构体除
,还有多种同分异构体,
请写出其中的另四种_________________________。
26、下列实验不能达到预期目的的是
A、用托盘天平称量50.56g氯化钾。
B、用 10mL量筒量取5.0mL稀H2SO4
C、用碱式滴定管量取18.5mL 1mol・L-1的NaOH溶液
D、现需200mL 0.1mol・L-1的Na2CO3溶液,可用250mL容量瓶配制
E、用50mL酸式滴定管量取25mL稀盐酸的操作是:将盐酸加入酸式滴定管使凹液面正好与25mL刻度相切,将溶液全部放入燃杯,可准确量取25mL稀盐酸。
F、用pH试纸检验溶液碱性的操作是,先取一块试纸放在表面皿或玻璃片上,用沾有待测液的玻璃棒点在试纸中部,观察颜色的改变并在半分钟内与标准比色卡对比,确定溶液的pH。
27.简答下面有关标准氢氧化钠溶液滴定测盐酸的问题。
(1)盛放待测盐酸的锥形瓶下放垫一张白纸的作用是_________________。
(2)用酚酞作指示剂,滴定到达终点时,溶液的颜色变化是_____________。
(3)有下列错误操作:①碱式滴定管用蒸馏水洗净后,未经标准溶液润洗就注入标准氢氧化钠溶液;②用酸式滴定管取用待测酸液前,尖嘴部分有气泡,取用过程中气泡消失;③滴定前,读碱液体积时视线低于碱式滴定中的液面;滴定后,读出碱液体积时,视线高于碱式滴定管中的液面;④锥形瓶用待测酸液润洗两次。
①哪些错误操作会使盐酸浓度的测定值偏低?(填序号)____________。
②哪些错误操作会使盐酸浓度的测定值偏高?(填序号)______________________。
四.计算题
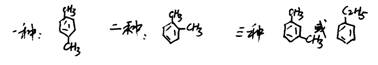
28.某烃含碳90.6%,其蒸气与空气密度比值为3.66,则写出其分子式和下列情况下该烃结构简式为:
(1) 若该烃硝化时,一硝基取代物只有一种
(2) 若该烃硝化时,一硝基取代物只有两种
(3) 若该烃硝化时,一硝基取代物有三种
(以上均苯环上的H被取代)
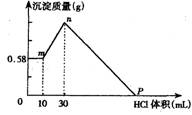 29.把有NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀析出,向所得的浊液里,逐滴加入0.5mol・L-1的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:
29.把有NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58g白色沉淀析出,向所得的浊液里,逐滴加入0.5mol・L-1的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:
(1) 混合物中NaOH的质量是_______g,AlCl3的质量是__________g,MgCl2的质量是________________ g。
(2) P点所表示盐酸加入体积是_____________mL。
【参考答案】
一.选择题
1.B 2.B 3.B 4.C 5.B 6.D 7. B 8.B 9.C 10.B
二.选择题
11.BC 12.AD 13.CD 14.B 15.B 16.D 17.C 18.AC 19.B 20.C
三.填空题
21. 2,2-二甲基丙烷 2,4-二甲荃- 4 - 乙基庚烷
22.
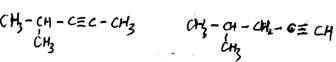
23.
| 试 剂 | ||
| 溴水 | ||
| NaOH 溶液 | ||
| NaOH 溶液 |
24.
![]()
 25.
25.
26. AE
27. (1)变色明显准确 (2)无色变为浅红色 (3)②③ ①④
 28.
28.
29. (1) 2.6 1.335 0.95
(2). 130