上学期期末考试题
高二化学(非化学班用)
(命题人:叶月丽 审题人:詹海东)
第Ⅰ卷 选择题(共60分)
可能用到的原子量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5 Fe:56 Cu:64 Zn:65
一、选择题(本题包括30小题,每小题只有一个正确答案,每小题2分共60分)
1、金属具有优良的导热性,原因是
A.金属受热时易熔化为液态,液体易流动,传热性能好
B.金属离子有优良的导热性能
C.热量易在金属内部形成对流
D.自由电子受热时能量增加,运动速度加快,通过碰撞将能量
传递给其它金属离子或电子
2、利用铝合金代替铝制钥匙是利用铝合金的
A.熔点低 B.不易锈蚀
C.硬度大 D.密度小
3、我国最新报道的高温超导体中,铊是组成成分之一,已知铊与铝是同族元素,关于铊的判断错误的是
A.铊是质软的银白色的金属
B.铊能生成+5价化合物
C.铊能置换出盐酸中的氢
D.铊能与氧气发生反应
4、目前已经发现和通过人工合成的有机物有一千多万种。有机物种类繁多的主要原因是:
A.碳元素可以与许多其它元素结合而形成化合物;
B.有机物不但存在于动植物体内,而且可以通过人工的方法合成;
C.碳元素在自然界中的含量丰富,故形成化合物的种类多;
D.碳原子含有4个价电子,可以跟其它原子形成4个共价健,也可以在碳原子跟碳
原子间形成共价键,从而形成长的碳链。
5、下列物质中,不能用单质直接化合而得到的是:
A FeCl3 B FeCl2
C FeS D Fe3O4
6、下列烷烃的一氯代物没有同分异构体的是:
A 2-甲基丙烷 B 丙烷
C 丁烷 D 乙烷
7、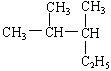 的名称是
的名称是
A 2—甲基—3—乙基丁烷 B 3,4—二甲基戊烷
C 2,3—二甲基—4—乙基丙烷 D 2,3—二甲基戊烷
8、下列叙述中错误的是:
A.点燃甲烷不必象点燃氢气那样事先验纯;
B.甲烷燃烧能放出大量的热,所以是一种很好的气体燃烧;
C.煤矿的矿井要注意通风和严禁烟火,以防爆炸事故的发生;
D.如果隔绝空气,将甲烷加热到1000℃以上,能分解成炭黑和氢气。
9、下列物质①金刚石②四氯化碳③甲烷④氨气⑤乙烯⑥乙炔,分子具有正四面体型的是:
A.①②③ B.③④⑤
C.①③⑥ D.全部
10、区别CH4和C2H4的方法最好是:
A.比较它们在水中的溶解度大小;
B.嗅闻它们的气味;
C.通入溴水中观察溶液颜色的变化;
D.点燃它们后,观察火焰。
11、关于实验室制备乙烯的下列说法正确的是:
A.反应物是乙醇和过量的3mol/L H2SO4的混和液;
B.温度计插入反应溶液液面下,以便控制温度在140℃;
C.反应完毕 先灭火再从水中取出导管;
D.反应容器(烧瓶)中应加入少量瓷片。
12、下列混合气体一定比乙烯含碳百分率高的是( )
A.甲烷+乙烯 B.乙烷+乙炔
C.乙炔+乙烯 D.乙烯+丙烯
13.同系物具有:①相同的通式;②相同的最简式;③相同的物理性质;④相似的化学性质( )
A.①②④ B.①④
C.③④ D.②③
14.2,2,3,3,—四甲基戊烷的结构简式是
A.CH3(CH2)3CH3 B.(CH3CH2)2CHCH3
C.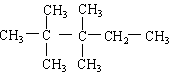 D.(CH3)3CC(CH3)3
D.(CH3)3CC(CH3)3
15、天然气、液化石油气燃烧的化学方程式分别为:![]() 、
、![]() 现有一套以天然气为燃料的灶具,改燃液化石油气,应采用的正确措施是:
现有一套以天然气为燃料的灶具,改燃液化石油气,应采用的正确措施是:
A.两种气体进入量都减少
B.增大空气进入量或减少液化气进入量
C.两种气体进入量都增大
D.减少空气进入量或增大液化气进入量
16、金属的下列性质中和金属晶体无关的是
A. 良好的导电性
B 反应中易失电子
C 良好的延展性
D.良好的导热性
17、称取两份铝粉,第一份加足量NaOH溶液,第二份加足量硫酸,如果要得到相同体积(同温同压)的氢气,两份铝粉的质量比是
A.1∶2 B.1∶3
C.3∶2 D.1∶1
18、两种金属粉末的混合物12g,投入足量的稀硫酸中,在标准状况下产生11.2 L气体,则这种混合物可能是
A.Zn、Al B.Fe、Zn
C.Al、Mg D.Mg、Cu
19、在金属晶体中,如果金属原子的价电子数越多,原子半径越小,金属的熔沸点越高,则下列各组金属熔沸点高低顺序正确的是
A.Mg>Al>Ca B.Al>Na>Li
C.Al>Mg>Ca D.Mg>Ba>Al
20、在下列反应中,光照对反应几乎没有影响的是:
A 氯气与氢气的反应
B 氯气与甲烷的反应
C 甲烷与氧气的反应
D 次氯酸的分解
21、物质的量浓度都是0.1摩/升的下列各溶液中,PH值最大的是:
A HCl B Al2(SO4)3
C H2SO4 D CH3COONa
22、下列化学方程式,书写不正确的是:
A 2Fe+6HCl = 2FeCl3+3H2↑
B 2Al+6HCl = 2AlCl3+3H2↑
C Al2O3+2NaOH = 2NaAlO2+H2O
D Fe+CuCl2 = FeCl2+Cu
23、A、B、C都是金属,把A放入C的盐溶液中,A的表面附着一层C;A与B组成原电池时,A为电池的正极。A、B、C三种金属的活动性顺序是:
A A>B>C B A>C>B
C B>A>C D B>C>A
24、只用一种试剂,可区别Na2SO4、MgSO4、AlCl3、NH4Cl四种溶液,这种试剂是:
A HCl B BaCl2
C AgNO3 D NaOH
25、下列各反应的化学方程式中,属于水解反应的是:
A H2O+H2O![]() H3O++OH-
H3O++OH-
B
HCO3-+OH-![]() H2O+CO32-
H2O+CO32-
C CO2+H2O![]() H2CO3
H2CO3
D
Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
26、对于达到平衡状态的可逆反应:N2+3H2![]() 2NH3(正反应为放热反应)下列叙述正确的是:
2NH3(正反应为放热反应)下列叙述正确的是:
A 反应物和生成物的浓度相等
B N2和H2的浓度之比一定为1:3
C 降低温度,平衡混合物里NH3的浓度增大
D 增大压强,不利于氨的合成
27、下列关于甲烷和乙烯的说法中,不正确的是:
A 它们所含元素的种类相同,但甲烷属饱和烃,乙烯属不饱和烃
B 甲烷与溴水发生取代反应,乙烯与溴水发生加成反应
C 甲烷和乙烯均能发生氧化反应
D 甲烷中碳的含量比乙烯中碳的含量小
28、下列关于乙炔性质的叙述中,既不同于乙烯,又不同于乙烷的是:
A 能燃烧生成二氧化碳和水
B 能发生加成反应
C 能与KMnO4发生氧化反应
D 能与氯化氢反应生成氯乙烯
29、用一定物质的量浓度的NaOH溶液,使物质的量浓度和体积均相同的FeSO4、Fe2(SO4)3溶液中的Fe2+、Fe3+完全沉淀,则所消耗的NaOH的体积之比为:
A 1:3 B 2:3
C 1:6 D 1:2
30、下列各组烃的混合物,只要总质量一定,无论它们按何种比例混合,完全燃烧后生成的CO2和H2O都是恒量的是( )
A C2H2、C2H4 B C2H4、C3H6
C C2H6、C3H8 D CH4、C2H2
上学期期末考试题
高二化学
(非化学班用)
第Ⅱ卷 非选择题(共40分)
班别_______姓名________________学号____________成绩______________
二、填空题(本题包括4小题,共13分)
31、(3分)衣服上沾有动、植物油污,用水洗不掉,但可用汽油洗去,这是因为大多数有机
物难 ________而易 ______。有机化工厂附近严禁火种,这是因为绝大多数
有机物__________________。
32、(3分)冶炼金属常用以下几种方法:①以C或CO、H2作还原剂还原(2②电解法③热分解法,现冶炼下列金属Al、Fe、Hg,试标明适宜的冶炼方法(填序号):
Al Fe Hg 。
33、(3分)把下列物质的相互关系填入下表中的空格中(填序号)
①同种物质 ②同位素 ③同系物 ④同素异形体 ⑤同分异构体
| 物质名称 | 相互关系 |
| 丙烷与2-甲基丙烷 | |
| 金刚石和石墨 | |
| 辛烷与壬烷 | |
| 氯仿与三氯甲烷 | |
| 氕、氘、氚 | |
| 新戊烷与2-甲基丁烷 |
34、(4分)现有①CH4、②C2H2、③C2H4、④C2H6、⑤C3H6五种有机物,等质量的以上物质
中,在相同状况下体积最大的是 ,同状况同体积的以上五种物质完全燃烧时消耗
氧气最多的是 生成二氧化碳最小的是 ,生成水最小的是 。(填序号)
三、实验题(本题包括2小题,共15分)
35、(6分)分别除去下列各种物质中的少量杂质,写出所用试剂的化学式:
| 物质 | 杂质 | 除杂试剂 |
| MgCl2 | MgCO3 | |
| FeCl2 | Cu2+ | |
| Fe | Al |
36、(9分)按要求写出下列反应的化学方程式及指出相应的反应类型:
| 要求 | 化学方程式(写主要反应) | 反应类型 |
| 甲烷和氯气混合光照 | ||
| 乙烯通入 溴水 | ||
| 氯乙烯制 聚氯乙烯 |
四.计算题(本题包括2小题,共12分)
36、(4分)取等质量的镁、铝合金,与足量的盐酸和NaOH溶液反应时,分别生成8.96L(标
况)和6.72L(标况)氢气,则该合金中镁、铝分别为:镁: mol 铝: mol
37、(8分)将11.2升(标准状况)乙烯和乙烷的混合气体通入足量的溴的四氯化碳溶液中,充分反应后,溴的四氯化碳溶液的质量增加了8.4g。求原气体混合物中乙烯与乙烷的物质的量和质量各为多少?
双向细目表
| 内容 | 识记 | 理解 | 应用 | 题型 | 分值 |
| 金属的通性 | √ | 选择 | 4 | ||
| 金属的冶炼 | √ | 填空 | 3 | ||
| 铝及其化合物的性质 | √ | √ | 选择、填空、计算 | 8 | |
| 铁及其化合物的性质 | √ | √ | 选择、填空 | 8 | |
| 金属与酸的反应 | √ | 选择、计算 | 4 | ||
| 有机物的特点 | √ | 选择、填空 | 5 | ||
| 同分异构体 | √ | 选择、填空 | 4 | ||
| 同系物及相关概念 | √ | 选择、填空 | 10 | ||
| 有机物的命名 | √ | 选择 | 4 | ||
| 甲烷的结构 | √ | 选择 | 2 | ||
| 甲烷的性质 | √ | 选择 | 6 | ||
| 乙烯的性质、制法 | √ | 选择 | 6 | ||
| 乙炔的性质 | √ | 选择 | 4 | ||
| 有机反应类型 | √ | 选择 | 3 | ||
| 有机反应方程式的书写 | √ | 填空 | 6 | ||
| 有机物的燃烧 | √ | √ | 选择、填空 | 7 | |
| 有机物混合计算 | √ | 计算 | 8 | ||
| 原电池 | √ | 选择 | 2 | ||
| 盐类水解 | √ | 选择 | 2 | ||
| 化学平衡 | √ | 选择 | 2 |
上学期期末考试题
(高二非化学班)
附答案:
一、选择题:(2分/题,共60分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| D | B | B | D | B | D | D | A | A | C |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| D | C | B | C | B | B | D | A | C | C |
| 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| D | A | C | D | B | C | B | D | A | B |
二、填空题(共13分)
31、(各1分共3分) 难溶于水 易溶于有机溶剂 易燃烧
32、(各1分共3分) ② ① ③
33、(各0.5分共3分) ③ ④ ③ ① ② ⑤
34、(各1分共4分) ① ⑤ ① ②
35、(各2分共6分)HCl Fe NaOH
36、(每条方程式各2分,反应类型各1分 共9分)
取代反应 加成反应 加聚反应
37、(各2分共4分)镁:0.1mol 铝:0.2mol
38、(各2分共4分)C2H4:0.3 mol 8.4g C2H6:0.2mol 6g