�߶��꼶��ѧ����ĩ�������ƻ�ѧ�Ծ�
����ʱ��Ϊ90���ӣ�����Ϊ100�֡�
�����õ���ԭ������C��12��H��1��O��16
һ������ѡ���⣨ÿ��ֻ��һ����ȷ�𰸣�ÿ��2�֣���40�֣�
1������ ����˵������ȷ����
A���� ������ɷǽ���Ԫ�ػ����ϳɵĻ��������ǹ��ۻ�����
B���� ������Һ���ȶ��ܵõ�����
C����ȥʳ����������NH4Cl���ӹ������ռ���Һ���������
D��������ȷֽⶼ������ʹ��ɫʯ���Ա���������
2����ȡ��ͬ������Cu(NO3)2ʱ��������������������
A�������� ͭ��ŨHNO3��ӦB��ͭ��ϡ���ᷴӦC������ͭ�����ᷴӦD��������ͭ�����ᷴӦ
3�����з�Ӧ�У�����ֻ���ֳ����Ե���
A.![]()
B.![]()
C.![]()
D.![]()
4����ҵ�����е�����������Ҫ�Ĵ�����ȾԴ֮һ����֪��3NO2+2NaOH=2NaNO3+NO+H2O��NO2+NO+2NaOH=2NaNO2+H2O����amolNO2��bmolNO�Ļ����������������NaOH��Һ�ܽ�����ȫ��������������������������ʵ�����������Ĺ�ϵ��
A��a=b/3���� ��B��2a=b���� ��C��a��b���� ��D��2a<b
5����NO2��NH3��O2�Ļ������22.4Lͨ��ϡ�����,��Һ����������26.7��,���������СΪ4.48L(����������ڱ�״���²ⶨ),ʣ��������ʹ�������ľ����ȼ,���������ƽ��������Ϊ
A��28.1������������ B��30.2���������� C��33.1�� ���� D��34.0
6��1.92gͭͶ��һ����ŨHNO3�У�ͭ��ȫ�ܽ⣬����������ɫԽ��Խdz�����ռ���672mL���壨��״���²ⶨ������ʢ�д����������������ˮ�У�ͨ��һ�������O2����״���£���ǡ��ʹ������ȫ����ˮ�У���ͨ��O2�������
A��504mL��������B��168mL��������C��336mL��������D��224mL
7���������ữ��CrO3���ƾ�������ɫ��Ӻ�ɫ��Ϊ����ɫ�������������Բ������˾���Ƿ�ƺ�����Ӧ�ķ���ʽΪ2CrO3 + 3C2H5OH + 3H2SO4 == Cr2(SO4)3 + 3CH3CHO + 6H2O���˷�Ӧ����������
��A����H2SO4���� (B)��CrO3����(C)��Cr2(SO4)3������(D)��C2H5OH
8�����з����廯���ﳣ���£�������ˮ����ȡ����Ӧ����
(A)��![]() ����(B)��
����(B)��![]() ����(C)��
����(C)��![]() ����(D)��
����(D)��![]()
9��ijЩ�����廯����ķ���ʽ��ΪC7H8O��������FeCl3��Һ��Ϻ�����ɫ�Ͳ�����ɫ������ֱ�Ϊ
(A)��2�ֺ�1�֡� ��B����2�ֺ�3�֡� (C)��3�ֺ�2�� (D)��3�ֺ�1��
10������ʽΪC8H16O2���л���A������������������ˮ������B��C����B��һ����������ת����C�����л���A�Ŀ��ܽṹ��
��A����1�֡� (B)��2�֡���(C)��3�֡���(D)��4��
11�����Ϊ1L��̼ԭ����Ϊx��x+1��������̬ϩ���Ļ����ڱ�״���£�������Ϊ2g����xֵ��
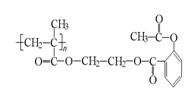 (A)��3��������(B)��4���� (C)��5��
(D)��6
(A)��3��������(B)��4���� (C)��5��
(D)��6
12��ijҩ��Ľṹ��ʽ����ͼ��������1 mol��������NaOH��Һ��Ӧ������NaOH�����ʵ���Ϊ
(A)��3 mol������(B)��4 mol��
(C)��3n mol���� (D)��4n mol
13���л��������ԭ�Ӽ䣨��ԭ����ԭ���ż䣩���Ӱ��ᵼ�����ʻ�ѧ���ʵIJ�ͬ�����и������ʵ��˵�������۵����
A���ױ���ʹ���Ը��������Һ��ɫ����������ʹ���Ը��������Һ��ɫ
B����ϩ�ܷ����ӳɷ�Ӧ�������鲻�ܷ����ӳɷ�Ӧ
C�����ӵ����Ա�������
D������ϩ����ˮֱ�ӾͿɷ�Ӧ����������ˮ��Ӧ����Ҫ��������
14��ij�л���Ľṹ��ʽΪ��![]() ������л���ɷ����ķ�Ӧ�����У�
������л���ɷ����ķ�Ӧ�����У�
��ȡ�� �ڼӳ� ����ȥ ������ ��ˮ�� ������ ������ ���к�
A���٢ڢۢݢޡ�(B)���ڢۢܢݢޢࡡ(C)���٢ڢۢܢݢޢࡡ(D)���٢ڢۢܢݢޢߢ�
15����ȫȼ��2.00g�л��������4.40gCO2��1.44gH2O������л���Ļ�ѧʽΪ
(A)��C5H8����(B)��C5H8O����(C)��C5H8O2����(D)��C10H16O4
16��ij�л�����������ȫȼ��ʱ�����������������O2�������������������CO2�����л��������
(A)��C2H2����(B)��CH3CHO���� (C)��CH3COOH���� (D)��C2H5OH
17�������й�ԭ��ص������У�����ȷ����
A��ԭ����У���Ի��õĽ�������Ϊ����
B���γ�ԭ���ʱ����������ԭ��Ӧ�ֱ����������Ϸ���
C��ԭ��ع���ʱ�����������ƶ�
D����������ļ�������
18������������ʴʱ�������Ϸ����ķ�ӦΪ
A��2Fe-4e=2Fe2+������ B��2Fe2++4e=2Fe
C��2H2O+O2+4e=4OH-����D��Fe3++e=Fe2+
19����ͼ�У�������Ϊ����������ʵ�����������Ϊ��ij��Һ�м��뷴Ӧ������ʵ��������У�1����2����3����4����Ӧ��Ӧ��ͼ�ηֱ���
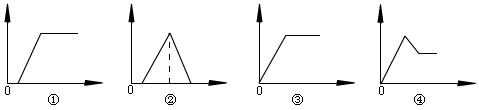 |
��1����������Һ�е���С�մ���Һ��������2��������NaOH��NaAlO2��Һ����μ���������������3��������KOH��KAlO2��Һ����μ���AlCl3��������4����MgCl2��AlCl3�Ļ����Һ����μ���NaOH��Һ������
A���٢ڢۢܡ�B���ܢۢ٢ڡ�C���ۢڢ٢ܡ�D���٢ڢܢ�
20��þ���������̻�����Ҫԭ��֮һ������þ��ʱ����þ������ij��������ȴ�������������Ϊ��ȴ�������
A�������������� B��������������C������� ���� D��������̼
�������������������������� ����⣨�������3С�⣬��30�֣�
21����6�֣���ͼ��ʾ��֪��
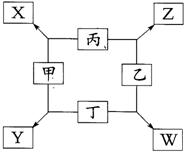 �ټס��ҡ���������Ϊǰ������Ԫ�صĵ��ʡ�
�ټס��ҡ���������Ϊǰ������Ԫ�صĵ��ʡ�
����һ�������¼�����ͼ��붡�������ʵ���
֮��1�U3��Ӧ���ֱ�����X��Y���ڲ�����
Ԫ�ؼ׳ʸ��ۡ�
����һ������������������붡�������ʵ���
֮��1�U2��Ӧ���ֱ�����Z��W���ڲ�����
Ԫ���ҳʸ��ۡ�
����գ���1������������������������������
��2���������Ӧ����X�Ļ�ѧ����ʽ�������������������������� ��
��3�����붡��Ӧ����W�Ļ�ѧ����ʽ���������������������������� ��
22����8�֣����У�A��CH3OH������B��(CH3)3CCH2OH������C��(CH3)3COH��
D��(CH3)2CHOH�� E��C6H5CH2OH������
��1����������ȩ����________��2��������ȥ��ϩ����_________________
��3����������ͪ����________��4��E����ᷢ��������Ӧ�IJ�����______________
23����16�֣�����������Ӧ��Ϣ��ȷ������������ķ�Ӧ���������������������������
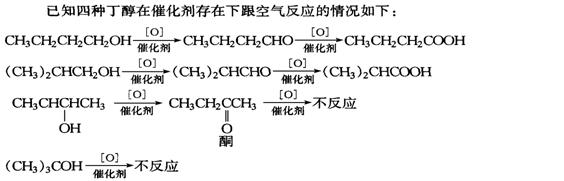
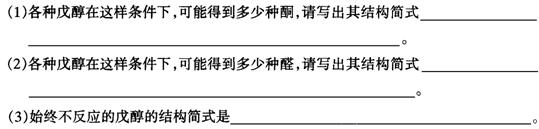
��������������������������
 ʵ���⣨�������2С�⣬��24�֣�
ʵ���⣨�������2С�⣬��24�֣�
24����14�֣���Ȫ��һ�ֳ�������Ȼ���������ԭ���Ǵ���ѹǿ���ͼΪ��ѧ��ѧ���õ���Ȫʵ��װ�á�����ƿ�г����������壬��ͷ�ιܼ��ձ��зֱ�ʢ��Һ�塣
(1)��������в������γ���Ȫ����__________
A��HCl��H2O B��O2��H2O��C��NH3��H2O�� D��CO2��NaOH��Һ
(2)ijѧ������˼��������Ȫ�������취���������������ͼ��ʾ��װ�á�
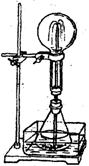 ��������ͼ����ƿ�У��ֱ�����������������ʣ���Ӧ����ܲ�����Ȫ������������
��������ͼ����ƿ�У��ֱ�����������������ʣ���Ӧ����ܲ�����Ȫ������������
A��Cu��ϡ���ᡡ������B��NaHCO3��NaOH��Һ
C��CaCO3��ϡ���ᡡ�� D��NH4HCO3��ϡ����
��������ͼ��ƿ��һˮ�ۣ�ƿ�м���ƾ���ˮ���м�����ˮ���ټ����������������ʣ����Ҳ��������Ȫ��ˮ���м�������ʿ�����������������
A��Ũ���ᡡ�� B��ʳ�Ρ��� C������ء���D������ͭ
���ַ���������Ȫ��ԭ������������������������������������ ������
�۱Ƚ�����ͼ������ͼ����װ�ã��Ӳ�����Ȫ��ԭ��������������ͼ���ϲ���ƿ������ѹǿ_______������ͼ���²���ƿ������ѹǿ________������������С����
(3)�����г�����������Ȫ����ɽ������ԭ���������� ��������ͼ������ͼ��װ�õ�ԭ�����ơ�
25����10�֣�þ��һ�ֻ��õĽ���������������������������ڵ��ӹ�ҵ������þ��ȡ��ķ�ӦΪ��![]() ��ͬʱ�и���Ӧ������
��ͬʱ�и���Ӧ������![]() ��Mg2Si������Ѹ�ٷ�Ӧ����SiH4(����)��SiH4��������һ�ֲ��ȶ����ֽ�����塣��ͼ��ʾ�ǽ���Mg��SiO2��Ӧ��ʵ��װ�á�
��Mg2Si������Ѹ�ٷ�Ӧ����SiH4(����)��SiH4��������һ�ֲ��ȶ����ֽ�����塣��ͼ��ʾ�ǽ���Mg��SiO2��Ӧ��ʵ��װ�á�
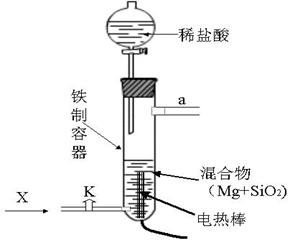
�Իش��������⣺
��1������O2�Ĵ��ڶԸ�ʵ���нϴ�Ӱ�죬ʵ����Ӧͨ��X������Ϊ��������X����Ӧѡ�â�CO2����N2����H2�е�___________��
��2��ʵ�鿪ʼʱ��������ͨ��X�����壬�ٽ�ͨ��Դ���ȷ�Ӧ���������____________������Ӧ�������жϵ�Դ����Ӧ�ܼ������У���ԭ����____________________��
��3����Ӧ����ʱ������ȴ������ʱ�ر�K���ӷ�Һ©��������ϡ���ᣬ�ɹ۲쵽���ܿ�a���������Ļ��ǡ��ݴ��������֪_______�ڿ�������ȼ����Ӧ�Ļ�ѧ����ʽΪ____________��
�ġ������⣨�������1С�⣬��6�֣�
26��0.2mol�л����0.4mol O2���ܱ�������ȼ�պ�IJ���ΪCO2��CO��H2O��g�������ᆳ��Ũ�����Ũ�������������10.8g����ͨ�����ȵ�CuO��ַ�Ӧ������������3.2g�����������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6g��
��1���жϸ��л���Ļ�ѧʽ��
��2����0.2mol���л���ǡ����4.6g��������ȫ��Ӧ����ȷ�����л���Ľṹ��ʽ
�߶��꼶��ѧ����ĩ�������ƻ�ѧ�Ծ����
�༶���������� ѧ�ţ��������� ������ �����������÷֣�
һ������ѡ���⣨ÿ��ֻ��һ����ȷ�𰸣�ÿ��2�֣���40�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� |
�����⣨�������3С�⣬��30�֣�
21����6�֣���1������������������ �������������������� ��
��2���������Ӧ����X�Ļ�ѧ����ʽ�������������������������������� ��
��3�����붡��Ӧ����W�Ļ�ѧ����ʽ�������������������������� ��
22����8�֣���1����������ȩ����_�������� ��2��������ȥ��ϩ����_����������
��3����������ͪ������������4��E����ᷢ��������Ӧ�IJ��������������������������� ����
23����16�֣���1������������������������������������������������ ��
��2������������������������������������������ ��3����������������
����ʵ���⣨�������2С�⣬��24�֣�
24����14�֣�(1) ����(2)������������ ������������������������������������������������ ������������ ���������� ��(3)���������������� ��
25����10�֣���1��_������������2��_������������ ��__������������ ��
��3��_���������� ��__���������������������� ��
�ġ������⣨�������1С�⣬��6�֣�
26���⣺
�߶��꼶��ѧ����ĩ�������ƻ�ѧ�Ծ���
һ������ѡ���⣨ÿ��ֻ��һ����ȷ�𰸣�ÿ��2�֣���40�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� | B | A | D | C | C | C | D | D | C | B | A | B | A | D | D | D | C | A | A | C |
�����⣨�������3С�⣬��30�֣�
21����6�֣���1������ ���������� ������
��2���������Ӧ����X�Ļ�ѧ����ʽ�� N2+3H2=2NH3��
��3�����붡��Ӧ����W�Ļ�ѧ����ʽ�� 2Na+O2=Na2O2��
22����8�֣���1����������ȩ����_A��B��D��E��2��������ȥ��ϩ����_C��D_
��3����������ͪ����_C��4��E����ᷢ��������Ӧ�IJ�����__HCOOCH2C6H5
23����16�֣���1��CH3CH2CH2COCH3��CH3CH2COCH2CH3��CH3COCH��CH3��2��
CH3CH2CO��CH3��2����2��CH3CH2CH2CH2CHO��CH3CH2CH��CH3��CHO����CH3��2CHCH2CHO��3����CH3��3CH2OH
����ʵ���⣨�������2С�⣬��24�֣�
24����14�֣�(1)B(2)�� D��A��Ũ��������ˮ���� ���¶����ߣ��ƾ��ӿ���������ƿ����ѹ��������������������(3)����ͼ��
25����10�֣���1��_H2_����2��_��������__���ȷ�Ӧ��
��3��_������__SiH4+2O2=SiO2+2H2O��
�ġ������⣨�������1С�⣬��6�֣�
26���⣺���л���Ļ�ѧʽΪCXHYOZ�����������У�
�������� CXHYOZ+2O2��CO2+CO+6H2O
����C2H6O2
����������CH2OH-CH2OH