高二化学第一学期期末试卷3
命题:王 勇
本试卷共150分。考试时间120分钟。
第I卷(选择题,共78分)
可能用到的原子量:H 1 C 12 N 14 O 16 Na 23 K 39 Mg 24 S 32 Ba 137
Ag 108 Cu 64 Fe 56 Cl 35.5 Al 27
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意。)
1、下列说法中不正确的是
A、冶金工业上常用铝热反应的原理,利用铝来冶炼钒、铬、锰。
B、氟氯烃大多是无色、无臭的气体,化学性质稳定。
C、金属的治炼一般需要经过三个步骤 :富集、冶炼、精炼
D、标准状况下,1L已烷所含碳原子数为6NA/22.4个
2、在允许加热的条件下,只用一种试剂就可以鉴别氯化钾、硫酸铵、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是
A、BaCl2 B、 NH3・H2O C、 AgNO3 D、 NaOH
3、相同温度下等物质的量浓度的下列溶液中,pH值最小的是
A、NH4Cl B、 NH4HCO3 C、 NH4HSO4 D、 (NH4)2SO4
4、下列除去杂质的方法不正确的是
A、除去CH4中的少量C2H4:通过饱和溴水,收集气体
B、除去CO2中的少量HCl:通入Na2CO3溶液,收集气体
C、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤
D、除去KCl溶液中的少量MgCl2:加入适量KOH溶液,过滤
5、在10mL0.1mol・L-NaOH溶液中加入同体积、同浓度的CH3COOH溶液,反应后溶液中各微粒的浓度关系错误的是(Ac-=CH3COO-)
A、C(Na+)+C(H+)=C(Ac-)+C(OH-)
B、C(Na+)=C(Ac-)+C(HAc)
C、C(Na+)>C(Ac-)>C(OH-)>C(H+)
D、C(Na+)>C(Ac-)>C(H+)>C(OH-)
6、科学家正致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质.如把CO2与H2混合,在一定的条件下以1:3的比例发生反应.生成某种重要的化工原料和水.该化工原料可能是:
A、烷烃 B、烯烃 C、 炔烃 D、芳香烃
7、一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,该混合气体质量为20.8g,当通过无水CaCl2时,CaCl2增重10.8g,原混合气体中CO2的质量为
A、10.5g B、7.5g C、4.4g D、8.8g
8、下列有关纯铁的描述正确的是
A、在潮湿空气中比生铁容易被腐蚀
B、与相同浓度的盐酸反应生成氢气的速率比生铁的快
C、在冷的浓硫酸中可钝化 D、熔点比生铁的低
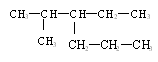
9、对于烃的命名,正确的是
A、2―甲基―3―丙基戊烷 B、3―乙基―2―甲基己烷
| |
10、在一定温度下的定容密闭容器中,当下列物理量不再变化时,不能表明反应:
![]() A(g)+2B(g)C(g)+D(g)已达平衡的是
A(g)+2B(g)C(g)+D(g)已达平衡的是
A、混合气体的压强 B、混合气体的密度
C、B的物质的量浓度 D、气体的总的物质的量
二、选择题(本题包括12小题,每小题4分,共48分。每小题只有一个或两个选项符合题意。若正确答案包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分。)11、有8种物质:①甲烷、②苯、③聚乙烯、④裂化汽油、⑤2-丁炔、⑥溴乙烷、⑦邻二甲苯、⑧环已烯,其中既能使酸性高锰酸钾溶液褪色,又能与溴水反应使之褪色的是
A、③④⑤⑧ B、④⑤⑦⑧ C、④⑤⑧ D、③④⑤⑦⑧
12、一定条件下,将2摩尔的二氧化硫和2摩尔的三氧化硫气体混合于一固定容器的密闭容器中,发生反应:2SO2(气) + O2(气)![]() 2SO3(气),平衡时SO3为n摩尔。在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
2SO3(气),平衡时SO3为n摩尔。在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
A、2摩尔SO2+1摩尔O2 B、4摩尔SO2+1摩尔O2
C、2摩尔SO2+1摩尔O2+2摩尔SO3 D、3摩尔SO2+1摩尔O2+1摩尔SO3
13、经测定某溶液中只有NH4+、Cl-、H+、OH-四种离子,下列说法错误的是:
A、溶液中四种粒子之间不可能满足:C(Cl-)>C(H+)>C(NH4+)>C(OH-)
B、若溶液中粒子间满足:C(NH4+)>C(Cl-)>C(OH-)>C(H+)则溶液中溶质一定
为:NH4Cl、和NH3・H2O
C、若溶液中粒子间满足:C(Cl-)>C(NH4+)>C(H+)>C(OH-)则溶液中溶质一
定只有NH4Cl
D、若溶液中C(NH4+)==C(Cl-),则溶液一定呈中性
14、能正确表示下列化学反应的离子方程式是
A、用碳酸钠溶液吸收足量二氧化硫: CO32-+SO2=CO2+SO32-
B、硫氢化钠溶于水中:HS-+H2O![]() S2-+H3O+
S2-+H3O+
C、金属铝溶于稀硝酸中:Al+2H+=Al3++H2↑
D、碳酸镁溶于盐酸中:CO32-+2H+=H2O+CO2↑
15、有amL三种气态烃的混合物与足量的氧气混合点燃爆炸后,恢复到原来状况(常温常压),体积共缩小2amL,则这三种烃不可能是
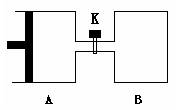 A、CH4
C2H4 C3H4 B、C2H6
C3H6 C4H6
A、CH4
C2H4 C3H4 B、C2H6
C3H6 C4H6
C、C2H2 C2H6 C3H8 D、CH4 C2H6 C2H2
16、如图,向A 中充入1molX和1molY,向B中充入2molX 和2molY,起始时VA=VB=aL,在相同温度和催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g)
![]() 2Z(g)+W(g),此反应是吸热反应.当达到平衡时,VA==1.2aL.下列说法中错误的是:
2Z(g)+W(g),此反应是吸热反应.当达到平衡时,VA==1.2aL.下列说法中错误的是:
A、反应开始时, 容器中化学反应速率快
B、A容器中X的转化率为40%,且比B容器中X的转化率小
C、打开K一段时间达到新平衡时,A的体积为1.6aL(忽略连通管的气体体积)
D、打开K达到新平衡后,升高B容器的温度,A容器体积会增大。
17、我国首创的铝―空气―海水电池被称为“海洋电池”,是一种无污染的长效电池,以铁铂合金网(接触空气)和铝分别为电池的两极放入海水中即可供电,下列反应与该电池的工作原理有关的是
① Fe-2e-===Fe2+ ②Al-3e- ===A13+ ③O2+2H2O+4e- ===4OH-
④4Al+3O2+6H2O===4Al(OH)3 ⑤2Fe+O2+2H2O===2Fe(OH)2
A. ①③⑤ B. ②③④ C.①⑤ D.③④
18、若溶液中由水电离产生的c(OH-)=1×10-14mol・L-1,满足此条件的溶液中一定不能大量共存的离子组是
A、 Al3+ Na+ NO3- Cl- B、 K+ Na+ Cl- CO32-
C、 K+ Na+ Cl- AlO2- D、 K+ Fe2+ SO42- NO3-
19、某有机物中碳和氢原子个数比为3:4,不能与溴水反应却能使酸性KMnO4溶液褪色。其蒸汽密度是相同状况下甲烷密度的7.5倍。在铁存在时与溴反应,能生成两种一溴代物。该有机物可能是
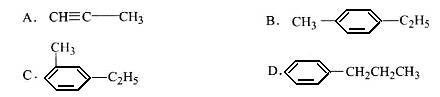 |
20、六苯乙烷为白色固体,其结构表示如图:下列有关说法中不正确的是:
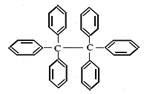 A、它是一种芳香烃,易溶于乙醚中
A、它是一种芳香烃,易溶于乙醚中
B、它的分子式为C38H30,是非极性分子
C、它的一氯代物只有一种
D、在同一平面上的原子最多有14个
21、将0.2mol・L-1HCN溶液和0.1mol・L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是
A、C(HCN)<C(CN-) B、C (Na+)>C(CN-)
C、C(HCN)-C(CN-)=C(OH-)
D、C(HCN)+C(CN-)=0.2mol・L-1
22、在硫酸亚铁、硫酸铁、硫酸铜 的混合溶液600mL,其中C(SO42-)=0.1mol/L
投入一些锌粉,反应后得到一些沉淀,经测定其中含Cu、Fe,但不含Zn,溶液中含Fe2+
0.01mol。据此可知投入锌粉的质量是:
A、13克 B、9.75克 C、6.5克 D、3.25克
第Ⅱ卷(非选择题 共72分)
三、(本题包括三小题,共24分)
23、(本题共4分)下列各组物质可用分液漏斗分离的是_______________________________
①硝基苯和水 ②溴乙烷和水 ③酒精和水 ④苯和水 ⑤正已烷和水 ⑥硫酸钡和水
24、(本题共4分)某研究性学习小组欲检验卤代烃分子中的卤素,设计如下操作:
 ①加热煮沸 ②加入硝酸银溶液③取少量卤代烃 ④加稀硝酸酸化 ⑤加入氢氧化钠溶液 ⑥冷却.你认为正确操作顺序_____________________________
①加热煮沸 ②加入硝酸银溶液③取少量卤代烃 ④加稀硝酸酸化 ⑤加入氢氧化钠溶液 ⑥冷却.你认为正确操作顺序_____________________________
25、(本题共16分)实验室制取乙烯,常因温度过高而使反应产生少量的二氧化硫.某同学设计了如图的实验装置,以确证反应制得的混合气体中含有乙烯和二氧化硫.可供选择的药品: ①酸性高锰酸钾溶液 ②稀硝酸 ③浓硫酸 ④品红溶液 ⑤石蕊试液 ⑥NaOH溶液
1、各装置中所盛放的试剂分别是(填序号):A________ B_______ C______ D________
2、装置B的作用______________;装置C的作用__________________________
3、能说明混合气体中含二氧化硫的实验现象是________________________
确证混合气体中有乙烯的实验现象是______________________
四、(本题包括四小题,共32分)
26、(本题共8分)已知某碳氢化合物A的分子中:①有6个碳原子②每个碳原子都以3个键长相等的共价键分别跟其他3个碳原子相连,形成2个90°的碳―碳―碳键角和1个60°的碳―碳―碳键角。根据以上事实判断:
(1)A的化学式为________________________。
(2)分子中(填“有”或“无”)_______________碳碳双键。
(3)A的结构可表示为__________(只要求画出碳架的空间结构,不要求写出C、H的符号)
27、(本题共14分) AxByCz是由A、B、C三种处于不同短周期的日常生活中常见元素组成的化合物,原子序数由大到小。
已知(1)x、y、z均为正整数,且有x+y+z=13。(2)取0.025mol此化合物与过量水反应,产生1.2g气态物质N,同时生成0.025mol白色胶状沉淀R,R既溶于氢氧化钠溶液,又溶于盐酸,但不溶于氨水。(3)同温同压下40mL由B、C两元素组成的气态物质N,完全燃烧时需O2为80mL,燃烧产物只有CO2和H2O。试确定A______B____ C_______(填元素符号)。
(2)N物质的结构式_______________
(3)化合物AxByCz的化学式________________
写出该物质与水反应的化学方程式____________________________________
28、(本题共10分)某链烃A的相对分子质量为156,在CCl4溶液中跟Br2不起反应。但在光照下可以跟Br2发生取代反应,。取代产物的相对分子质量为235的只有两种:产量较多的一种为B,产量较少的为C。
(1)写出A、B、C的结构简式A、__________ B、___________C、_________。
(2)B或C与NaOH的水溶液反应生成醇,其化学方程式为__________________(只写一个)
五、(本题包括两小题,共16分)
29、(本题共6分)有一金属钠投入到盛有100mL氯化镁和氯化铝的混合溶液的烧杯中,发现烧杯中沉淀先多后少,反应完毕后收集到标准状况下的氢气13.44L,同时得到21.4g沉淀。将此沉淀溶于过量苛性钠溶液中,发现沉淀减轻了15.6g。求原混合溶液中Mg2+、Al3+及Cl-的物质的量浓度。
30、(本题共10分)2mol丁烷气体与一定量氧气共贮于一固定体积的容器中,压强为7KPa,点火燃烧后,回到原室温容器只存在一定量的水(其体积可忽略不计)和两种气体,总压强为4KPa. 求
(1)生成水的质量
(2)反应前氧气的物质的量
(3)反应后CO、CO2的各自物质的量