高二化学(理)上学期期中考试
试卷
本卷可能用到的相对原子质量:N―14 O―16 H―1 Na―23 Se―79
Cu―64 Mg―24 I―27 K―39
一、选择题(每小题只有一个正确选项,共45分)
1、1999年曾报导合成和分离子含有高能量的正离子![]() 的化合物
的化合物![]() ,下列叙述错误的是B
,下列叙述错误的是B
A、![]() 共有34个电子
共有34个电子
B、化合物![]() 中,
中,![]() 的化合价为+1
的化合价为+1
C、![]() 中,N与N原子间以共用电子对结合
中,N与N原子间以共用电子对结合
D、化合物![]() 中,F为-1价
中,F为-1价
2、“摇摇冰”是一种即用即冷的饮料,吸食时将饮料罐隔离层中的化学物质和水混合后摇动即会制冷。该化学物质是B
A、氯化钠 B、固体硝酸铵
C、固体氢氧化钠 D、生石灰
3、下列各组溶液,同时开始反应,出现浑浊最早的是C
A、10℃,![]()
![]()
![]() 与
与![]()
![]()
![]() 溶液混合
溶液混合
B、10℃,![]()
![]()
![]() 与
与![]()
![]()
![]() 溶液混合
溶液混合
C、20℃,![]()
![]()
![]() 与
与![]()
![]()
![]() 溶液混合
溶液混合
D、20℃,![]()
![]()
![]() 与
与![]()
![]()
![]() 溶液混合
溶液混合
4、已知![]() 是此
是此![]() 还弱的酸,反应
还弱的酸,反应![]() 达平衡后,要使
达平衡后,要使![]() 浓度增加可加入C
浓度增加可加入C
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
5、酸雨是过度燃烧煤和石油,生成硫、氮的氧化物,溶于水生成硫酸和硝酸的缘故,某次雨水分析数据如下:![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() ,则此次酸雨的pH值接近于(
,则此次酸雨的pH值接近于(![]() )D
)D
A、6.5 B、5 C、4.5 D、4
6、下列贮存药品的方法正确的是A
A、少量的白磷贮存在水中,切割时必须在水下进行
B、将苛性钠固体存放在有橡皮塞的细口瓶中
C、将浓硝酸保存在橡胶塞的无色试剂瓶中
D、将苛性钠溶液保存在带玻璃塞的玻璃瓶中
7、从某些性质来看:![]() ,
,![]() ,
,![]() ,
,![]() 两两相当,据此判断下列反应D
两两相当,据此判断下列反应D
①![]() ②
②![]()
③![]() ④
④![]()
其中正确的是
A、①② B、①②③ C、①③④ D、①②③④
8、在![]() 反应中,经10min达平衡,此时各物质的浓度变化为A减少
反应中,经10min达平衡,此时各物质的浓度变化为A减少![]() ,B减少
,B减少![]() ,C增加
,C增加![]() ,这时给体系加压,平衡不移动,则
,这时给体系加压,平衡不移动,则![]() 为B
为B
A、2:1:2:1 B、3:1:2:2 C、3:1:2:1 D、3:3:2:4
9、某温度下重水(![]() )的离子积常数为
)的离子积常数为![]() ,用定义pH一样来规定
,用定义pH一样来规定![]() ,则该温度下,下列叙述正确的是C
,则该温度下,下列叙述正确的是C
A、纯净的重水中,![]()
B、1L溶解有![]() 的重水溶液,其
的重水溶液,其![]()
C、纯净的重水中,![]()
D、1L溶解有![]() 的重水溶液,其
的重水溶液,其![]()
10、用蒸馏水稀释![]() 的醋酸溶液至
的醋酸溶液至![]() ,随溶液的稀释(T不变),下列各项中始终保持增大趋势的是C
,随溶液的稀释(T不变),下列各项中始终保持增大趋势的是C
A、![]() B、
B、![]()
C、![]() D、
D、![]()
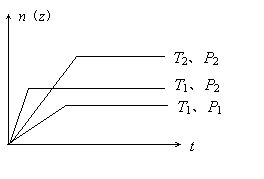 11、反应
11、反应![]() (正反应放热)在不同温度(T1、T2)及不同压强(P1和P2下)产物
(正反应放热)在不同温度(T1、T2)及不同压强(P1和P2下)产物![]() 的物质的量
的物质的量![]() 与反应时间
与反应时间![]() 关系如图所示,下述判断正确的是C
关系如图所示,下述判断正确的是C
A、![]() ,
,![]()
B、![]() ,
,![]()
C、![]() ,
,![]()
D、![]() ,
,![]()
12、某温度下,在固定容积的容器中,可逆反应:![]() 达到平衡,测得平衡时物质的量之比为2:2:1,保持温度不变,以2:2:1的体积比再充入A、B、C,则C
达到平衡,测得平衡时物质的量之比为2:2:1,保持温度不变,以2:2:1的体积比再充入A、B、C,则C
A、平衡向逆反应方向移动 B、平衡不移动
C、C的体积分数增大 D、C的体积分数有可能减小
13、铜和镁的合金4.6g完全溶于浓![]() ,若反应中硝酸被还原只产生
,若反应中硝酸被还原只产生![]() 的
的![]() 气体和
气体和![]() 的
的![]() 气体(标准状况)在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为B
气体(标准状况)在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为B
A、![]() B、
B、![]() C、
C、![]() D、无法计算
D、无法计算
14、在一密闭容器中,对于可逆反应:![]() 不能说明反应已达平衡的是B
不能说明反应已达平衡的是B
A、容器内压强不随时间而变化
B、![]() 四物质的浓度之比为1:1:2:1
四物质的浓度之比为1:1:2:1
C、![]() 浓度不再变化
浓度不再变化
D、单位时间内,每消耗![]() ,同时消耗
,同时消耗![]()
15、砷在元素周期表中位于第VA族,且![]() 与
与![]() 性质相似,均具有还原性,
性质相似,均具有还原性,![]() 性质相似,均具有氧化性,当
性质相似,均具有氧化性,当![]() 与
与![]() 相互反应时,所得产物是D
相互反应时,所得产物是D
①![]() ②
②![]() ③
③![]() ④
④![]()
A、①② B、②③ C、③④ D、①③
二、填空题(共32分)
16、(6分)在新疆和青海两省交界处有一狭长山谷,每当牧民和牲畜进入后,风和日丽的晴天顷刻电闪雷鸣,狂风大作,人畜常遭雷击而倒毙。奇怪的是这里牧草茂盛,四季常青,被当地牧民称为“魔鬼谷”,试用化学方程式表示“魔鬼谷”牧草茂盛的原因。
① ②
③
17、(10分)A、B、C、D为四种气体单质,在一定条件下,B可以分别与A、C、D化合生成甲、乙、丙,C和D化合生成丁,已知甲、乙、丙每个分子中含有的电子数相同,并且甲、乙、丙、丁有下图所示关系:
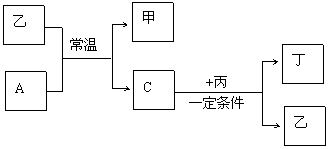 |
则
(1)单质B的分子式为 ,单质D的结构式为 。
(2)单质A与化合物乙反应的化学方程式为 。
(3)单质C与化合物丙反应的化学方程式 。
(4)试根据化合物丙、丁中D元素的价态,判断丙和丁能否在一定条件下反应,若能,写出化学方程式,若不能,写出原因。
18、(8分)在25℃,有![]() 的盐酸和
的盐酸和![]() 的
的![]() 溶液,取
溶液,取![]() 盐酸溶液与
盐酸溶液与![]() 溶液中和,需
溶液中和,需![]()
![]() 溶液,问:
溶液,问:
(1)若![]() ,则
,则![]() (填数字)
(填数字)
(2)若![]() ,则
,则![]() (填数字)
(填数字)
(3)若![]() ,则
,则![]() (填表达式)且
(填表达式)且![]()
![]() (填>、<或=)
(填>、<或=)
19、(8分)有A、B两容器,A容器容积固定,B容器容积可变。一定温度下,在A中加入2![]() 、
、![]() ,反应:
,反应:![]() 达平衡时生成
达平衡时生成![]() 的物质的量为
的物质的量为![]() 。
。
(1)在相同温度下,在B中加入![]() 、
、![]() ,当B的压强与A的压强相等,B中反应达平衡时,生成
,当B的压强与A的压强相等,B中反应达平衡时,生成![]() 的物质的量为
的物质的量为
![]() (填大于、等于或小于多少
(填大于、等于或小于多少![]() ,下同)
,下同)
当B的容积与A的容积相等,B中反应达平衡时,生成的![]() 的物质的量为
的物质的量为 ![]() 。
。
(2)相同温度下,保持B的容积为A的一半,并加入![]() ,要使B中反应平衡时,各物质的质量分数与上述A容器中达平衡时相同,则起始应加入
,要使B中反应平衡时,各物质的质量分数与上述A容器中达平衡时相同,则起始应加入 ![]() 与
与
![]() 。
。
三、实验题(15分)
20、实验室里用空气和如下图所示药品、仪器装置制取少量氮化镁:
(1)当装置按顺序连接好以后,首先应检查气密性,然后进行实验
a:如果所制气体的流向从左向右时,上述各仪器的正确连接顺序是
(填接口符号)
b:实验开始,应先在 处(填写接口符号)接通自来水管,然后依次点燃有 粉 (填元素符号,下同)装置的酒精灯和装有 粉装置的酒精灯。
(2)浓![]() 的作用是
,饱和
的作用是
,饱和![]() 溶液的作用是
,
溶液的作用是
,
装置⑤的作用是 。
(3)装置①中发生的化学方程式为 。
(4)制成![]() 后剩余气体是
。
后剩余气体是
。
四、计算题(8分)
21、已知对于氧化性比![]() 强的物质,可在一定条件下用
强的物质,可在一定条件下用![]() 还原,并产生碘单质,然后用
还原,并产生碘单质,然后用![]() 标准液滴定
标准液滴定![]() 这种方法叫间接碘量法。
这种方法叫间接碘量法。
现将3.320g纯净的某金属碘化物![]() (
(![]() 为整数)溶于稀
为整数)溶于稀![]() ,制成500
,制成500![]() 溶液,从中取出50
溶液,从中取出50![]() 试样,加入0.003
试样,加入0.003![]() ,充分反应后煮沸除去反应中生成的碘,然后加入足量的
,充分反应后煮沸除去反应中生成的碘,然后加入足量的![]() 溶液,与过剩的
溶液,与过剩的![]() 作用,最后用标准
作用,最后用标准![]() 溶液滴定生成的
溶液滴定生成的![]() ,结果消耗溶液中的
,结果消耗溶液中的![]()
![]() ,上述反应中有关离子方程式为:
,上述反应中有关离子方程式为:![]() ;
;![]() 。求(1)
。求(1)![]() 等于多少?(2)M的相对原子质量等于多少?
等于多少?(2)M的相对原子质量等于多少?
 上学期期中考试
上学期期中考试
高二化学(理)答卷
一、(15×3分=45分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | ||||||||
| 题号 | 9 | 10 | 11 | 12 | 13 | 12 | 15 | |
| 答案 |
二、填空题(共32分)
16、(6分)
![]() ①N2+O2 2NO
①N2+O2 2NO
②2NO+O2==2NO2
③3NO2+H2O==2HNO3+NO
17、(10分)
![]() (1)H2、N N
(1)H2、N N
(2)2F2+2H2O==4HF+O2
(3)4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
![]() (4)4NH3+6NO 5N2+6H2O
(4)4NH3+6NO 5N2+6H2O
18、(8分)
(1) 1 。
(2) 0.1 。
(3) 10a+b-14 、 > 。
19、(8分)
(1) 等于2m 、大于2m 。
(2) 0.5 、 0 。
三、实验题(15分)
20、(1)a、 G-H-F-E-C-D-N-M-A 。
b、 G 、 Cu 、 Mg 。
(2) 吸收空气中的水分 、 吸收空气中的CO2
吸收空气中的O2 。
(3) N2+3Mg![]() Mg3N2
。
Mg3N2
。
(4)稀有气体。
四、计算题(8分)
(1)x = 1 。
(2)M的相对原子质量为 39 。
解 IO3-~~3I2~~~~6Na2S2O3
1mol 6mol
n(IO3-)=0.0026mol 0.0156mol
与MIX反应的KIO3为0.003-0.0026=0.0004mol
5I-~~~~~~~~~~~IO3-
50mL溶液中n(I-)=0.002mol 0.0004mol
则原溶液中n(I-)=0.002×=0.02mol
有:×X=0.02 R=39X
X=1 则R=39
X=2、3 无此金属