高二化学第二学期期中考试
化学试卷
命题:黎婉君 审题:卢成
第Ⅰ卷(选择题 共74分)
原子量:H 1 N 14 O 16
一、选择题(本题包括8小题,每小题只有一个正确答案,每小题3分共24分)
1、下列各原子或原子团,不属于官能团的是( )
A、OH― B、―Br C、―SO3H D、>C=C<
2、现代以石油化工为基础的三大合成材料是( )
①合成氨 ②塑料 ③医药 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤
A、②④⑦ B、②④⑥ C、①③⑤ D、④⑤⑥
3、下列各组物质按熔沸点由低到高顺序排列的是( )
A、二氧化硅、烧碱、萘 B、铝、镁、钠
C、干冰、氧化镁、磷酸 D、丙烷、2-甲基丙烷、丁烷
4、下列试剂可用无色、带胶塞的玻璃瓶保存的是( )
A、液溴 B、氢氟酸 C、硝酸银溶液 D、碳酸钠溶液
5、下列各组微粒氧化性比较不正确的是( )
A、H+ > Na+ B、Cu2+ > H+ C、Cu2+ > Fe3+ D、Fe2+ > Zn2+
6、下列变化过程中,共价键被破坏的是( )
A、烧碱溶于水 B、氯化氢气体溶于水
C、二氧化碳变成干冰 D、碘溶于酒精
7、下列物质的水溶液中,pH值大于7的是( )
A、Na2CO3 B、NH4NO3 C、Na2SO4 D、KNO3
8、 增大压强,对已达到平衡的下列反应产生的影响是( )
3X(g)+Y(g)![]() 2Z(g)+2Q(S)
2Z(g)+2Q(S)
A、正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B、正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C、正、逆反应速率都增大,平衡向正反应方向移动
D、正、逆反应速率都没有变化,平衡不发生移动
二、选择题(本题包括10小题,每小题5分共50分。每小题有1―2个选项符合题意。若正确答案只包括一个选项,多选时该题为0分;若正确答案包括2个选项,只选一个且正确的给2分,选两个且都正确的得5分,但只要选错一个,该题就为0分)
9、设阿伏加德罗常数为NA,下列说法正确的是( )
A、 常温常压下,2g氦气所含原子数是0.5NA
B、 常温常压下,11.2L氯气所含分子数是0.5NA
C、 同温同压下,密度相同的两种气体的摩尔质量相同
D、同温同压下,原子数都是NA的两种气体的体积相同
10、下列反应的化学方程式(或离子方程式)错误的是
A、苯酚与氢氧化钠溶液反应 C6H5OH+OH― → C6H5O―+H2O
B、苯甲酸与甲醇、浓硫酸混和共热 C6H5COOH+CH3OH
![]() C6H5OCOCH3+H2O
C6H5OCOCH3+H2O
C、乙醛与银氨溶液反应 CH3CHO+2[Ag(NH3)2]OH → CH3COONH4+2Ag ↓ +3NH3+H2O
|
11、下列叙述正确的是( )
A、 离子化合物中可能含有极性共价键或非极性共价键
B、 在PCl5分子中,磷原子满足最外层8电子结构
C、 正四面体的分子中,键角一定为109°28′
D、石墨晶体为层状结构,同一层上平均每个正六边形所含碳原子数为2
12、某溶液中含有大量的AlO2-,则可以大量共存于该溶液的离子组是( )
A、K+、OH-、SO42- B、Na+、NH4+、NO3-
 C、Mg2+、Br-、CO32- D、Al3+、Na+、Cl-
C、Mg2+、Br-、CO32- D、Al3+、Na+、Cl-
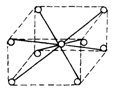
13、右图是某种离子化合物的晶胞,阳离子位于中间,阴离子位于8个顶角,该化合物中,阳离、阴离子的个数比为( )。
A、1∶8 B、1∶4
C、1∶2 D、1∶1
14、已知A、B、C三种短周期元素可以形成化合物AB2、CA2,则A一定为( )
A、金属元素 B、非金属元素 C、IA族元素 D、IVA族元素
15、同温同压下,等体积的两容器内分别充满由14N、13C、18O三种原子构成的一氧化氮和一氧化碳,下列说法正确的是
A、所含分子数和质量均不相同 B、含有相同的分子数和电子数
C、含有相同的质子数和中子数 D、含有相同数目的中子、原子和分子
16、下列各组均有两种有机物,若分别取相同的物质的量,在足量的氧气中完全燃烧,两种有机物耗氧量相同的是
A、乙烯和乙醇 B、乙炔和苯 C、乙烷和乙酸乙脂 D、乙醇和乙醛
17、下列物质中,在一定条件下能发生水解的高分子化合物是( )
A、肥皂 B、油脂 C、纤维素 D、蛋白质
18、钢铁发生腐蚀时,正极上发生的反应是( )
A、2Fe-4e― =2Fe2+ B、2Fe2++4e― =2Fe
C、2H2O+O2+4e―=4OH― D、Fe3++e―=Fe2+
第二学期期中考试
化学试卷
(高二化学班适用)
第Ⅱ卷(非选择题 共76分)
姓名______________班别__________学号____________成绩______________
三、无机题(本题包括2小题共22分)
19、(10分)W、X、Y、Z为短周期内(除稀有气体元素外)的四种元素。它们的原子序数依次增大,其中只有Y是金属元素,X与Z属于同一主族的元素,Y的最外层电子数和W最外层电子数相等,Y、Z两元素的质子数之和为W、X两元素的质子数之和的3倍。
由此可知元素W为_______;X为_______;Y 为_______;Z为_______(填元素符号)
上述元素中任意三种可组成盐,写出这些盐的化学式(写出其中两种)
______________________________________________________
四种元素中两两组合,能生成共价化合物的化学式有(写出其中的四种)
__________________________________________________________________
20、(12分)X、Y、Z是主族元素的单质,U、V是化合物,它们有如下的转化关系:
|
|
![]()
![]()
|
![]() ② 单质Z
② 单质Z
![]() ③ 单质Z
③ 单质Z
|
|
(1) 写出①和②反应所属的基本反应类型①属____________反应,②属___________反应
(2) 请写出符合整个反应体系的①的3个不同的化学方程式(要求:所有X、Y必须由不同主族的元素组成)
①_____________________________________________
②_____________________________________________
③_____________________________________________
(3) 现有化合物W,它跟化合物U或CO2反应都能生成单质Y,
则符合条件的单质X是_____________,单质Y是___________,单质Z是___________,
化合物W是___________。
四、有机题(本题包括2小题共17分)
21、(10分)现有八种有机物,分别是①乙醇 ②甲苯 ③苯酚 ④苯甲酸
⑤葡萄糖 ⑥溴乙烷 ⑦乙烯 ⑧乙酸,其中(填写序号)
(1) 能跟银氨溶液发生银镜反应的是_______________
(2) 能使氯化铁溶液变紫色的是_____________
(3) 在常温下能跟浓溴水反应生成白色沉淀的是______________
(4) 在一定条件下能跟羧酸发生酯化反应的是_____________
(5) 在一定条件下能跟氢氧化钠水溶液发生反应的是______________
22、(14分)某链烃A有下列的转化关系
![]()
|
|
|
|
|
|
|
|
已知,D的式量为60,它的水溶液能使石蕊试液变红,G是高分子化合物。
⑴请用结构简式表示下列物质:
A是 ,B是 ,C是 ,
D是 ,F是 ,G是 。
⑵ F → G的化学反应类型属于 反应。
五、实验题(本题包括2小题共18分)
23、(6分)铜丝网在酒精灯上烧成红热,立即插入盛有少量乙醇的试管底,这样反复几次,在上述操作中,乙醇与热铜丝反应的化学方程式是_________________________________,“插入”操作前后,试管口的气味由__________气味变成___________气味,铜丝网的颜色由_________色变成________色。
24、(12分)请你结合所学知识设计实验直接证实AlO2―结合H+的能力比CO32―强。现有试剂NaHCO3溶液、AlCl3溶液(仪器自选)
(1)请从下列物质中再选择必要的试剂( )
A、盐酸 B、Na2CO3溶液 C、NaOH溶液 D、FeCl3溶液
(2)写出你操作的步骤及现象:
①取少量AlCl3溶液于试管中,__________________________________________________
②____________________________________________________________________________
____________________________________________________________________________
(3)写出(2)中有关的反应的离子方程式:
____________________________________________________________________________
____________________________________________________________________________
六、计算题(本题包括2小题共12分)
25、(4分)把标准状况下的224LNH3溶于1L水中,若所得氨水的密度近似为1g/cm3,求此氨水的物质的量浓度和溶质的质量分数。
26、(8分)由碳、氢、氧三种元素组成的某有机物,分子中共有10个原子,其核外共有32个电子,1mol该有机物在氧气中完全燃烧时需要4molO2,回答:
⑴若该有机物可使溴水褪色,但不发生银镜反应,取0.2mol该有机物与足量钠反应,能产2.24LH2(标况),则该有机物的结构式可能是什么?
⑵若该有机物能发生银镜反应,则其结构简式是什么?写出它分别与氢气、新制的氢氧化铜发生反应的化学方程式。
第二学期期中考试
化学试卷
(高二化学班适用)
参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| 答案 | A | B | D | D | C | B | A | C | ||
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | AC | B | AD | A | D | B | D | A | CD | C |
19、 H O Na S Na2SO3 Na2SO4 NaHS SO2 SO3 H2O H2O2 H2S
20、(1)置换、化合
(2)2F2+2H2O=4HF+O2 2Al+6HCl=2AlCl3+3H2 2Mg+CO2=2MgO+C
Cl2+H2S=2HCl+S
(或其它符合条件的答案均可)
(3)F2、O2、H2、Na2O2
21、⑤、③、③、①③⑤、③④⑥⑧
22、(1)A是CH2=CH2 B是CH3CH2OH C是 CH3CHO D是CH3COOH
F是CH2=CHCl G是
(2)加聚
23、2CH2=CH2+O2![]() 2CH3CHO+2H2O 醇香
刺激性 黑色 红色
2CH3CHO+2H2O 醇香
刺激性 黑色 红色
24、(1)C
(2)①取少量AlCl3溶液于试管中,向试管内逐渐滴入NaOH溶液直至产生的沉淀又恰好全部消失,
②再向①所得的澄清溶液加入NaHCO3溶液至足量,有白色胶状沉淀。
(3)Al3++3OH―=Al(OH)3 ¯ Al(OH)3+OH―=AlO2―+2H2O
AlO2―+HCO3―+H2O=Al(OH)3 ¯ +CO32―
25、n=10mol,m(氨水)=170g m(水)=1000g V(溶液)=1.17L
P%=170/1170*100%=14.5%
C=10mol/1.17L=8.5mol/L
26、分子式为C3H6O
(1) 该有机物为CH2=CHCH2OH
(2) 有机物为CH3CH2CHO。
CH3CH2CHO + H2 → CH3CH2CH2OH
CH3CH2CHO + 2Cu(OH)2 → CH3CH2COOH + Cu2O ↓+2 H2O