高二化学第四章 烃 测验题(必修)
班级 姓名 成绩
可能用到的元素的相对原子质量:
H—1 C—12 O—16
一、选择题(每小题3分,共60分。每小题只有一个选项符合题意。)
1. 下列有机物的命名正确的是 ( )
A. 1,2─二甲基戊烷 B. 2─乙基戊烷
C. 3,4─二甲基戊烷 D. 3─甲基己烷
2. 下列互为同系物的是 ( )
A. C2H4与C3H6Cl2 B.CH≡C─CH3与CH3─C≡C─CH3
C. C2H2与C6H6 D. 石墨与金刚石
3. 下列反应的生成物为纯净物的是 ( )
A. CH4和Cl2光照 B. 乙炔与溴1:1加成
C. 乙醇和浓H2SO4共热 D. 乙烯和氯化氢加成
4 . 下列实验室制取气体的方案中,正确的是 ( )
A. 用食盐水和浓硫酸制取氯化氢
B. 将氯化铵晶体加热分解制取氨气
C. 将酒精和浓硫酸按1∶3混合,加热至170℃制取乙烯
D. 用二氧化锰和稀盐酸制取氯气
5. 下列反应属于置换反应的是 ( )
A. Cu+2FeCl3=CuCl2+2FeCl2 B. SO2+2H2S=2H2O+3S
C. Cl2+C2H6![]() C2H5Cl+HCl D. 2KClO3+I2
C2H5Cl+HCl D. 2KClO3+I2![]() Cl2+2KIO3
Cl2+2KIO3
6. 下列各组混合气体中,比乙烯含碳量高的是 ( )
A. 甲烷和丙烯 B. 乙烷和丁烯
C. 丙烷与丙烯 D. 丙烯与丙炔
7. 某气态烃10 mL与50 mL氧气在一定条件下作用,刚好耗尽反应物,
生成水蒸气40 mL、一氧化碳和二氧化碳各20 mL(各体积都是在同温
同压下测得)。该气态烃为 ( )
A. C3H8 B. C4H6 C. C3H6 D. C4H8
8. 下列说法正确的是 ( )
A. 分子组成相差一个或几个CH2原子团的有机物是同系物
B. 各组成元素质量分数相同的烃是同一种烃
C. 分子式相同而结构式不同的有机物一定互为同分异构体
D. 相对原子质量相同的原子一定互为同位素
9. 把体积相同的甲烷和氯气充入一个集气瓶中,光照一段时间后,发
现气体的黄绿色变浅,集气瓶壁上有淡黄绿色液滴,此时,集气瓶内
的物质可能有 ( )
A.四种 B.五种 C.六种 D.七种
10. 某气态有机物在相同温度和相同压强下对氧气的相对密度为
1.375,则这种气态有机物的式量为 ( )
A 44 B 42 C 38 D 36
11. 同分异构体具有 ( )
A 相同的式量和不同的组成 B 相同的分子组成和不同的式量
C 相同的分子结构和不同的式量
D 相同的分子组成和不同的分子结构
12. 已知丙烷的二氯代物有四种同分异构体,则其六氯代物的同分异构
体数目有 ( )
A 2种 B 3种 C 4种 D 5种
13. 两种气态烃组成的混合气体0.1mol,完全燃烧后生成0.16molCO2
和3.6 g水,则混合气体是 ( )
A 一定是甲烷 B 一定是甲烷和C2H4
C 一定没有乙烷 D 一定有C2H2
14. 有一类组成最简单的有机硅化合物叫硅烷,它的分子组成与烷烃相
似.下列说法中错误的是 ( )
A 硅烷的分子通式可表示为SinH2n+2
B 甲硅烷燃烧生成二氧化硅和水
C 甲硅烷的分子式为SiH4 D 甲硅烷的热稳定性强于甲烷
15. 关于实验室制备乙烯的实验,下列说法正确的是: ( )
A.反应物是乙醇和过量的3mol/L硫酸的混合物
B.温度计插入反应液面下,控制温度为140℃
C.反应容器中(烧瓶)应加入少许碎瓷片
D.反应完毕先熄灭酒精灯,再从水中取出导管
16. 不可能是乙烯加成产物的是: ( )
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
17. 既可用来鉴别CH4和C2H4,又可除去中混有C2H4的方法是:( )
A.通入KMnO4溶液中 B.通入足量溴水中
C.点燃 D.通入H2后加热
18. 1mol C2H4与Cl2完全加成,再与Cl2彻底取代,两个过程共用Cl2:
A.2mol B.4mol C.5mol D.6mol
19. 下列不是乙烯用途的是:
( )
A.作灭火剂
B.制塑料
C.制有机溶剂 D.做果实催熟剂
20. 等质量的乙烯和聚乙烯完全燃烧,消耗氧气的物质的量的关系是:
A.前者多 B.后者多 C.相等 D.不能肯定
二、选择题(每题3分,可能有二个正确选项,共30分)
21. 无水乙醇与浓硫酸混合加热制取乙烯气体,该反应中浓硫酸的作用
是:( )
A.干燥剂 B.催化剂 C.脱水剂 D.反应物
22. 下列物质既能使溴水褪色,又能使酸性高锰酸钾溶液褪色的是:
A.H2S B.C2H4 C.CCl4 D.C3H8
23. 把Mmol H2和N mol C2H4混合,在一定条件下使它们一部分发生反
应生成W mol C2H6将反应后的混合气体完全燃烧,消耗氧气的物质
的量为 ( )
A、M+3N B、![]() +3N C、
+3N C、![]() +3N+
+3N+![]() W D、
W D、![]() +3N—
+3N—![]() W
W
24. 制取下列气体时,不宜采用排空气法收集的是 ( )
A 氨气 B 乙烯 C 二氧化碳 D 一氧化氮
25. 下列各种烯烃中沸点最高的是( )
A CH2=CH-CH3 B CH3-CH2-CH=CH2
![]() C
CH2=CH-CH-CH3
D CH3-CH2-CH2-CH=CH2
C
CH2=CH-CH-CH3
D CH3-CH2-CH2-CH=CH2
CH3
26. 关于炔烃的下列叙述正确的是 ( )
A 分子里含有碳碳三键的不饱和链烃叫炔烃
B 炔烃分子里的所有碳原子都在同一条直线上
C 炔烃易发生加成反应,也易发生取代反应
D 炔烃可以使溴水褪色,也可以使酸性高锰酸钾溶液褪色
27. 用乙炔原料制取CH2Br—CHBrCl,可行的反应途径是 ( )
A 先加Cl2,再加Br2 B 先加Cl2,再加HBr
C 先加HCl,再加HBr D 先加HCl,再加Br2
28. 在同温同压下,1体积某气态烃与2体积氯化氢完全加成的产物能
与4体积氯气发生取代反应,所得产物中不再含有氢元素,则原气
态烃是 ( )
A 丙炔 B 乙炔 C 丙烯 D 丁烯
29. 下列有关温度计的使用正确的是 ( )
A、制乙烯时控制的是反应混合物的温度,所以温度计放在溶液中
B、制乙烯时控制的是气体温度,所以温度计放在液面之上
C、石油分馏时温度计放入石油中,控制石油的温度
D、石油分馏是把石油分成不同沸点范围的产品,控制的是气体的温度
30、下列变化中,由加成反应引起的是 ( )
A、乙炔通入高锰酸钾酸性溶液中,高锰酸钾溶液褪色
B、乙烯在一定温度、压强和催化剂的作用下,聚合聚乙烯
C、在一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成
D、在催化剂作用下苯和氢气反应生成环已烷
高二化学第四章 烃测验题(必修)答题卷
班级 姓名 成绩
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | D | B | D | C | D | D | D | C | D | A |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | D | C | C | D | C | B | B | C | A | C |
| 题号 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| 答案 | BC | AB | B | BD | D | AD | D | B | AD | BD |
三、填空题(除31题和35题(1)外其他每空2分,共52分)
31、填写下列空白(8分)
| 化合物类别 | 烷烃 | 烯烃 | 炔烃 | 苯 |
|
结构特点 |
仅含碳碳单键 |
含有C=C |
含有C≡C | 碳与碳之间形成介于单、双键之间的独特的键 |
| 通式 | CnH2n+2 | CnH2n | CnH2n-2 | CnH2n-6(n≥6) |
| 与溴反应类型 | 取代 | 加成 | 加成 | 取代 |
| 加入酸性高锰酸钾溶液现象 | 不褪色 | 褪色 | 褪色 | 不褪色 |
| 性质特点 | 易取代 | 易加成 | 易加成 | 易取代难加成 |
32、乙烯中当四个H原子换成四个F原子时称为四氟乙烯(CF2═CF2)
也与乙烯一样能发生加聚反应生成聚四氟乙烯,聚四氟乙烯在耐热
和化学性质的稳定性都超过了其他塑料,号称“塑料王”。在工业
上有广泛的用途,其合成路线如图所示:
![]() 氯仿
HF 二氟一氯甲烷 △ 四氟乙烯
聚四氟乙烯
氯仿
HF 二氟一氯甲烷 △ 四氟乙烯
聚四氟乙烯
A (SbCl5) B 热分解 C D
⑴在方框内填入合适的有机物的结构简式。CHCl3;CHClF2; CF2═CF2;
![]()
![]() [ CF2—CF2 ]n
[ CF2—CF2 ]n
![]() ⑵写出下列化学方程式:
⑵写出下列化学方程式:
![]() B C 2CHClF2 CF2═CF2+2HCl
B C 2CHClF2 CF2═CF2+2HCl
![]()
![]()
![]()
![]() C D nCF2═CF2 [ CF2—CF2 ]n
C D nCF2═CF2 [ CF2—CF2 ]n
33、现有CH4、C3H4、C2H4、C2H6、C3H6五种有机物,同质量的以上物质中,
在标准状况下体积最大的是 CH4 ;同质量的以上物质完全燃
烧时耗去O2最多的是 CH4 ;同状况、 同体积的以上五种物质完全
燃烧时耗去O2的量最多的是C3H6;同质量的以上五种物质完全燃烧
时,生成二氧化碳最多的是 C3H4 ,生成水最多的是 CH4
34、120℃分子式为CxHy的气态烃与氧气混合燃烧,恰好完全反应,测
得反应前后总体积相同。写出符合题设的代表不同类别的常见的3种
有机物的结构简式 CH4 、 C2H4 、 C3H4 ;
35、在实验室制取乙烯,常有少量二氧化硫生成,现设计如下实验,确
认混合气中有乙烯和二氧化硫。
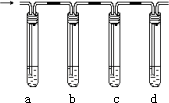 |
1)(每空1分)a、b、c、d装置可盛放的试剂是:
a A ,b B ,c A ,d D ,
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾
2)(2分)能说明二氧化硫气体存在的现象是 A中品红溶液褪色 .
3)(2分)使用b装置的目的是 除去SO2 .
4)(2分)使用c装置的目的是 检验SO2是否除净 .
5)(4分)确定含有乙烯的现象是
(1) C中品红不褪色 ,(2) D中酸性高锰酸钾
6)(2分)写出实验室制乙烯的化学反应方程式
![]() CH3CH2OH CH2═CH2↑+H2O
CH3CH2OH CH2═CH2↑+H2O
四、计算题
36、标准状况下1.68 L气态烃在足量氧气中完全燃烧。若将产物通入
足量澄清石灰水,得到的白色沉淀质量为15.0 g;若用足量碱石灰
吸收燃烧产物,增重9.3 g。(8分)
(l)计算燃烧产物中水的质量。2.7g
(2)通过计算推断它的分子式 C2H4