�л������ʽ�ͽṹʽ��ȷ��
�������Ļ���
һ��ѡ���⪥
1.���³�ѹ�£������������¸����ֱ���������O2���ȼ�գ�����O2������(����)�������ʵ��������и����ֱ�������O2�г��ȼ�գ�����O2������(����)��
A.���顡������ B.��ϩ�������� C.��Ȳ�������� D.���骥
2.1.01��105Pa��120��ʱ��ij��̬�����ܱ������������O2��͵�ȼ����ȫ��Ӧ�����¶ȣ�ѹǿ���䣬����������(����)��
A.CH4�������� B.C2H6����������C.C3H4�������� D.C2H2��
3.���ȼ�յ����ʵ����������л������ͬ��������Ҫ����������(����)��
A.C4H8O2�������� B.C4H10�������� C.C2H6O2�������� D.C2H2��
4.���ȼ�յ����������и����л������ͬ��������O2���������ȫ��ͬ��һ����(����)��
A.��Ȳ�������� ���������� B.�Ҵ�������(CH3-O-CH3)��
C.��Ȳ����������������� D.�����顢������
5.ij�л�������������ȫȼ��ʱ�������������ĵ����������ɵĶ�����̼��ͬ��ͬѹ�µ������Ϊ1��4��3�����л��ﲻ������(����)��
A.C3H4�������� B.C3H8O2�������� C.C3H6O�������� D.C3H6O2��
6.һ������ij�л�����ȫȼ�պ�ȼ�ղ���ͨ��������ʯ��ˮ�������˿ɵó���10g����������Һʱ��������ֻ��ԭʯ��ˮ����2.9g������л��������(����)��
A.��ϩ�������� B.�Ҷ����������� C.�Ҵ��������� D.���Ѫ�
7.���ⶨC3H7OH��C6H12��ɵĻ������������������Ϊ8%����˻�������������������(����)��
A.78%�������� B.22%�������� C.14%�������� D.13%��
8.ij�л��ﺬC52.2%����H13.0%�����л���1g�����������Ʒ�Ӧ�����������0.243LH2������л���ķ���ʽΪ(����)��
A.C2H6O�������� B.C2H4O2�������� C.CH4O�������� D.C4H10O��
��������⪥
9.ij����CԪ��Ϊ83%��������ķ���ʽΪ____________����ij���ķ�����Ϊ128�������ʽ����Ϊ____________��____________����
10.��A��B���ǿ�ȼ�����A��B�����ַ��������ȵ������ͬ�����»�Ϻ������һ������A��B�����ַ�������ȵ��л����ͬ�����»�Ϻ�������һ�����������������A��B��������A��B�Ժ��ֱ�����ϣ���ȫȼ�պ������������������䡣�Էֱ�д����������������������ʽ���л���ṹ��ʽ��һ�飬��˵��A��BӦ�����������
(1)����һ��ķ���ʽ____________��____________��Ӧ�����������_________����
(2)�л���һ��Ľṹ��ʽ____________��____________��Ӧ�����������___________��
11.��д������ѧ�����л���Ľṹ��ʽ����ȼ�պ����CO2��H2O(g)����ȷ������б�ֵ�Ī�(1)V(CO2)/V��H2O��=2��
��____________��____________��
(2)V(CO2)/V(H2O)=1/2��
��____________��____________��
12.ij��������̼�����������Ϊ5��1��������ķ���ʽΪ____________�Ƶ������ǣ�____________��
������������ߡ�
13.��֪����ʽ���ϣ�(CO)n(H2O)m��(n��m��Ϊ������)�ĸ����л��������ȫȼ��ʱ���ĵ�O2�����ɵ�CO2�����������1��2������һЩ��C��H��O����Ԫ�ص��л��������ȫȼ��ʱ������O2������CO2���������3��4�������ǵķ���ʽ�ã�(CxOy)n(H2O)m�ݱ�ʾ��
(1)��(CxOy)n(H2O)m��(m��n��Ϊ������)�У�x=____________��y=____________
(2)��Щ�л�������Է���������С�Ļ�����ķ���ʽ��____________��
(3)ij����̼ԭ������ͬ�������л�����ǵ���Է��������ֱ�Ϊa��b(a��b)����b-a�ض���____________(��һ������)������������
14.�ڳ����µ�һ�ܱ��������ȷ���1.56gNa2O2��Ȼ����ͨ��O2����ͨ��C2H6���õ����ȼ��ֱ����Ӧ��ȫΪֹ���ָ���ԭ�¶ȣ�������ѹǿ����Ϊ�㡣��
(1)��ͬ�����£�ͨ��O2��C2H6������ȵ�ȡֵ��Χ��____________��
(2)ͨ��O2�������ܳ���____________________g
15.0.2mol�л����0.4molO2���ܱ�������ȼ�պ����ΪCO2��CO��H2O(g)�����ᆳ��ŨH2SO4����������10.8g����ͨ�����ȵ�CuO����ַ�Ӧ��CuO��������3.2g�����������ͨ����ʯ�ұ���ȫ���գ���������17.6g��
(1)���ƶϸ��л���ķ���ʽ��
(2)��0.2mol���л���ǡǡ����9.2g��������ȫ��Ӧ����ȷ�����л���Ľṹ��ʽ
16.ij���ֽ����Ϊ̼�⻯���������̼�⻯����������ʵ�飺(1)��ȡһ������̼�⻯������ȫȼ�գ�ʹȼ�պ������ͨ��ʢŨH2SO4��ϴ��ƿ������0.72g����ͨ��ʯ��ˮ��ʯ��ˮ����2.2g��(2)���ⶨ����̼�⻯����(����)���ܶ�����ͬ״���������ܶȵ�34����(3)��̼�⻯����0.1mol�ܺ�32g����ӳɷ�Ӧ��(4)����������(3)���������У���ԭ�ӷֲ��ڲ�ͬ��̼ԭ���ϣ��ҷ�������һ��Cԭ����֧���ϡ����ƶϣ���
(1)��̼�⻯����Ľṹ��ʽΪ____________������Ϊ____________����
(2)���Ľṹ��ʽΪ_____________������Ϊ____________��
���
�������Ļ���
һ��1.AD��2.B 3.B��4.D��5.D 6.BC��7.C��8.A��
����9.C4H10��C9H20��C10H8��
10.(1)CO��H2�����ʵ�����ͬ����O2������ͬ��
(2)C2H5OH��CH3��O��CH3��������ͬ���칹�媥
11.(1)CH��CH��![]() ��(2)CH4��CH3OH
��(2)CH4��CH3OH
12.C5H12��������ķ���ʽΪCxHy������![]() =5/1��x/y=5/12���Է���ʽΪC5H12
=5/1��x/y=5/12���Է���ʽΪC5H12
������������ߡ�
13.(1)x=2��y=1��(2)C2H2O2 (3)18
14.(1)1��V(O2)/V(C2H6)��2.5��
��ֻ��CO2��Na2O2��Ӧʱ����Ӧͨ���O2��࣬��2C2H6+5O2+4Na2O2��4Na2CO3+6H2O(l)��V(O2)/V(C2H6)=5/2=2.5��
��C2H6ȼ�պ������CO2��H2O��ȫ����Na2O2��Ӧʱ����ͨ���O2Ӧ���٣��ɷ���ʽC2H6+O2+5Na2O2��2Na2CO3+6NaOH��V(O2)/V(C2H6)=1/1
��O2��C2H6�������x��ȡֵ��ΧΪ1��V(O2)/V(C2H6)��2.5
(2)0.8��
n(Na2O2)=![]() =0.02mol��2C2H6+5O2+4Na2O2��4Na2CO3+6H2O(l)�ã�
=0.02mol��2C2H6+5O2+4Na2O2��4Na2CO3+6H2O(l)�ã�
![]() =
=![]()
![]() n(O2)=0.025mol��ͨ��O2���������ܳ���32g/mol��0.025mol=0.8g
n(O2)=0.025mol��ͨ��O2���������ܳ���32g/mol��0.025mol=0.8g
15.(1)n(H2O)=![]() =0.6moln(CO2)=
=0.6moln(CO2)=![]() =0.4mol��
=0.4mol��
CuO��+ CO��=��Cu +��CO2������m(����)��
������ 1mol������ ��1mol��������16g��
������ n(CO)������������������ 3.2g��
![]()
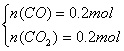
��ʵ���л���ȼ�ղ�����CO2Ϊ��0.4-0.2=0.2mol��
��0.2mol�л����к�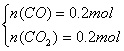
![]() 1mol�����C��H��O=2��6��2
1mol�����C��H��O=2��6��2
���л������ʽΪ��C2H6O2��
(2)n(Na)=![]() =0.4mol,0.2mol�л����ܺ�0.4molNa��Ӧ
=0.4mol,0.2mol�л����ܺ�0.4molNa��Ӧ
���Ը��л���Ϊ��Ԫ�����ṹ��ʽΪHO��CH2��CH2��OH��
16.(1)![]()
2-��-1��3-����ϩ(�������ϩ)��
(2)![]() ��������ϩ��
��������ϩ��