化学反应速率 化学平衡
班级 姓名
一.选择题(每小题只有一个正确答案)
1.对某一可逆反应来说,使用催化剂的作用是 ( )
A.提高反应物的平衡转化率 B.以同等程度改变正、逆反应的速率
C.增大正反应速率,减小逆反应速率 D.改变平衡混合物的组成
2.乙酸蒸气能形成二聚分子:2CH3COOH(气)==(CH3COOH)2(气)+Q。现欲测定乙酸的式量,应采用的条件是 ( )
A.高温低压 B.低温高压
C.低温低压 D.高温高压
3.在一定条件下,合成氨反应达到平衡后,混合气体中NH3的体积占25%。若反应前后条件保持不变,则反应后缩小的气体体积与原反应物体积的比值是 ( )
A.1/5 B.1/4 C.1/3 D.1/2
4.反应速率V与反应物浓度的关系是用实验方法测定的。化学反应H2+Cl2==2HCl的反应速率V可表示为V=k[H2]m[Cl2]n,式中k为常数,m、n的值可用下表中的数据确定。由此可推得m、n的正确值是 ( )
| [H2](mol/L) | [Cl2](mol/L) | V(mol・L-1・s-1) |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
A.m=1,n=1 B.m=1/2,n=1/2
C.m=1/2,n=1 D.m=1,n=1/2
5.某合成氨反应在恒容容器中达到平衡时,N2、H2、NH3的物质的量分别为a、3a、0.5a(mol),再向容器中通入0.2molN2、0.6molH2、0.1molNH3,平衡 ( )
A.向正反应方向移动 B.向逆反应方向移动
C.不发生移动 D.移动方向无法确定
二.选择题(每小题有1~2个正确答案)
6.在一定条件下的定容容器中,当下列物理量不再变化时,表明反应:A(固)+2B(气)==C(气)+D(气)已达平衡的是 ( )
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
7.有反应2X(气)=Y(气)+2Z(气)―Q在不用催化剂的条件下达到平衡,现要使正反应速率降低,且Y的浓度减小,可采用的措施是 ( )
A.升高温度 B.扩大体积
C.降低温度 D.缩小体积
8.在体积相同的注射器Ⅰ管和Ⅱ管里,分别吸入1/4容积颜色相同的NO2和Br2(气),把注射器前端密封后,将活塞同时向外拉,使容器的容积比原来扩大一倍,一段时间后观察到的现象是 ( )
A.Ⅰ管(盛NO2)内的气体颜色比Ⅱ管(盛Br2)内的颜色深
B.Ⅰ管内气体颜色比Ⅱ管内的深
C.两管内气体颜色相同
D.Ⅰ管内气体颜色可能比吸入时深
9.某密闭容器中放入一定量的NO2,发生反应2NO2==N2O4+Q,达平衡后,若分别单独改变下列条件,重新达平衡后,能使混合气体平均相对分子质量增大 的是 ( )
A.通入N2 B.通入NO2
C.通入N2O4 D.升高温度
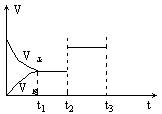 10.对于一个气态反应体系,图中表示的是反应速率和时间的关系,其中t1为到达平衡所需时间,则t2~t3是改变什么条件时可能出现的情况 ( )
10.对于一个气态反应体系,图中表示的是反应速率和时间的关系,其中t1为到达平衡所需时间,则t2~t3是改变什么条件时可能出现的情况 ( )
A. 加压
B.增大反应物浓度
B. 减压
C. D.加入催化剂
11.在密闭容器中,进行如下气体间的反应:A(气)+B(气)==C(气),若增大A的浓度而使平衡移动,下列叙述中正确的是 ( )
A.达到平衡时,A的转化率一定大于原平衡时A的转化率
B.达到平衡时,C的浓度一定大于原平衡时C的浓度
C.达到平衡时,C的百分含量一定大于原平衡时C的百分含量
 D.达到平衡时,B的转化率一定大于原平衡时B的转化率
D.达到平衡时,B的转化率一定大于原平衡时B的转化率
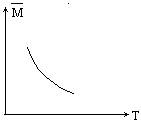
12.可逆反应2A+B==2C(气)+Q(Q>0)随温度变化气体平均相对分子质量如图所示,则下列叙述正确的是 ( )
A.A和B都可能是固体
B.A和B一定都是气体
C.若B是固体。则A一定是气体
D.A和B不可能都是气体
13.在一个容积固定的密闭容器中充入1molHI,建立如下平衡:2HI(气)==H2(气)+I2(气),测得HI的转化率为a%。其它条件不变,在上述平衡体系中再充入1molHI,待新平衡建立时HI的转化率为b%,则a、b的关系为 ( )
A.a>b B.A<b C.a=b D.无法确定
三.填空、证明题
14.已知氯水中有如下平衡:Cl2+H2O==HCl+HClO。常温下,在一个体积为50ml的针筒里吸入40ml氯气后,再吸入10ml水。写出针筒里可能观察到的现象。若将此针筒长时间放置,又可能看到何种变化?试用平衡观点加以解释。
15.若平均摩尔质量定义为混合物总质量除以混合物的总物质的量。据此判断,对反应
C(固)+H2O(气)==CO(气)+H2(气)达平衡后,在其它条件不变的情况下增大压强,混合气体的摩尔质量将如何变化?请加以证明。
16.298K时,合成氨反应的热化学方程式为:N2(气)+3H2(气)==2NH3(气)+92.4Kj,在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,试问实际测得反应放出的热量与92.4kJ的大小关系如何? ,理由是
。
四.计算题
17.在一定温度和压强下,将SO2和O2按5:3的体积比混和,反应达到平衡时混合气体体积缩小为原来的4/5。试求:
(1) SO2的转化率; (2)混合气体中SO2的体积分数;
(3) 平衡时混合气体的平均摩尔质量。
18.已知:常温下,1体积水溶解2.3体积氯气;饱和氯水中1/3量的氯气和水发生反应;氯化钠的溶解度为36g,其饱和溶液密度为1.18g/cm3;浓盐酸的溶质质量分数为36.5%,密度为1.20g/cm3。
试根据以上数据,通过计算加以说明:氯气中混有少量氯化氢气体,可通过饱和食盐水被吸收。