高二级化学单元目标检测题(理科) (B)
综合
满分100分,时间90分钟
可能用到的相对原子质量:H-1 Na 23 Mg 24 Al 27 Cl 35.5
第I卷 (选择题 共50分)
一、选择题(本题共25个小题,每小题只有一个选项符合题意,每小题2分,共50分)
1. 下列物质中酸性最强的是
A.H3PO4 B.HNO3 C.H2CO3 D.CH3COOH
2. 既会造成光化学烟雾,又会使臭气层遭到破坏的气体是
A.CO B.NO C.SO2 D.Cl2
3. 苯分子环状结构的提出者是
A.法拉第 B.米希尔里希 C.凯库勒 D.拉瓦锡
4. 实验室制取下列气体时,与实验室制取氯气的发生装置相同的是
A.C2H2 B.H2 C.C2H4 D.NH3
5. 纯水在20℃比在80℃时的PH
A.大 B.小 C.相等 D.不能确定
6. 只用一种试剂即可使NH4Cl,(NH4)2SO4,NaCl ,Na2SO4四种溶液区分开,这种试剂是
A.Ba(OH)2溶液 B.NaOH 溶液 C.BaCl2溶液 D.AgNO3溶液
7.
反应4NH3+5O2 ![]() 4NO+6H2O在5L密闭容器中进行,30s后NO的物质的量增加了6 mol,则此反应的平均速率为
4NO+6H2O在5L密闭容器中进行,30s后NO的物质的量增加了6 mol,则此反应的平均速率为
A.V(O2)=1 mol・L-・S- B.V(NO)=0.2 mol・L_・S-
C.V(H2O)=0.1 mol・L_・S- D.V(NH3)=0.5 mol・L_・S-
8.
对已达到平衡的下列反应:2X(g)+Y(g)![]() 2Z(g)减小压强时,对反应产生的影响是
2Z(g)减小压强时,对反应产生的影响是
A. 正、逆反应速率都减小,平衡向逆反应方向移动
B. 正、逆反应速率都增大,平衡向正反应方向移动
C. 逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
D. 逆反应速率减小,正反应速率增大,平衡向正反应方向移动
9. 下列物质中,不能用作饮用水处理剂的是
A.Al2(SO4)3 B.Cl2 C.Ca(ClO)2 D.SO2
10. 下列关于铝的叙述中,不正确的是
A.铝是地壳中含量最多的金属元素 B.铝属于第IIIA族元素
C.在常温下,铝不能与氧气反应 D.铝既能溶于酸,又能溶于强碱溶液
11. 下列烧杯中盛放的都是稀硫酸,在铜电极上不能产生气泡的是
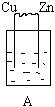
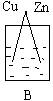
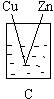
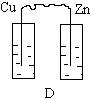
12. 下列各组离子中,能在溶液中大量共存的是
A.Ca2+ Na+ HCO3- B. Al3+ Ca2+ OH-
C.Mg2+ H+ HCO3- D.Fe2+ AlO2- Cl-
13. 在常温下,把一个盛有一定量甲烷和氯气的密闭玻璃容器放在光亮的地方,两种气体发生反应,下列叙述正确的是
A.容器内的原子总数不变 B.容器内的分子总数不变
C.发生的反应属于取代反应 D.容器内的压强不变
14. 下列物质中既不能与盐酸反应,又不能与氢氧化钠溶液反应的是
A.NaHCO3 B.NaCl C.Al(OH)3 D.(NH4)2CO3
15. 相同质量的镁和铝,分别与足量的盐酸反应,生成气体的体积比是
A. 1 :1 B. 1 :2 C. 2 :3 D. 3 :4
16. 下列物质中不能使溴水和高锰酸钾酸性溶液褪色的是
A.C2H2 B.C3H6 C.C5H12 D.C4H8
17. 一次性餐具目前最有发展前景的是
A.瓷器餐具 B.淀粉餐具 C.塑料餐具 D.纸木餐具
18. 区别浓H2SO4和稀H2SO4,既简单又可靠的方法是
A.各取少许溶液分别放入铜片 B.分别与石蕊试液作用
C.用玻璃棒各蘸少许液体涂在纸上 D.各取少许溶液分别加入BaCl2溶液
19. 除去溶解在苯中少量苯酚,正确的方法是
A.用过滤器直接过滤 B.用分液漏斗直接分液
C.通往入足量的CO2后过滤 D.加入过量NaOH溶液后,再分液
20. 下列物质中,可用来鉴别苯酚稀溶液、乙醇、氢氧化钠溶液和硝酸银溶液的一种试剂是
A.氯水 B.新制Cu(OH)2 C`Fe(NO3)3溶液 D.金属钠
21. 可用来清洗做完银镜反应实验后试管中银的试剂的是
A.盐酸 B.硝酸 C.烧碱溶液 D.蒸馏水
22.
向CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O的平衡体系中加入H218O,过了一段时间后,平衡体系中分子含有18O的有机物是
CH3COOC2H5+H2O的平衡体系中加入H218O,过了一段时间后,平衡体系中分子含有18O的有机物是
A.CH3COOH B. C2H5OH
C. CH3COOH和CH3COOC2H5 D. CH3COOH、CH3COOC2H5 和 C2H5OH
23. 油脂皂化后,使肥皂和甘油分离,可采用的方法是
A.萃取 B.蒸馏 C.结晶 D.盐析
24. 下列有机物的名称正确的是
A.2,3-二甲基丁烷 B.1,3,5-三甲基己烷
C.2-甲基-4-乙基戊烷 D.2-乙基丙烷
25. 下列说法中正确的是
A. 淀粉和纤维素是能水解成多个分子单糖的糖类
B. 淀粉和纤维素都是纯净物
C. 人造丝和蚕丝都是蛋白质
D. 分子式符合Cn(H2O)m的物质一定是糖类化合物
第I卷答题栏
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | |||||||||||||
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答案 |
第II卷(非选择题 共50分)
二、空题(本题9 个小题,共26分)
26.(3分)浓硝酸常常略显黄色是因为其中混有 杂质;浓硝酸使金属铝钝化是因为浓硝酸具有 ;浓硝酸与苯反应生成硝基苯,这一反应属于 反应。
27.(1分)元素A的原子比元素B的原子多一个电子层,A,B元素的单质能与水剧烈反应放出气体,所生成的两种气体混合点燃可发生爆炸,则A,B分别可能是 。
28.(3分)根据下图所示转化关系及现象,填写下列空白:
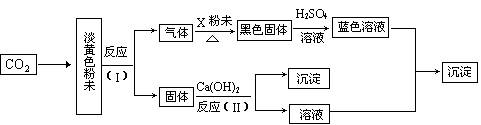
(1)X的名称为 ;
(2)反应(I)的化学方程式为 ;
(3)反应(II)的离子方程式为 。
29(4分)已知A、B、C、D分别是AlCl3 、BaCl2、 FeSO4 、NaOH四种化合物中的一种,它们的水溶液之间的反应现象如下:
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解
②B+D→白色沉淀
③C+D→白色沉淀,继续加入D溶液,白色沉淀消失
(1)A、C的化学式分别为:A. C 。
(2)C溶液与D溶液反应生成白色沉淀及其溶解于D溶液中的离子方程式为:
C+D→ 。
沉淀溶于D: 。
30.(2分)工业制CuSO4时,不是直接用铜跟浓H2SO4在加热条件下反应,而是将铜丝浸入稀H2SO4中,再不断由容器下部吹入细小的空气泡,这样做的好处是① ;② 。
31.(4分)现有三种烃:①C2H6②C2H4③C2H2,易发生取代反应的是(填序号,下同) ;易发生加成反应的是 ;碳碳键的键长由长到短的顺序为 ;通入或滴入酸性KMnO4溶液中,能使之褪色的是 。
32.(4分)某有机物A,由C、H、O三种元素组成,在一定条件下。有如下的转化关系:
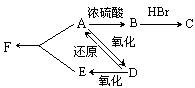
已知:E是食醋的主要成分,D可发生银镜反应。
(1) 写出B、D的名称和结构式
B. D.
(2) 写出下列转化的化学方程式,并指出反应类型。
A→B: 。
33.(1分)某有机物的结构简式为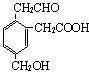 ,它在一定条件下可能发生下列反应:①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去中的(填序号): 。
,它在一定条件下可能发生下列反应:①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去中的(填序号): 。
34.(4分)选用合适的试剂除去下列物质中含有的杂质(括号内物质为杂质)
(1)Cu (Zn) (2) HCl (H2SO4)
(3)NaOH (Na2O2) (4)NaOH (Na2CO3)
三、简答题(本题3个小题,共14分)
35.(6分)2003年在我国广东、北京等地发生的“非典型肺炎”引起了许多人的恐慌。消毒、保持环境和个人卫生成了一项十分重要的工作。
(1) 现在请你用氯气、熟石灰为主要原料自制具有消毒作用的漂白粉(用化学方程式表示):
(2) 漂白粉的有效成分是 。
(3) 漂白粉的消毒原理是 。
36.(4分)在化学实验中,常常会有有害气体产生,试举出三种防止污染空气的方法。
37.(4分)只从下列试剂中选择实验所需的试剂,采用两种不同的方法区分0.1 mol・L_的H2SO4和0.01 mol・L_的H2SO4溶液,简述操作过程。
试剂:①紫色石蕊试液 ②酚酞试液 ③蒸馏水 ④BaCl2溶液 ⑤PH试纸 ⑥0.1 mol・L_的Na2SO3溶液
方法一: 。
方法二: 。
四、计算题(本题2个小题,共10分)
38.(4分)实验室用MnO2和浓盐酸反应制取Cl2,当有14.6gHCl被氧化时,求生成 Cl2在标准状况下的体积。
39.(6分)一种无色液态有机物有下列性质:①能与Na反应生成氢气 ②与碳酸钠不发生反应 ③该有机物的相对分子质量为60。
(1) 推断该物质属于哪一类有机化合物;
(2) 写出其分子式;
(3) 写出有机物可能有的同分异构体的结构简式。
综合B 答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | B | B | C | C | A | A | C | A | D | C | D | A | D |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答案 | B | D | C | B | C | D | C | B | A | D | A | A |
二、
26.NO2 氧化性 取代
27. Na F
28. (1) 铜 (2) 2Na2O2 + 2CO2 = 2Na2CO3 + O2
(3)CO32- + Ca 2+ = CaCO3 ↓
29. (1) A: BaCl2 C: AlCl3 (2) Al3+ + 3OH- = Al(OH)3↓ Al(OH)3+OH- = AlO2- + 2H2O
30.①减少硫酸用量 ② 不会产生对大气污染的SO2
31.①;②③;①②③;②③
32.(1) 己烯:![]() 乙醛 :
乙醛 :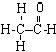
(2) CH3CH2OH ![]() CH2=CH2 +H2O ,消去反应
CH2=CH2 +H2O ,消去反应
33. ①③④⑤
34.(1)稀硫酸 (2)适量BaCl2 (3) 水 (4) 适量 Ca(OH)2
三、
35.(1)Cl2 +2Ca(OH)2 = CaCl2 +Ca(ClO)2 + 2 H2O (2)Ca(ClO)2
(3) Ca(ClO)2 +H2O + CO2 = 2HClO + CaCO3 ↓ H ClO是一种强氧化剂,能杀菌消毒。
36. ①点燃法。适用于具有可燃性,且点燃后产生的物质对空气无污染的气体
②溶液吸收法。如Cl2,可用NaOH溶液作尾气处理。
③用塑料袋或气球等收集起来,回收再利用。
37.方法一:用玻璃棒各蘸少许两种液体点在PH试纸上,用比色卡比色,PH小的为0.1mol/L的H2SO4
方法二:取等体积的BaCl2溶液于两支试管中,同时分别加入等体积的两种溶液,先出现浑浊的为0.1mol/L的H2SO4。
四、
38.4.48L
39.(1)醇类 (2)C3H8O (3) ![]()
![]()