高二下期第一学月化学考试题
命题人:吕建中
可能用到的原子量:C-12,O-16,H-1。
一、选择题(本题包括20小题,每小题2分,共40分。每题只有1个选项符合题意)
1.居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料会释放出一种刺激性气味的气体,该气体是 ( )
A.甲烷 B.氨气 C.甲醛 D.二氧化硫
2.在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是 ( )
A.CH4和C2H4 B.CH4和C2H6 C.C2H4和C2H6 D.C3H4和C3H6
3.下列有机物中,既能使溴水褪色,又能使酸性KMnO4溶液褪色,还能与新制Cu(OH)2发生反应生成沉淀的是 ( )
A.1,3―丁二烯 B.苯酚 C.对一二甲苯 D.丙烯醛
4.能证明乙醇中含有水的试剂是
A、无水硫酸铜粉末 B、新制生石灰 C、金属钠 D、胆矾
5.“可燃冰”是天然气与水相互作用形成的晶体物质,主要存在于冻土层和海底大陆架中。
据测定每0.1m3固体“可燃冰”要释放20m3的甲烷气体,则下列说法中不正确的 ( )
A.“可燃冰”释放的甲烷属于烃 B.“可燃冰”是水变油,属于化学变化
C.“可燃冰”将成为人类的后续能源 D.青藏高原可能存在巨大体积的“可燃冰”
6.甲烷和乙烯的混合气体100 mL ,能催化加成氢气30 mL ,则混合气体中含有甲烷( ) A.50 mL B.70 mL C.30 mL D.15 mL
7.比较丙烷的二氯取代物和六氯取代物的种类,前者与后者比较 ( ) A.前者多 B.后者多 C.一样多 D.无法确定
8.下列说法中正确的是 ( )
A.乙烯和乙炔都能使溴水褪色,但与乙炔反应时消耗的溴要比等物质的量的乙烯反
应消耗的多
B.乙炔有特殊难闻的气味
C.乙炔可用电石与水反应而制得,故实验里最好选用启普发生器为气体的发生装置
D.乙炔含碳量比乙烯含碳量高,等物质的量的乙炔和乙烯燃烧时,乙炔所耗氧气多
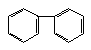
![]() 9.下列物质中,属于芳香烃且属于苯的同系物的是
( )
9.下列物质中,属于芳香烃且属于苯的同系物的是
( )
![]()
![]() A.
B.
C.
D.
A.
B.
C.
D.
10.下列反应中,不属于取代反应的是 ( )
A.在催化剂存在条件下苯与溴反应制溴苯
B.苯与浓硝酸、浓硫酸混合共热制取硝基苯
C.苯与浓硫酸共热制取苯磺酸
D.在一定条件下苯与氢气反应制环己烷
11.一氯代物的同分异体有两种,二氯代物的同分异构体四种的烷烃是 ( )
A.甲烷 B.丙烷 C.丁烷 D.环丁烷
12.分离水和1―氯丁烷的混合物的正确方法是( )
A、分馏 B、过滤 C、分液 D、加入溴水
13.下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是 ( )
A.甲苯能反应生成三硝基甲苯 B.甲苯能使酸性高锰酸钾溶液褪色
C.甲苯燃烧产生带浓烟的火焰 D.1 mol甲苯与3 molH2发生加成反应
14.等质量的下列烃完全燃烧,消耗氧气最多的是 ( )
A.CH4 B.C2H6 C.C3H6 D.C6H6
15.下列反应属于有机物的还原反应的是 ( )
![]() A.CH2=CH2 + H-OH
A.CH2=CH2 + H-OH ![]() CH3CH2OH
CH3CH2OH
B.H2 + Cl2 2HCl
C.![]() +H2
+H2
![]() CH3CH2OH
CH3CH2OH
![]() D.CH3CH3 + 2Cl2
D.CH3CH3 + 2Cl2
![]() +2HCl
+2HCl
16、某学生将1―氯乙烷与NaOH溶液共热几分钟后,冷却,滴入AgNO3溶液,结果未见到白色沉淀生成,其主要原因是( )
A、加热时间太短 B、不应冷却后再加入AgNO3
C、加AgNO3溶液前未用稀硝酸酸化 D、反应后的溶液中不存在Cl―
17、1,4―二氧六环是一种常见溶剂,它可以通过以下方法合成:
 |
A 烃类 B C
则烃A为 ( )
A、1―丁烯 B、1,3―丁二烯 C、乙炔 D、乙烯
18、分离苯和苯酚的混合物,通常采用的方法是 ( )
A.加水振荡后,用分液漏斗分离 B.加稀盐酸振荡后,用分液漏斗分离
C.加入浓溴水振荡后过滤 D.加NaOH溶液振荡后,用分液漏斗分离,取下层液体通入CO2或加入适量盐酸后,再用分液漏斗分离
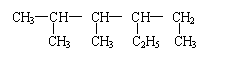 19.某烷烃的结构为:
,下列命名正确的是 ( )
19.某烷烃的结构为:
,下列命名正确的是 ( )
A.
1,2-二甲基-3-乙基戊烷 B. 3-乙基-4,5-二甲基已烷
C .4,5-二甲基-3-乙基已烷 D. 2,3-二甲基-4-乙基已烷
20.物质的量相等的下列烃,在相同条件下完全燃烧,耗氧量最多的是 ( )
A.C2H6 B.C3H6 C.C4H6 D.C7H8
二、选择题(本题包括5小题,每小题3分,共15分。每题有1-2个选项符合题,少选
扣1分,多选、错选均不给分)
21.某烃分子中有1个环状结构和2个双键,它的化学式可能是 ( )
A.C2H4 B.C7H8 C.C5H6 D.C10H8
22.有五种无色试剂:C2H5OH、NaOH、C6H5OH、AgNO3,可将它们一一鉴别出来的是( )
A.溴水 B.盐酸 C.氯化铝溶液 D.氯化铁溶液
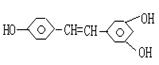
23、白藜芦醇(见下图)广泛存在于食物中,它可能具有抗癌性。能够跟1mol该化合物起反应的Br2或H2的最大用量分别是
|
A.1mol、1mol B.3.5mol、7mol
C.3.5mol、6mol D.6mol、7mol
24.下列烷烃分子中去掉一个氢原子后所得的烃基不止一种的是 ( )
A.甲烷 B.乙烷 C.丙烷 D.丁烷
25.有一类组成最简单的有机硅化合物叫硅烷,它的分子组成与烷烃相似。下列有关说
法中错误的是 ( )
A.硅烷的分子通式可表示为SinH2n+2
B.甲硅烷燃烧生成二氧化硅和水
C.甲硅烷(SiH4)相同条件下的密度小于甲烷(CH4)
D.甲硅烷的热稳定性强于甲烷
三、填空题
26、写出下述化学方程式(有机物用结构简式表示):
(1)实验室制乙烯
(2)实验室实验室制乙炔
(3)苯酚与足量浓硝酸、浓硫酸的混合液反应
(4)乙二醛的还原反应
(5)丙醛的银镜反应
27、已知丙烯在某种催化剂、450℃下可与氯气反应生成CH2=CH-CH2Cl,再经一系列反应得丙烯酸,最后聚合成聚丙烯酸,试依次写出各步反应的化学方程式(有机物用结构简式表示)。
28.(6分)某烃A和炔烃B的混合物共1L,完全燃烧生成相同状况下的二氧化碳1.4L,
水蒸气1.6L,写出两种烃的结构简式.A ________________;B _________________,
两者物质的量之比为._______________。
29.配制银氨溶液时,把氨水滴入硝酸银溶液的操作关键是 ;把苯酚晶体加入试管内的热水中得澄清的溶液,把试管浸入冷水中,溶液变浑浊,这是因为 ,
再往试管内滴入氢氧化钠溶液又变澄清,其反应方程式是: ,
再通入CO2又变浑浊,该反应的离子方程式为 。
30.(5分)下列各组物质 ① O2和O3 ② H2、D2、T2 ③ 12C和14C ④ CH3CH2CH2CH3 和 (CH3)2CHCH3 ⑤乙烷和丁烷 ⑥ CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH2CH(CH3)C2H5
互为同系物的是__________, 互为同分异构体的是_____________, 互为同位素的是______, 互为同素异形体的是__________, 是同一物质的是__________。
31.(6分)自20世纪90年代以来,芳炔类大环化合物的研究发展十分迅速,具有不同分子结构和几何形状的这一类物质在高科技领域有着十分广泛的应用前景。合成芳炔类大环的一种方法是以苯乙炔(CH≡C-![]() )为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
)为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
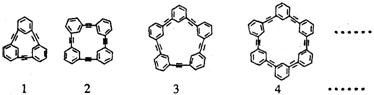
(1)上述系列中第1种物质的分子式为 。
(2)以苯乙炔为基本原料,经过一定反应而得到最终产物。假设反应过程中原料无损失,理论上消耗苯乙炔与所得芳炔类大环化合物的质量比为 。
(3)在实验中,制备上述系列化合物的原料苯乙炔可用苯乙烯(CH2=CH-![]() )为起始物质,通过加成、消去反应制得。写出由苯乙烯制取苯乙炔的化学方程式(所需的无机试剂自选)
)为起始物质,通过加成、消去反应制得。写出由苯乙烯制取苯乙炔的化学方程式(所需的无机试剂自选)
32、卤代烃在氢氧化钠存在条件下水解,这是一个典型的取代反应,其实是带负电的原子团(如OH-等阴离子)取代了卤代烃中的卤原子。
例如:CH3CH2―Br+OH-(或NaOH)→CH3CH2―OH+Br-(或NaBr)
试写出下列反应的化学方程式:(1)溴乙烷与NaHS反应;(2)碘甲烷与CH3COONa反应;
(3)由碘甲烷、无水乙醇和金属钠合成甲乙醚(CH3―O―CH2CH3)。
33.(4分)有A、B两种烃,它们的组成相同,都含90%的碳,烃A对氢气的相对密度是20;烃B式量是烃A的3倍,烃A在一定条件下能与足量的Cl2起加成反应,生成1,1,2,2-四氯丙烷,烃B是苯的同系物,当它与Cl2发生取代反应时(取代苯环上的H原子),生成的一氯代物、二氯代物、三氯代物分别都只有一种,根据以上实验事实,推断A、B两烃的分子式、结构简式分别为A、 、 ;B、 、 。
四、计算题
34.取某有机物3.7g 完全燃烧,只生成CO2、H2O,质量分别为8.8g、4.5g;该有机物与钠反应,产生H2;该有机物的相对氢气密度为37;求该有机物的分子式并写出可能的结构简式。
高二下期第一学月化学考试答题卷
班,班内学号 姓名 总分
一、选择题 (20小题,每小题2分,每小题只有一个答案符合题意)
| 1、C | 2、A | 3、D | 4、A | 5、B | 6、B | 7、C | 8、A | 9、B | 10、D |
| 11、B | 12、C | 13、A | 14、A | 15、C | 16、C | 17、D | 18、D | 19、D | 20、D |
二、选择题(本题包括5小题,每小题3分,共15分。每题有1-2个选项符合题,少选扣1分,多选、错选均不给分)
| 21、C | 22、AD | 23、D | 24、CD | 25、CD |
三、填空题
|
|
|
|
|
![]()
![]()
![]()
![]() n CH2=CH-COOH
[ CH2-CH ]n
n CH2=CH-COOH
[ CH2-CH ]n
COOH
28.(6分)A、CH4;B、CHΞCH ;比为3:2 。
29、(4分)逐滴加入,边滴边振荡至沉淀恰好溶解;苯酚在常温时的水溶性远低于65℃以上时的;C6H5OH + NaOH → C6H5ONa + H2O ;
C6H5O- + CO2 +H2O →C6H5OH + HCO3- .
30、(5分)⑤、④、③、①、⑥。
31、(5分)(1)C24H12;(2)51:50;
|
![]()
![]() ―CHBrCH2Br + 2NaOH
CH≡C-
―CHBrCH2Br + 2NaOH
CH≡C-![]() +
2NaBr + 2H2O
+
2NaBr + 2H2O
32、(4分)(1)C2H5Br + NaHS → C2H5HS + NaBr
(2)CH3I + CH3COONa → CH3OOCCH3 + NaI
(3)2C2H5OH + 2Na→2C2H5ONa + H2↑; C2H5ONa + CH3I→C2H5OCH3 +NaI;
33、(4分)A、C3H4、CHΞC-CH3;B、C9H12、略 。
四、计算题
34、(7分)解: 3.7g该有机物
含C的物质的量为:8.8g/44g/mol=0.2mol ;
含H的物质的量为:4.5g/18g/mol×2=0.5mol ;
含O的物质的量为:(3.7g-2.4g-0.5g)÷16g/mol=0.05mol ;
故此有机物的最简式为:C4H10O ;
该有机物相对分子质量为:37×2=74 ,故其分子式也为C4H10O ;
结构简式可能为:CH3CH2CH2CH2OH ;CH3CH2CHOHCH3 ;
(CH3)3COH ; (CH3)2CHCH2OH 。