高二下学期化学期末考试A
本试卷分卷Ⅰ和卷Ⅱ两部分,卷Ⅰ共4页为选择题,卷Ⅱ共3页为非选择题。
本试卷共计100分,考试时间90分钟。
注意事项:1。答卷前,考生务必将自己的姓名、考试号、科目填涂在答题卡上,考试结束,监考人员将答题卡收回。
2。每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。答在试卷上无效。
卷 Ⅰ(选择题,共45分)
相对原子质量 H 1 C 12 O 16 Cl 35.5
一、选择题(每小题只有一个选项符合题意,本题共9小题,每小题2分,共18分)
1. 下列各项中两种物质均为化合物的是 [ ]
A. 重水 王水 B. 干冰 冰醋酸
C.汽油 煤油 D.水玻璃 硫酸铝钾
2.等质量的下列气体,在同温度下充入相同容积的密闭容器内,测得其压强最
大的是[ ]
A.氢气 B.甲烷 C.一氧化碳 D.氧气
3.同周期的X、Y、Z三种主族元素,已知它们的最高价氧化物对</PGN0301.TXT/PGN>应水化物是HXO4、
H2YO4、 H3ZO4,则下列判断正确的是 [ ]
A.含氧酸的酸性:H2ZO4>H2YO4>HXO4
B.元素的非金属性:X>Y>Z
C.气态氢化物的稳定性按X、Y、Z顺序由弱到强
D.简单阴离子的还原性按X、Y、Z的顺序减弱
4.下列反应产生的气体,对空气不会造成污染的是 [ ]
A.浓盐酸和二氧化锰 B.硫化亚铁和稀硫酸
C.二氧化碳和过氧化钠 D.煅烧硫铁矿石
5.设NA代表阿伏加德罗常数,下列说法不正确的是 [ ]
A.3.55g氯气由分子变为氯离子时,得到的电子数为0.1NA
B.20g重水(D2O)所含的电子数为10NA
C.22.4L氮气所含的原子数为2NA
D.常温下,1mol氩气所含的原子数为NA
6.实验室制取下列气体,反应物都为固态,且都可用相同的排空气集气法收集
的是[ ]①CH4 ② Cl2 ③ H2S ④ HCl ⑤ SO2 ⑥ O2 ⑦ H2 ⑧ NH3⑨ CO2
A.③⑦⑨ B.①⑥⑧ C.①⑧ D.②④
7. 维通橡胶是一种耐腐蚀、耐油、耐高温、耐寒性能都特别好的氟橡胶。它的结构
简图见右图:![]() 。合成它的单体为:
。合成它的单体为:
A.氟乙烯和氟异丙烷 B.1,1―二氟乙烯和全氟丙烯
C.1―三氟甲基―1,3丁二烯 D.全氟异戊二烯
8.下列离子方程式中,正确的是 [ ]
A.在氯化铝溶液中加入过量氨水Al3+ + 3OH-= Al(OH)3↓
B.在硫酸铜溶液中加入过量氢氧化钡溶液Ba2++SO42-= BaSO4 ↓
C.在澄清石灰水中通入过量二氧化碳OH-+CO2= HCO3-
D.在碳酸氢钙溶液中加入过量氢氧化钠溶液Ca2++HCO3-+OH-= CaCO3↓+H2O
9.将100℃时某物质的饱和溶液93g冷却到40℃时,析出晶体13g(不含结晶水),
剩余的溶液中溶质的质量分数为37.5%。则此物质在100℃时的溶解度 为
[ ]
A.86g B.60g C.43g D.37.5g
二、选择题(每小题有1~2个选项符合题意,共9小题,每小题3分,共27分。)
10.将一定量的乙烷、丙烷混合气体完全燃烧,生成3.52g CO2和1.98g H2O,
则混合气体中乙烷和丙烷的体积比为 [ ]
A.1∶2 B.2∶1 C.1∶3 D.3∶2
11.某无色透明溶液中放入铝片,即刻有大量氢气产生,则下列离子在该溶液中
一定能大量存在的是 [ ]
A. Na+ B. Fe2+ C.NO3- D.HCO3-
12.有机物甲能发生银镜反应,甲经催化加氢还原为乙,1mol乙与足量钠反应产生氢气22.4L(标准状况下),据此推断乙可能是:
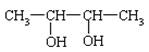 A.CH3―CH2―OH
B.CH3―CH2―CH2―OH
A.CH3―CH2―OH
B.CH3―CH2―CH2―OH
C.HO―CH2―CH2―CH2―OH D.
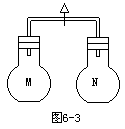
13.如图6-3,室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温
![]() 同压), 当
处接通,使两烧瓶内气体相互接通后,容器内压强由大到小顺
同压), 当
处接通,使两烧瓶内气体相互接通后,容器内压强由大到小顺
序正确的是 [ ]
编号: ① ② ③ ④
M H2S HCl SO2 NO
N SO2 NH3 O2 O2
A.④①③② B.④③①② C.③④①② D.②④①③
14.质量相同的下列混合气体不管混合比例如何变化,完全燃烧后生成的CO2和
H2O的质量都不会改变的是 [ ]
A.乙烷和乙烯 B.乙炔和苯蒸气
C.甲醛和乙酸蒸气 D.丙烯和丙炔
15.等物质的量的下列各有机物,完全燃烧耗氧量最大的是: [ ]
A.CH4 B.CH2O C.CH3OH D.CH3COOH
16.以下实验能获得成功的是: [ ]
A.用含结晶水的醋酸钠和碱石灰共热制甲烷气体
B.将铁屑、液溴、苯混合制溴苯
C.在苯酚溶液中滴入少量稀溴水出现白色沉淀
D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
17.体积为V mL,密度为d g/mL的溶液,含有分子量为M的溶质m g。其物质
的量浓度为c mol/L,质量分数为ω%,下列关系式中正确的是 [ ]
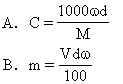
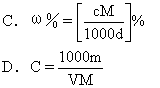
18.某期刊物封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或叁健。不同颜色的球代表不同元素的原子,该模型图可代表一种:
A.卤代羧酸 B.酯
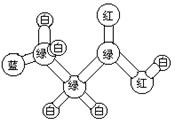 C.羧酸
D.醇钠
C.羧酸
D.醇钠
卷 Ⅱ(主观题 共55分)
三、填空题(本题共6小题,共49分。)
20.(6分)某溶液A可能含有Cu2+、NH4+、Al3+、Mg2+、Na+、
Fe3+、SO42-中的几种。若取A溶液加固体Na2O2,
有无色无味气体放出,并生成白色沉淀,加入Na2O2
的量x与生成沉淀的量y用图6-4表示。
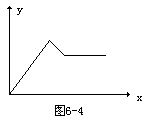
问:(1) A中一定存在的离子有________</PGN0305.TXT/PGN>
(2) A中一定不存在的离子有__________
(3) A中可能存在的离子是____________
21.(6分)亚硫酸钠中有+4价的硫,它既有氧化性,又有
还原性。现有试剂:溴水、硫化钠溶液、Na2SO3溶液、
稀硫酸、NaOH溶液、氨水。问:
(1)要证明Na2SO3具有还原性,应选用的试剂是______,
看到的现象是__________________,反应的离子方程为
___________________________________________。
(2)要证明Na2SO3具有氧化性,应选用的试剂为_______,
看到的现象是_________________,反应的离子方程为
_______________________________________。
22.(4分)配平下列反应的化学方程式:
____K2S +____HNO3(稀)―___KNO3 + S +___NO + ___H2O,
电子转移总数为______,若有4mol HNO3参加反应,其中有______mol硝
酸被还原。
23.(10分)分子中只含有2个碳原子的某烃A是其同系物中含碳量最高的物质;
1mol A与1mol HCl加成可得到B;1mol A与1mol H2加成可得到C,并能
继续发生如下列图表所示的转变:</PGN0306.TXT/PGN>
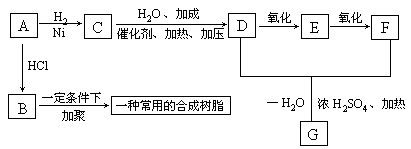
据此回答下列问题
(1)写出实验室制取A的化学方程式
_________________________________________________________。
(2)B的名称为__________,以B为原料经过加聚反应所得的合成树脂的结构简
式为_______________________。
(3)将铜丝灼热到表面生成一薄层黑色的氧化铜后,立刻插入D中,铜丝能复原
成紫红色。这个反应的化学方程式是:
_________________________________________________________________。
(4)写出E与新制Cu(OH)2悬浊液共热的化学方程式
________________________________________________________________。
(5)G的结构简式为_________________________。
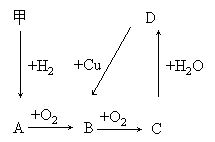
24.(10分)单质甲能发生如下变化(反应条件均未标明)。其中A、B、C、D都含
有相同的一种元素,试举出两个符合题意的实例,写出对应物质的化学式:
甲_________, A_________,B_________,C_________,D_________;
甲′_______, A′_______,B′_______,C′_______,D′_______。
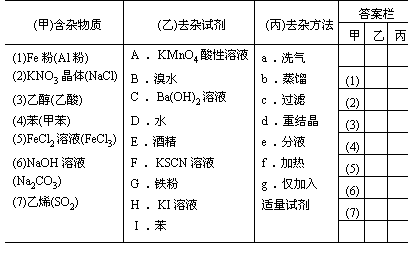
25.(14分)为了除去下表甲栏中的少量杂质(括号内为杂
质),请选择乙栏中的试剂和丙栏中的操作方法,用
编号填写在“答案栏”内。</PGN0307.TXT/PGN>
四、计算题(5分)
26.某饱和一元醇与足量钠反应生成0.5g氢气。用等量
的此醇在空气中燃烧生成36g水。求此醇的分子式
并写出其结构简式。
下学期高二化学期末考试答案
一、1.B 2.A 3.B 4.C 5.C 6.C 7.B 8.C 9.A
二、10.A 11.A 12.C 13.C 14.BC 15.AD 16.BD
17.BD 18.A
![]()
21.(1)溴水,溴水褪色,
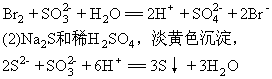
22.3,8――6,1,2,4, 6e, 1
23.(1)CaC2+2H2O→Ca(OH)2+C2H2↑
![]()
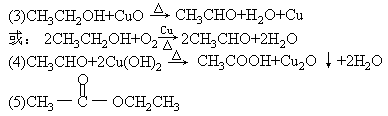
24.S,H2S,SO2,SO3,H2SO4;N2,NH3,NO,NO2,HNO3
25.甲:(1)(2)(3)(4)(5)(6)(7)
乙:CDCAGCC
丙:cdbecca
![]()