高二下学期期中化学试题
(文科专用 有机检测)命题人 。薛全锦
一、选择题 【 每小题3分 共51分】
1.下列关于烃的说法中,正确的是 ( )
A.烃是指分子里含有碳、氢元素的化合物
B.烃是指分子里含有碳元素的化合物
C.烃是指燃烧反应后生成二氧化碳和水的化合物
D.烃是指仅由碳和氢两种元素组成的化合物
2.下面烃的名称是 ( )
![]() A.2-甲基-3-乙基丁烷 B.3,4-二甲基戊烷
A.2-甲基-3-乙基丁烷 B.3,4-二甲基戊烷
C.2,3-二甲基-4-乙基丙烷 D.2,3-二甲基戊烷
3.下列物质中,其分子式为C6H14的可能是 ( )
A.2-甲基丁烷 B.2,3-二甲基戊烷
C.2-甲基己烷 D.2,3-二甲基丁烷
4. 同分异构体具有 ( )
A.相同的式量和不同的组成 B.相同的分子组成和不同的式量
C.相同的分子结构和不同的式量 D.相同的分子组成和不同的分子结构
5.下列各对物质中,互为同系物的是 ( )
A.CH3-CH3和CH3-CH=CH2 B.CH3-CH=CH2和CH3-CH2CH=CH2
C.CH3-CH2-CH3和CH3-CH=CH2 D.CH3-CH2C≡CH和CH3-CH=CH2
6.下列关于烷烃和烯烃的说法中,不正确的是 ( )
A.它们所含元素的种类相同,但通式不同
B.均能与氯气反应
C.烯烃分子中的碳原子数≥2,烷烃分子中的碳原子数≥1
D.含碳原子数相同的烯烃和烷烃互为同分异构体
7.1moL某气态烃完全燃烧,生成3moL CO2和3moL H2O,此烃是 ( )
A.C3H4 B.C3H6 C.C3H8 D.C4H10
8.与新制的氢氧化铜共热,出现砖红色沉淀的物质是 ( )
A.福尔马林 B.稀硫酸 C.苯酚溶液 D.醋酸
![]()
![]() 9.下列有机物:①CH3CH2COOH ②CH3OH ③ ④CH3CHO ⑤ ,
9.下列有机物:①CH3CH2COOH ②CH3OH ③ ④CH3CHO ⑤ ,
能发生银镜反应的有 ( )
A.③ B.②③⑤ C.①② D.④
10.醋酸乙酯在KOH溶液催化下水解得到的产物是 ( )
A.乙酸和乙醇 B.乙酸钾和乙醇 C. 甲酸和乙醇 D.乙酸和甲醇
11.根据下列物质结构的官能团判断CH2―CH=CH―COOH不能发生的反应( )
A.酯化反应 B.加聚反应
C.加成反应 D.银镜反应
12.针对下图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的是 ( )
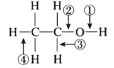 A.与醋酸、浓硫酸共热时,②键断裂
A.与醋酸、浓硫酸共热时,②键断裂
B.与金属钠反应时,①键断裂
C.与浓硫酸共热至170 ℃ 时,② 、④ 键断裂
D.在Ag催化下与O2 反应时,① 、③ 键断裂
13.下列实验处理方法正确的是 ( )
A.苯酚不慎沾到皮肤上,应立即用酒精洗涤
B.长期盛放石灰水的试剂瓶壁上的残留物用水洗
C.沾附在试管内壁上的铜,用稀盐酸洗涤
D.做银镜反应后残留物,用稀氨水洗涤
14.下列说法正确的是 ( )
A.凡能发生银镜反应的有机物一定含醛基
B.在氧气中燃烧时,只生成CO2和H2O的物质一定是烃
C.苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸
D.在酯化反应中,羧酸脱去羧基中的氢,醇脱去羟基而生成水和酯
15、将淀粉浆和淀粉酶的混合物放入玻璃纸袋中,扎好后浸入流动的蒸馏水中,过较长时间后,取出袋内液体,分别与碘水,新制的Cu(OH)2浊液(可加热)、浓硝酸(可微热)作用,其现象分别是( )
A.显兰色、无外观变化、显黄色
B.显兰色、有红色沉淀、无外观变化
C.无外观变化、无外观变化、显黄色
D.无外观变化、有红色沉淀、无外观变化
16、在酸性条件下可以水解生成两种物质A和B,且A和B的分子量相同,该物质是( )
A.蔗糖 B.麦芽糖 C.淀粉 D.甲酸乙酸
17、用来证明淀粉已部分水解的试剂是( )
A.碘水 B.KI溶液 C.银氨溶液 D.FeCl3溶液 二、填空题【每空1分供31分】
18.烷烃的通式是 (用n表示碳原子个数,下同);烯烃的通式是 ; 炔烃的通式是 。
19.烷烃同系物的通式为 ,分子中碳原子数相差n个,则相对分子质量相差 ,1mol某烷烃完全燃烧时耗O2为 mol ,生成水 mol 。
苯属于 烃,化学式为 ,结构简式为 。苯分子中6个C原子之间的键是一种介于 特殊的化学键,在一般情况下, 加成, 取代 (易或难)。
20.现有六种链烃: ①C6H12 ②C9H16 ③C15H32 ④C16H32 ⑤C8H16 ⑥C8H14 其中属于烷烃的是__________,属于烯烃的是_____ _____,属于炔烃的是___________(填序号)。
21.从结构上看,烃的衍生物是 分子中的 原子被 的产物。决定烃的衍生物化学特性的 或 叫做官能团,例如:决定乙醇、乙醛和乙酸化学特性的官能团分别是 、 、 。
22.乙醇俗称 ,其结构简式为 ,乙醇可以看作是水分子里的氢原子被乙基取代的产物。写出乙醇与金属Na 反应的方程式: 。
23.乙酸又叫 ,它是日常调味品 的主要成分。乙酸在水中的电离方程式是 ,其酸性比碳酸 。(填“强”或“弱”) 三。 实验室用右图装置制取乙酸乙酯:【8分】
24. (1)在大试管中配置一定比例的乙醇、浓H2SO4和乙酸的混合液的方法是_____________
。
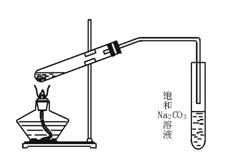 (2)加热前,大试管中加入几粒碎瓷片的作用是______
_,导气管不能插入饱和Na2CO3溶液中是为了______
。
(2)加热前,大试管中加入几粒碎瓷片的作用是______
_,导气管不能插入饱和Na2CO3溶液中是为了______
。
(3)浓H2SO4的作用是:①_________ _,②_________ _。
(4) 实验室制取的乙酸乙酯,其密度比水________(填“大”或“小”),有___ ___气味。
四、计算题 【10分】
25.将11.2升(标准状况)乙烯和乙烷的混合气体通入足量的溴水中,充分反应后,溴水溶液的质量增加了8.4g。求原气体混合物中乙烯与乙烷的物质的量和质量各多少?
参考答案:
1.D 2.D 3.D 4.D 5.B 6.D 7.B 8. A 9.D 10.B 11.D 12.A 13A .A 14.A 15D 16.A 17.AC
18.CnH2n+2,CnH2n, CnH2
![]() 19.CnH2n+2,14n,
19.CnH2n+2,14n,![]() ,n+1,芳香,C6H6,
,n+1,芳香,C6H6,
20.③,①④⑤,②⑥
21.烃 H 其它原子或原子团 原子 原子团 羟基 醛基 羧基
22.酒精 ![]()
![]()
23.醋酸 食醋 ![]() 强
强
24.(1)略 (2)防暴沸 防止受热不均引起倒吸 (3)催化剂 吸水剂
(4)小 果香
25.乙烯:8.4g 0.3mol
乙烷:6g 0.2mol