高二有机复习(有机计算)
复习目标:
掌握有机物的相对分子质量及确定分子式的计算方法,掌握有机物通式及燃烧通式的应用
知识要点:
一、烃及烃的含氧衍生物燃烧规律
1、气态烃完全燃烧前后体积的变化规律
任何一种气态烃CxHy完全燃烧前后体积是如何变化的?(反应前后温度不变且高于100℃)
例1.两种气态烃以任意比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L.下列各组混合烃中不符合此条件的是
(A)CH4 C2H4 (B)CH4 C3H6 (C)C2H4 C3H4 (D)C2H2 C3H6
2、等质量的烃完全燃烧时耗氧量大小的规律
对于烃(CxHy),当质量一定时, 元素的质量百分含量越大,即 的值越大,其耗氧量也就越大;质量相等的两种烃完全燃烧时若耗氧量相等,则这两种有机物的 必然相同。
3、物质的量相等的烃(CxHy)及其含氧衍生物(CxHyOz)完全燃烧时的耗氧量取决于 ,
其值越大,耗氧量越多。
4、混合物总物质的量一定,无论以何种比例混合,下列情况下必须满足的条件是
(1)产生CO2的量为一定值
(2)产生H2O的量为一定值
(3)耗氧量为一定值
5、混合物总质量一定,无论以何种比例混合,下列情况下必须满足的条件是
(1)产生CO2的量为一定值
(2)产生H2O的量为一定值
(3)耗氧量为一定值
例2.在下列烃中
〔 〕①等质量完全燃烧耗O2量最大的是;
〔 〕②等物质的量完全燃烧耗O2量最大的是
A. C3H8 B.C4H6 C.C2H2 D.C2H6
例3.对于下列各组内的两种有机物,
〔 〕①等质量完全燃烧耗O2量相等的是;
〔 〕②等物质的量完全燃烧耗O2量相等的是
A.甲醛和乙酸 B.甲烷和乙酸 C.乙烯和丙烯 D.乙炔和乙醛
例4.下列各组混合物,无论两组分以何种比例混合,只要混合物的总质量一定时
〔 〕完全燃烧时耗氧量不变的是
〔 〕生成水的量一定的是
A. CH3COOH和HCHO B.C2H6和C3H6 C. C7H8和C3H8O3 D.C4H10和C4H8
例5.下列各组混合物,无论两组分以何种比例混合,只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗氧气的质量均不变的是
A.C3H6和C4H6O2 B. C2H4和C2H6O
C.C2H2和C6H6 D.CH4O和C3H4O5
例6.有机化合物A、B分子式不同,它们只可能含碳、氢、氧元素中的两种或三种.如果将A、B不论以何种比例混和,只要其物质的量之和不变,完全燃烧时所消耗的氧气和生成的水的物质的量也不变.那么,A、B组成必须满足的条件是 .若A是甲烷,则符合上述条件的化合物B中,分子量最小的是(写出分子式) ,并写出分子量最小的含有甲基(-CH3)
的B的2种同分异构体结构简式 。
二、有机物分子组成通式的应用
规律1 最简式相同的有机物(或某些元素最简比相同的有机物),无论多少种以任何比例混合,混合物中元素的质量比值相同(应为一常数)
例:由乙炔、苯、乙醛组成的混合物,经测定其中碳的质量分数为0.72 ,则氧的质量分数
为 。
(MCE98)5、某种ABS工程树脂,由丙烯腈(CH2=CHCN,符号A)、1,3-丁二烯(CH2=CH-CH=CH2,符号B)和苯乙烯(C6H5-CH=CH2,符号S)按一定配比共聚而得。
(1)A、B和S三种单体中,碳氢比(C:H)值最小的单体是
。
(2)经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比是
(用a、b、c表示)。
规律2、具有相同的相对分子质量的有机物为(思考?)
(1)
(2)
(3)
(优化设计P489)例:某有机物在气态时与相同状况下的氦气密度之比为18.5:1,又知14.8g该有机物与足量金属钠反应放出0.2gH2,符合此条件的有机物可能有:
A.3种 B.4种 C.5种 D.6种
二、有机物分子式的确定
1、根据燃烧产物的质量、元素的质量分数确定分子式
例7 某有机物由C、H、O三种元素组成,其相对分子质量为76。0.05mol该有机物完全燃烧的产物用碱石灰完全吸收,碱石灰增重6.2g。相同质量的该有机物完全燃烧后的产物通过Na2O2,它只增重3 g。求
(1)该有机物的分子式(2)若该有机物既能与乙醇又能与乙酸发生酯化反应,写出该有机物的结构简式。该有机物相互间反应能生成具有四个氧原子的酯,写出该反应的化学方程式(答案:C2H4O3)
2、运用有机物的通式计算确定分子式
例8 A是饱和一元醇,B是饱和二元醇,两种醇的分子中所含碳原子数相同,且都小于4。在3.85g由A和B组成的混合物中加入足量的金属钠,标况下放出1.12L氢气。试写出A、B的结构简式并计算出混合液中A的质量。
3、根据燃烧方程式计算确定分子式
例9.10毫升某种气态烃,在50毫升氧气里充分燃烧,得到液态水和体积为35毫升的混和气体(所有气体体积都是在同温同压下测定的),则该气态烃可能是
(A)甲烷 (B)乙烷 (C)丙烷 (D)丙烯
4、根据有机反应关系式确定分子式
例:某3g醛和足量的银氨溶液反应,结果析出43.2gAg,则该醛为
A.甲醛 B.乙醛 C.丙醛 D.丁醛
巩固练习:
1、某混合气体由两种气态烃组成,取2.24L该混合气体完全燃烧后得到4.48LCO2(标况)和3.6g水,则这两种气体可能是
A.CH4 和C3H8 B.CH4 和 C3H4 C. C2H4 和 C3H4 D. C2H2 和 C2H6
( )4、有乙醛蒸汽与乙炔的混合气体a L,当其完全燃烧时,消耗相同状况下氧气的体积为 A. 2a L B. 2.5a L C. 3a L D. 条件不足,无法计算
5、X、Y、Z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下,V L的X、Y、Z的混合气体可与V LH2发生加成反应,则混合气体中X、Y、Z的体积比可能是
A 1:1:1 B 1:2:3 C 1:2:1 D 3:2:1
6、某醛发生银镜反应可得2.16g银。同质量的此醛完全燃烧可生成0.54g水。此醛是
A.乙醛 B.丙醛 C.丁醛 D.丁烯醛
〔 〕4. 只含C、H、O三种元素的有机物完全燃烧时消耗的氧气和生成的CO2的体积比是1:2 ,这类有机物中,
A. 相对分子质量最小的化合物的化学式是CH2O
B. 相对分子质量最小的化合物的化学式是CH2O2
C. 含相同碳原子数的各化合物,其相对分子质量之差是18的整数倍
D. 含相同碳原子数的各化合物,其相对分子质量之差是16的整数倍
〔 〕5.将一定量有机物充分燃烧后的产物通入足量石灰水中完全吸收,经过滤得到沉淀20克,滤液质量比原石灰水减少5.8克.该有机物可能是
(A)乙烯 (B)乙二醇 (C)乙醇 (D)甲酸甲酯
〔 〕6.分别燃烧下列各组物质中的两种有机化合物,所得CO2和H2O的物质的量之比相同的有
(A)乙烯、丁二烯 (B)乙醇、乙醚(C2H5-O-C2H5) (C)苯、苯酚 (D)醋酸、葡萄糖
〔 〕7..一定质量的无水乙醇完全燃烧时放出的热量为Q,它所生成的CO2用过量饱和石灰水完全吸收,可得100克CaCO3沉淀,则完全燃烧1摩尔无水乙醇时放出的热量是
(A)0.5Q (B)Q (C)2Q (D)5Q
〔 〕12.等物质的量的下列各物,在氧气中充分燃烧,消耗氧气最少的是
A. C3H4O2 B. C2H6O2 C. C3H6O2 D.C3H8O3
〔 〕13.一定温度下,w g 下列物质在足量氧气中充分燃烧,产物与过量的过氧化钠完全反应,过氧化钠固体增重w g ,符合此要求的是
① H2 ② CO ③CO和H2 ④HCOOCH3 ⑤HOOC―COOH
A. 全部 B. 仅④⑤ C. 仅①②③ D.除⑤以外
2、有a mL三种气态烃的混合物与足量的氧气混合点燃爆炸后,恢复到原来的状况(常温常压),体积共缩小2a mL,则这三种烃不可能是
A.CH4 C2H4 C3H4 B. C2H6 C3H6 C4H6 C.C2H2 C2H6 C3H8 D.CH4 C2H6 C2H2
3、将10mL某两种气态烃组成的混合物与过量的氧气混合燃烧,将燃烧产物通过浓硫酸后体积减少了15mL,再通过碱石灰后又减少了20mL(体积是在相同状况下测定的),则此混合物可能是
A.CH4 C3H6 B.C2H4 C2H6 C. C2H2 C2H4 D.C2H2 C2H6
4、浓度不等的两种硫酸溶液等质量混合时,质量分数为a%,等体积混合时为b% ;而浓度不等的两种乙醇溶液等质量混合后,质量分数也为a%,等体积混合时则为c%。则
A.a>b>c B.b>a>c C.c>a>b D.无法确定
15、a、b、c三种物质的组成分别符合烷、烯、炔的通式,若在一定条件下,4L a、b、c混合气体,可与4L H2发生加成反应,则混合气体中a、b、c的体积之比可能是
【
】A.1∶1∶1 B.1∶2∶3 C.2∶1∶2 D.3∶2∶1
8、常温下有A和B两种气体混合物,它们只含有碳、氢两种元素,A、B气体以何种比例混合,碳、氢质量比总是小于9:1,大于9:2,若混合气体中碳、氢的质量比为5:1时,则相对分子质量较小的气体在混合气体中所占体积分数为
【 】A、20% B、40% C、60% D、80%
9、将3g 某饱和一元醛和酮的混合物与足量的银氨溶液反应,反应完全后可还原出16.2g银。下列说法正确的是
【 】A.混合物中 一定有甲醛 B.混合物中可能含乙醛
C.醛和酮的质量比为3:5 D.该酮为丙酮
33、在烃分子结构中,若每减少2个氢原子,则相当于碳碳间增加一对共用电子对。试回答下列问题:
(1)分子式为CnH2n+2的烃分子中碳碳间共用电子对的数目为 。
(2)分子式为CnH2n-6的烃分子中碳碳间共用电子对的数目为 。
(3)Cx可看作是烃减氢后的产物,若某物质分子中碳碳间的共用电子对的数目为160。则符合该条件的碳单质的分子式为 ;符合该条件的单烯烃的分子式为 。
(黄岗兵法342)33、400K,1.01×105Pa时,2L烃A的蒸汽能在m L氧气中完全燃烧,反应后体积增至(m+4)L(体积在同前条件下测定)。
(1)烃A的组成上应满足的条件是 。
(2)当m=15时,该烃可能的分子式为 。
(3)若A在常温常压下为气态,m的取值范围是 。
34、现有A、B两份混合气体,A是烯烃R与足量O2的混合气体;B是烯烃R、炔烃Q与足量O2的混合气体,在0℃,1.01×105Pa下,取A、B各2.24L分别引燃。A充分燃烧后气体体积仍为2.24L,B充分燃烧后总体积为2.34L(燃烧后的产物均为气态,其体积已换算成的标准状况)。
求:(1)烯烃R的分子式
(2)炔烃Q的分子式
(3)2.24LB中烯烃R所允许的最大体积
15.现有① 烷烃 ② 烯烃 ③ 炔烃 ④ 环烷烃 任取两种,完全燃烧生成CO2的体积小于H2O的体积
(1)这两种烃中必含有 ,
(2)这两种烃的组合可能是 。
(2001试测)20.(9分)某有机化合物爆炸后的气体中,各组份的体积分数如下:CO241.38%,H2O(气)34.48%,N220.69%,O23.45%。设爆炸时,并没有掺入空气,试推算该化合物的:
(1)最简式 。
(2)分子式(分子中有20个原子) 。
(3)结构式 。
(99试测)22、下面是一个四肽,它可以看作是4个氨基酸缩合掉3个分子水而得。
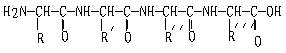
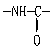 |
式中,R、R′、R″、R′″可能是相同的或不同的烃基,或有取代基的烃基。
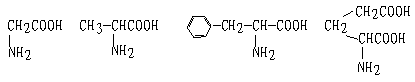 称为肽键。今有一个“多肽”,其分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸:
称为肽键。今有一个“多肽”,其分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸:
甘氨酸 丙氨酸 苯丙氨酸 谷氨酸
(C2H5NO2 ) (C3H7NO2 ) (C9H11NO2 ) (C5H9NO4 )
问:⑴该多肽是 (填数字)肽。
⑵该多肽水解后有 (填数字)个谷氨酸。
⑶该多肽水解后有 (填数字)个苯丙氨酸。
14、常温常压下,某气态烃与O2混合气体共a L,完全燃烧后将生成物通过浓硫酸后,恢复到原状态,体积变为a/2 L,则该烃可能为(写结构简式)
15、由乙炔、苯、乙醛组成的混合物,经测定其中碳的质量分数为0.72 ,则氧的质量分数
为 。
16.某有机物X燃烧只生成CO2和H2O ,请写出你学过的有机物的结构简式。这些化合物燃烧后产生的CO2和H2O的体积比符合如下比值(各写两种):
(1)V(CO2):V(H2O)=2:1的有 (2)V(CO2):V(H2O)=1:2的有
(3)V(CO2):V(H2O)=1:1的有 (4)V(CO2):V(H2O)=2:3的有
(5)V(CO2):V(H2O)=3:4的有
(96试测)吗啡和海洛因都是严格查禁的毒品。吗啡分子含C 71.58%、H 6.67%、 N 4.91%、其余为O。已知其分子量不超过300。
试求:
(1)吗啡的分子量 (2)吗啡的分子式 。
已知海洛因是吗啡的二乙酸酯。试求:
(1)海洛因的分子量 ;(2)海洛因的分子式 。
(MCE97)34A、B都是芳香族化合物,1 mol A水解得到1 mol B和1 mol醋酸.A、B的分子量都不超过200,完全燃烧都只生成CO2和H2O.且B分子中碳和氢元素总的质量百分含量为65.2%(即质量分数为0.652).A溶液具有酸性,不能使FeCl3溶液显色.
(1)A、B分子量之差为_______________.
(2)1个B分子中应该有_______________个氧原子.
(3)A的分子式是_______________.
(4)B可能的三种结构简式是:_______________、_______________、
_______________.
17.在通常条件下,只含C、H、O三种元素的某些有机物在足量的O2中充分燃烧,恢复到室温后,其燃烧所消耗的氧气的物质的量和燃烧所产生气体的物质的量相等
(1)写出符合上述条件的有机物的通式
(2)在符合条件的有机物中,若其分子中含一个碳原子,则该物质的结构简
式为 ,若分子中含两个碳原子,写出对应的两种互为同分异构
体的物质的结构简式
(3)若符合题设条件的物质为酚类化合物,已知该物质的一卤代物(卤原子直接取代苯环上的氢原子)只有一种,则该酚类化合物的结构简式
为 。
18.今有A、B两种有机物,A是苯的同系物,B是烃的含氧衍生物。各取1molA、B完全燃烧。生成的CO2分别为7mol和3mol 。A、B不论以何种比例相混合,只要混合物总物质的量一定或总质量一定,完全燃烧时生成的水的量也一定。
(1)A的结构简式是
(2)B分子中一个碳原子最多与一个氧原子成键,则B与足量的硝酸、浓硫酸的混合酸完全
反应的化学方程式是
19.某有机物完全燃烧时只生成CO2和H2O ,已知1 mol 该有机物含碳原子n mol ,在恰好完全燃烧时耗氧气1.5 n mol 。请回答有关问题:
(1)该有机物的化学式可能为:
① ② ③ 。(用 n 表示化学式内碳原子数,你认为有几种化学式就填几种)
(2)若4.4 g 该有机物(R)与足量的钠反应可收集到 H2 560mL(标况),则该有
机物(R)的分子式为: ,
(3))若有机物(R)能催化氧化生成醛,则该有机物(R)的结构可能有 种。
35、某气态烷烃和一气态单烯烃组成的混合气体,在同温同压下对氢气的相对密度为13。标况下,此混合气体12L,通入足量溴水中,溴水增重70g。求(1)混合气体中的气态烷烃是什么?(2)混合气体中两气体的物质的量之比是多少?(3)混合气体中单烯烃的分子式是什么?写出其结构简式。
36、标准状况下 1.68L无色可燃气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水,得到的白色沉淀质量为15.0 g;若用足量的碱石灰吸收燃烧产物,增重9.3 g。
(1)计算燃烧产物中水的质量。
(2)若原气体是单一气体,通过计算推断它的分子式。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组)。
12.某有机物A是由C、H、O三种元素组成。完全燃烧1mol A,需要4mol O2,该有机物不跟金属钠反应放出H2,但可以被氧化剂氧化成既能跟Na2CO3反应又能跟NaOH反应的化合物B,0.37g B跟0.2mol/L的NaOH溶液25.0mL恰好完全中和。试确定A、B的结构简式。
(黄岗兵法375)
22.某有机物X由C、H、O三种元素组成。X的沸点为471K。已知①在一定温度、压强下,在密闭容器中把4.2LX的蒸汽和18.9L氧气(过量)混合后点燃,充分反应后将温度压强恢复到原来状态,得到混合气体A 29.4L(另知该状况下1mol气体的体积为42L) ;②当A处于标准状况时,气体体积变为8.96L,其密度为1.696g/L。试推断
(1)A中各组分的物质的量
(2)X的化学式
23、在压强为1.01×105Pa、127℃时,由两种常见有机物组成的混合气体20mL跟相同状态下的25mLO2混合,引燃恰好使之完全燃烧,所生成的CO2和H2O(气)经测定其平均相对分子质量为28.4,当恢复到反应前状况时,混合气体密度比反应前减少1/10 。这种混合气体由哪两种物质组成?各组分的体积百分比为多少?(点拨154)
22、0.2mol有机物和0.4molO2在密闭容器中燃烧后的产物为CO2、CO和H2O(g),产物经过浓H2SO4后,质量增加10.8g;再通过灼热的CuO充分反应后,质量减轻3.2g;最后气体再通过碱石灰吸收,质量增加17.6g。
(1)试推断该有机物的分子式和相对分子质量
()若0.2mol该有机物恰好与9.2g金属钠完全反应,试确定该有机物的结构简式并命名
11、完全燃烧一定质量的乙烯与某烃的混合气体后测得其生成物中气体的质量是反应前混合烃质量的2.86倍。试通过计算,确定该气态烃的分子式及它在该混合气体中所占的体积分数(气体体积和质量均在常温下测定)
10、有标况下的乙烷与某烃的混合气体共1.344L,将该混合气体与足量的氧气点火爆炸后,把所得的气体通入240mL0.500mol/LnaOH溶液中,使逸出气体不含CO2。把吸收CO2的溶液在减压低温的条件下蒸干得固体7.60g(不含结晶水)。求原混合气体的成分及各组分的体积。
(反馈精编66)
12、A、B、C三种有机物组成混合物X。A、B、C的相对分子质量均为90,且互为同分异构体。① 把1.8gX完全燃烧后得到2.64g CO2和1.08g H2O。A和B具有相同的物质的量。
② 4.5g X中,A和B均能与钠反应,生成896mLH2(标况),C不反应
③ 4.5gX中A和B均能与Na2CO3反应生成448mLCO2(标况),C不与Na2CO3反应
④ 2molA在催化剂条件下能酯化生成1mol六原子的环,2molB亦能酯化形成1mol八原子环。⑤ C不能发生上述反应,但能起银镜反应,且有醚的结构。
(1)推导A、B、C的分子式。(2)推测A、B、C的结构简式及在X中A、B、C物质的量。
(黄岗兵法390)
12、有一混合气体由一种气态烯烃A和一种气态烷烃B组成,它对H2的相对密度为12 。把1体积此混合气体和4体积氧气混合,放在密闭的容器中用电火花引燃,使两种烃都充分氧化,如果反应前后的温度皆为150℃,测得容器内压强由反应前的1×105Pa增加至燃烧后的1.04×105Pa。问A和B各是什么烃?它们的体积各是多少?(反馈精编65)
12、某些有机物在供氧不足时燃烧,常会产生CO,它是常见的大气污染物之一。将某液态烃的含氧衍生物CxHyOz0.400mol在一定量的氧气中燃烧,高有机物反应完后,气体体积减少了8.96L.再将剩余气体通过足量的Na2O2固体,并在电火花的连续作用下充分反应后,体积又减少了31.36L,最终所得气体只有氧气,而固体质量增加了56.0g(气体体积都在标况下测定)。
(1)写出该有机物不完全燃烧的化学方程式(CO的系数用m表示)
(2)求燃烧后产物中CO和CO2的物质的量之比
(3)求有机物可能的分子式
40、常见有机物A与足量NaOH溶液在常温下反应,得到盐B 、水和剩余NaOH的混合溶液。将混合液蒸干,取出固体加强热后,除得到盐D与剩余NaOH的固体混合物外,还收集到一种无色液体C。盐D与足量盐酸反应能产生一种无色无味的能使澄清石灰水变浑浊的气体。又知:①无色液体C的每个分子中含有42个电子,C在氧气中充分燃烧的产物为CO2和H2O,且CO2和H2O的质量之比为44:9; ②盐B的分子量不大于200,其中钠元素的质量分数为16.0%; ③有机物A在氧气中充分燃烧生成CO2和H2O,且CO2和H2O的物质的量之比为7:3;试通过必要的计算和推理回答下列问题
(1)C物质中是否含有氧元素?
(2)盐B的相对分子质量是
(3)求有机物A 的结构简式(写出简答过程)
(98高三调查测试)
高二有机复习(3)
〔 〕1.为了减少大气污染,许多城市推广汽车使用清洁燃料。目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG)。这两类燃料的主要成份都是
A.碳水化合物 B.碳氢化合物 C.氢气 D.醇类
〔 〕2.为了保护臭氧层,可采取的有效措施是
A.减少二氧化硫的排放量 B.减少含铅废气的排放量
C.减少氟氯代烃的排放量 D.减少二氧化碳的排放量
〔 〕3.10毫升某种气态烃,在50毫升氧气里充分燃烧,得到液态水和体积为35毫升的混和气体(所有气体体积都是在同温同压下测定的),则该气态烃可能是
(A)甲烷 (B)乙烷 (C)丙烷 (D)丙烯
〔 〕4. 只含C、H、O三种元素的有机物完全燃烧时消耗的氧气和生成的CO2的体积比是1:2 ,这类有机物中,
A. 相对分子质量最小的化合物的化学式是CH2O
B. 相对分子质量最小的化合物的化学式是CH2O2
C. 含相同碳原子数的各化合物,其相对分子质量之差是18的整数倍
D. 含相同碳原子数的各化合物,其相对分子质量之差是16的整数倍
〔 〕5.将一定量有机物充分燃烧后的产物通入足量石灰水中完全吸收,经过滤得到沉淀20克,滤液质量比原石灰水减少5.8克.该有机物可能是( ).
(A)乙烯 (B)乙二醇 (C)乙醇 (D)甲酸甲酯
〔 〕6.分别燃烧下列各组物质中的两种有机化合物,所得CO2和H2O的物质的量之比相同的有
(A)乙烯、丁二烯 (B)乙醇、乙醚(C2H5-O-C2H5)
(C)苯、苯酚 (D)醋酸、葡萄糖
〔 〕7..一定质量的无水乙醇完全燃烧时放出的热量为Q,它所生成的CO2用过量饱和石灰水完全吸收,可得100克CaCO3沉淀,则完全燃烧1摩尔无水乙醇时放出的热量是
(A)0.5Q (B)Q (C)2Q (D)5Q
8.在下列烃中
〔 〕①等质量完全燃烧耗O2量最大的是;
〔 〕②等物质的量完全燃烧耗O2量最大的是
A. C3H8 B.C4H6 C.C2H2 D.C2H6
9.对于下列各组内的两种有机物,
〔 〕①等质量完全燃烧耗O2量相等的是;
〔 〕②等物质的量完全燃烧耗O2量相等的是
A.甲醛和乙酸 B.甲烷和乙酸 C.乙烯和丙烯 D.乙炔和乙醛
10.下列各组混合物,无论两组分以何种比例混合,只要混合物的总质量一定时
〔 〕完全燃烧时耗氧量不变的是
〔 〕生成水的量一定的是
A. CH3COOH和HCHO B.C2H6和C3H6
C. C7H8和C3H6 D.C4H10和C4H8
〔 〕11.下列各组混合物,无论两组分以何种比例混合,只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗氧气的质量均不变的是
A.C3H6和C4H6O2 B. C2H4和C2H6O
C.C2H2和C6H6 D.CH4O和C3H4O5
〔 〕12.一定温度下,w g 下列物质在足量氧气中充分燃烧,产物与过量的过氧化钠完全反应,过氧化钠固体增重w g ,符合此要求的是
② H2 ② CO ③CO和H2 ④HCOOCH3 ⑤HOOC―COOH
A. 全部 B. 仅④⑤ C. 仅①②③ D.除⑤以外
〔 〕13.等物质的量的下列各物,在氧气中充分燃烧,消耗氧气最少的是
A. C3H4O2 B. C2H6O2 C. C3H6O2 D.C3H8O3
15.现有① 烷烃 ② 烯烃 ③ 炔烃 ④ 环烷烃 任取两种,完全燃烧生成CO2的体积小于H2O的体积
(1)这两种烃中必含有 ,(2)这两种烃的组合可能是
16.某有机物X燃烧只生成CO2和H2O ,请写出你学过的有机物的结构简式。这些化合物燃烧后产生的CO2和H2O的体积比符合如下比值(各写两种):
(1)V(CO2):V(H2O)=2:1的有 (2)V(CO2):V(H2O)=1:2的有
(3)V(CO2):V(H2O)=1:1的有 (4)V(CO2):V(H2O)=2:3的有
(5)V(CO2):V(H2O)=3:4的有
17.在通常条件下,只含C、H、O三种元素的某些有机物在足量的O2中充分燃烧,恢复到室温后,其燃烧所消耗的氧气的物质的量和燃烧所产生气体的物质的量相等
(1)写出符合上述条件的有机物的通式 Cn(H2O)m
(2)在符合条件的有机物中,若其分子中含一个碳原子,则该物质的结构简
式为 CH2O,HCHO ,若分子中含两个碳原子,写出对应的两种互为同分异构体的物质的结构简式 CH3COOH HCOOCH3 HO-CH2CHO
(3)若符合题设条件的物质为酚类化合物,已知该物质的一卤代物(卤原子直接取代苯环上的氢原子)只有一种,则该酚类化合物的结构简式为 1,3,5-苯三酚 。
18.今有A、B两种有机物,A是苯的同系物,B是烃的含氧衍生物。各取1molA、B完全燃烧。生成的CO2分别为7mol和3mol 。A、B不论以何种比例相混合,只要混合物总物质的量一定或总质量一定,完全燃烧时生成的水的量也一定。
(1)A的结构简式是
(2)B分子中一个碳原子最多与一个氧原子成键,则B与足量的硝酸、浓硫酸的混合酸完全
反应的化学方程式是
(C7H8、 C3H8O3)
19.某有机物完全燃烧时只生成CO2和H2O ,已知1 mol 该有机物含碳原子n mol ,在恰好完全燃烧时耗氧气1.5 n mol 。请回答有关问题:
(1)该有机物的化学式可能为:
① ② ③ 。(用 n 表示化学式内碳原子数,你认为有几种化学式就填几种)
(2)若4.4 g 该有机物(R)与足量的钠反应可收集到 H2 560mL(标况),则该有机物(R)的分子式为:
(3))若有机物(R)能催化氧化生成醛,则该有机物(R)的结构可能有 种。
20.有机化合物A、B分子式不同,它们只可能含碳、氢、氧元素中的两种或三种.如果将A、B不论以何种比例混和,只要其物质的量之和不变,完全燃烧时所消耗的氧气和生成的水的物质的量也不变.那么,A、B组成必须满足的条件是 .若A是甲烷,则符合上述条件的化合物B中,分子量最小的是(写出分子式) ,并写出分子量最小的含有甲基(-CH3)的B的2种同分异构体结构简式 。
21.某有机物X由C、H、O三种元素组成。X的沸点为471K。已知①在一定温度、压强下,在密闭容器中把4.2LX的蒸汽和18.9L氧气(过量)混合后点燃,充分反应后将温度压强恢复到原来状态,得到混合气体A29.4L(另知该状况下1mol气体的体积为42L) ;②当A处于标准状况时,气体体积变为8.96L,其密度为1.696g/L。试推断
(1)A中各组分的物质的量
(2)X的化学式
22.常温下,一种烷烃A和一种单烯烃B组成混和气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多.
(1)将1升该混和气体充分燃烧,在同温同压下得到2.5升CO2气体.试推断原混和气体中A和B所有可能的组合及其体积比,并将结果填入下表:
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比VA:VB |
(2)120℃时取1升该混和气体与9升氧气混和,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%.试通过计算确定A和B的分子式.
23.石油及其分馏产物在供氧不足时燃烧,常常产生CO,这也是常见的大气污染物之一。将某气态烃在5倍体积的纯氧中燃烧,产物通过足量Na2O2并在电火花连续作用下充分反应,生成的气体体积缩小到燃烧后产物体积的3/8(气体体积都在100℃以上,1.01×105Pa时测定)
(1)试写出通式为CXHY的某烃在供氧不足时燃烧的化学方程式 (CO2的系数设定为m)
(2)当m=2时,求该烃的分子式。
(3)若1摩某气态烃在供氧不足时燃烧,产物在足量Na2O2的电火花连续作用下产生3摩氧气,且固体Na2O2增重范围为90克≤△W≤118克,求烃可能的分子式和燃烧产物CO与CO2的物质的量之比,将结果填入下表
| 烃的分子式 | nco/nCO2 |