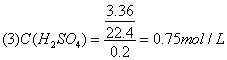高二化学下学期期中测试题
| 题 号 | 一 | 二 | 三 | 四 | 总 分 |
| 得 分 |
(考试时间60分钟)
一、选择题(每小题只有一个答案符合题意,每小题2分,共16分)
“非典不可怕,关键在预防”,过氧乙酸是抗“非典”中一种重要消毒剂,其分子式:C2H4O3 。其配制方法是:240kg冰乙酸与442kg双氧水混合,外加浓硫酸至0.3%,低温混合8~15h,即制得过氧乙酸。
此据回答下列1——3题
1.有关过氧乙酸的叙述正确的是 ( )
A.过氧乙酸的化学式为:CH3-O-COOH
B.可用过氧乙酸擦拭金属器皿及大理石地板以消毒
C.过氧乙酸属非电解质
D.属于烃的衍生物
2.配制过氧乙酸原料中,冰醋酸与过氧化氢的物质的量之比是 ( )
A.6∶13 B.13∶5 C. 4∶13 D. 4∶3
3.2003-5-12号河南电视台报道:某过氧乙酸消毒剂制备厂,装运过氧化氢的卡车突然发生爆炸,造成5人受伤。下面是各“行家”的分析,你认为正确的是 ( )
A.过氧化氢振动,产生了大量可燃性气体,遇明火发生爆炸。
B.过氧化氢分解,产生高浓度氧气,遇某些易燃物在明火作用下而发生爆炸
C.可能是某工人在附近吸烟引起过氧化氢爆炸。
D.可能是工厂的冰醋酸蒸气与过氧化氢蒸气相遇发生爆炸。
第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类 1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳五个CH4分子或1个游离H2O分子。
根据上述信息,完成第4、5题.
4.下列关于天然气水合物中两种分子极性的描述正确的是于 ( )
A.两种都是极性分子 B.两种都是非极性分子
C.CH4是极性分子,H2O是非极性分子 D.H2O是极性分子,CH4是非极性分子
5.若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为 ( )
A.CH4·14H2O B.CH4·8H2O C.CH4·(23/3)H2O D.CH4·6H2O
 6.已知C5H11OH有8种同分异构体,则C6H12O2属于羧酸结构有
6.已知C5H11OH有8种同分异构体,则C6H12O2属于羧酸结构有
A.4种 B.8种
C.16种 D.6种
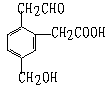
7.某有机物的结构式为它在一定条件下能发生的反应有 ( )
①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去
A.②③④ B.①③⑤⑥ C.①③④⑤ D.②③④⑤⑥C
8.常温常压下,某气态烃和氧气的混合气体nL,完全燃烧后,通过浓硫酸恢复到原来的温度和压强,气体体积为原来的一半,假设烃在燃烧后无剩余,则该烃的组成可能是下列组合中的 ( )
①甲烷 ②乙烯 ③乙炔 ④乙烷
⑤丙烯 ⑥丙炔 ⑦丙烷 ⑧丁炔
A.①②③④ B.⑤⑥⑦⑧ C.①③⑤⑦ D.①②④⑦
二、选择题(每小题3分,共30分,每小题有1-2个答案符合题意)
9.下列说法中正确的是 ( )
A.能发生银镜反应的物质不一定是醛
B.酯在碱性条件下的水解都是皂化反应
C.参与酯化反应的物质一定有两种
D.能使淀粉溶液显蓝色的物质一定是碘单质
10.化合物丙由如下反应得到 ( )
![]()
![]() C4H10O
C4H8
C4H8Br2
C4H10O
C4H8
C4H8Br2
C4H8Br2的结构简式不可能为 b
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
11.分子式为C5H12O2的二元醇有多种同分异构体,其中能够氧化成主链上碳原子数为3的二元醛有x种,能氧化成主链上碳原子数为4的二元醛共有y种,则x、y的值是
( )
A.x = 1,y = 2 B.x = 1,y = 7
C.x = 1,y = 1 D.x = 2,y = 1
12.将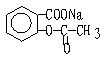 转变为
转变为![]() 的方法是
( )
的方法是
( )
A.与足量的氢氧化钠溶液共热后,再通入CO2
B.溶液加热,并通入足量的SO2
C.与稀硫酸共热后,加入足量的NaOH
D.与稀硫酸共热后,加入足量的NaHCO3
13.有机物CH2=CH-CH2-OOC-CH3可能具有的性质是AB ( )
A.能使溴水褪色 B.能发生加聚反应
C.能发生银镜反应 D.能溶于水
14.天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素 P的叙述错误的是 ( )
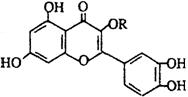 A.可以和溴水反应
A.可以和溴水反应
B.可用有机溶剂萃取
C.分子中有三个苯环
D.1mol维生素P可以和4molNaOH反应
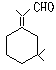
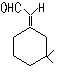
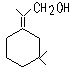
15.人们使用四百万象鼻虫和它们的215磅糞物,历
经30多年时间弄清了棉子象鼻虫的四种信息素的组成,它们的结构可表示如下(括
号内表示④的结构简式)
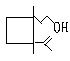 (
(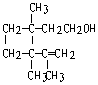 )
)
① ② ③ ④
以上四种信息素中互为同分异构体的是 C ( )
A.①和② B.①和③ C.③和④ D.②和④
16.氢气是工业上用以合成氨的原料之一,有一种来源是取自石油气,例如丙烷。有人设计以下反应途径,假设反应都能进行,你认为最合理的是 C
A.C3H8 ![]() C +
H2
C +
H2
B.C3H8 ![]() C3H6
+ H2
C3H6
+ H2
C.C3H8 + H2O![]() CO +
H2
CO +
H2
D.C3H8 + O2 →CO2
+ H2O H2O![]() H2↑ + O2↑
H2↑ + O2↑
17.某有机物分子式为C3H6O2,水解后生成一元酸M和一元醇N,且M和N的相对分子质量相等,下列说法不正确的是 BD ( )
A.M具有还原性 B.M中含碳质量分数为40%
C.N分子中有乙基 D.N氧化后得一元酸,其酸性比M强
18.C8H18经多步裂化,最后完全转化为C4H8、C3H6、C2H4、C2H6、CH4五种气体的混
合物。该混合物的平均相对分子质量可能是bc ( )
A.28 B.30 C.38 D.40
三、填空题
19.(6分)某芳香化合物A的分子式为C7H6O2,溶于NaHCO3,将此溶液加热,能用石蕊试纸检验出有酸性气体产生。
(1)写出化合物 A的结构简式。
______________________________________________________________
(2)依题意写出化学反应方程式。
______________________________________________________________
(3)A有几个属于芳香族化合物的同分异构体,写出它们的结构简式。
______________________________________________________________________
20.(8分)某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是a g·cm-3。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的分子量,拟定的实验步骤如下
①准确量取该卤代烷b mL,放入锥形瓶中。
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反反应。③反应完成后,冷却溶液,加稀NaOH溶液,塞上带有长玻璃的塞子,加热,发生反应。④过滤、洗涤、干燥后称重,得到固体c g。
回答问题
⑴装置中长玻璃管的作用是________________。
⑵步骤④中,洗涤的目的是为了除去沉淀上吸附的________离子。
⑶该卤代烷中所含卤素的名称是____________,判断的依据是_____________。
⑷该卤代烷的分子量是_____________(列出算式)。
⑸如果在步聚③中,加HNO3的量不足,没有将溶液酸化,则步骤④中测得的c值(填下列选项代码)_______。
A.偏大 B.偏小 C.不变 D.大小不定
21.(8分)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基,例如
![]()
![]()
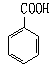
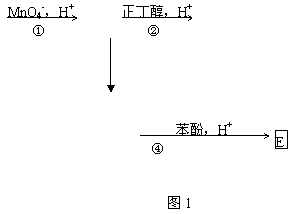
化合物A-E的转化关系如图1所示,已知A是芳香族化合物,只能生成3种一溴化合物,B有酸性,C是常用增塑剂,D是有机合成的重要中间体和常用化学试剂
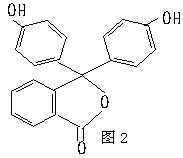
(D也可由其他原液催化氧化得到),E是一种常用的指示剂酚酞,结构如图2。
写出A.B.C.D的结构简式
⑴A_____________________ ⑵B_____________________
⑶C_____________________ ⑷D_____________________
|
 A
B
C
A
B
C
C8H10 C16H22O4
③ 250℃
D
C8H4O3
22.烯烃A在一定条件下可以按下面的框图进行反应
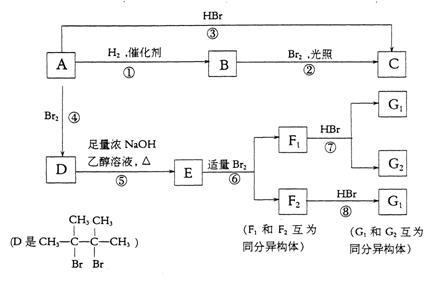
已知![]() ,
,
请填空
(1)A的结构简式是________________________________。
(2)框图中属于取代反应的是(填数字代号)________________________。
(3)框图中①、③、⑥属于__________________反应。
(4)G1的结构简式是__________________________。
23.(6分)如图所示,某容器分隔成A.B两部分,A部分容积固定不变,充有2molSO2和1mol02;
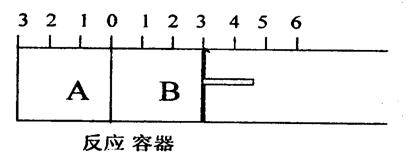
B部分有可移动的活塞,充有2molS03和lmolN2,活塞恰好处于“3”处,在相同温度下发生可逆反应:2SO2(g)+02(g)![]() 2S03(g),根据下列要求回答:
2S03(g),根据下列要求回答:
(1)若反应开始时,就将活塞固定于“3”处不动,A.B中反应均达到平衡时,A.B中压强关系是p(A) _________p(B),A.B中S02的浓度关系是C(A) _________C(B) (填“>”、“<”或“=”)。
(2)若反应达到平衡时,B的活塞在“5”处,B中S03为bmol,A中SO3为amol,则a_________b(填:“>”、“<”或“=”)
四、计算题(12分)
24.(6分)标准状况下1.68 L无色可燃气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水,得到的白色沉淀质量为15.0 g;若用足量碱石灰吸收燃烧产物,增重9.3 g。
(l)计算燃烧产物中水的质量。
(2)若原气体是单一气体,通过计算推断它的分子式。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组)。
25.(6分)在铜片、锌片和200mL稀硫酸组成的原电池中,若铜片上放出3.36L(标准状况)气体时,H2S04恰好作用完毕。试计算:
(1)产生这些气体所消耗锌的质量;
(2)产生这些气体时,通过导线的电子的物质的量;
(3)原200mL稀硫酸的物质的量浓度。
参考答案
一、选择题(每小题只有一个答案符合题意,每小题2分,共16分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8B |
| D | C | B | D | B | B | C | D |
二、选择题(每小题3分,共30分,每小题有1-2个答案符合题意)
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| AD | B | AD | AD | AB | C | C | C | BD | BC |
![]()
19(1) (2分)
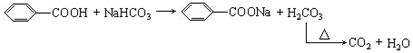
(2)
(2分)
(3)有4个同分异构体
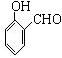 、
、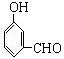 、
、![]() 、
、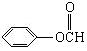 (各1分)
(各1分)
20、⑴防止卤代烷挥发(或答 冷疑)(1分)
⑵Ag+,Na+和![]() (说明答出Ag+就给2分;只答Na+和
(说明答出Ag+就给2分;只答Na+和![]() 给1分)
给1分)
⑶氯(1分);得到的卤化银沉淀是白色的(1分)
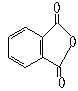 ⑷
⑷![]() (2分) ⑸A(1分)
(2分) ⑸A(1分)
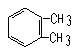
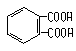
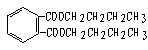
21、A B C D
22.(8分)
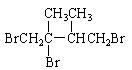 (1)
(1)![]() (2分)(2)②
(2分)
(2分)(2)②
(2分)
(3)加成 (2分)(4) (2分
23、(1)< = (2)>(每空2分,计6分)
24、(1)m(CO2)=15.0g×44 g·mol-1/100 g·mol-1=6.6g
m(CO2+H2O)=9.3g
m(H2O)=9.3g-6.6g=2.7g
(2)n(CO2)=6.6g/44 g·mol-1=0.15mol
n(H2O)=2.7g/18 g·mol-1=0.15mol
分子中C:H=1:2
n(无色可燃气体)=1.68L/22.4 L·mol-1=0.075mol
分子中C原子数=0.15mol/0.075mol=2,分子中氢原子数=2×2=4
所以该气体的分子式是C2H4
(3)C4H6和H2(或C3H8和CO,C3H6和CH2O等)
![]()
![]()