●高二化学素能培养2
巩固类
一、选择题
1.通常用于衡量一个国家石油化工发展水平的标志是( )
A.石油产量 B.乙烯产量
C.天然气产量 D.汽油产量
解析:乙烯是石油化学工业最重要的基础原料,它主要用于制造塑料、合成纤维、有机溶剂等。乙烯工业的发展,带动了其他以石油为原料的石油化工的发展。因此,一个国家乙烯工业的发展水平,已成为衡量该国家石油化学工业水平的重要标志之一。
答案:B
2.除去乙烷气中混有的乙烯,最好的方法是( )
A.加入氢气与乙烯反应 B.点燃
C.通入适量的溴水中 D.通过KMnO4溶液
解析:最好通过溴水,使乙烯与溴发生加成反应,且没有副产物生成。
答案:C
3.下列反应属于加成反应的是( )
A.C3H8+Cl2![]() C3H7Cl+HCl
C3H7Cl+HCl
B.2FeCl2+Cl2====2FeCl3
C.CH2==CH2+H2O![]() CH3CH2OH
CH3CH2OH
D.CH3CH2OH![]() CH2==CH2↑+H2O
CH2==CH2↑+H2O
解析:由加成反应的定义可知,C项为加成反应。
答案:C
4.关于实验室制乙烯的实验,下列说法正确的是( )
A.反应物是乙醇和过量的3 mol/L硫酸的混合液。
B.温度计插入反应溶液的液面下,控制温度140℃
C.反应容器中应加入碎瓷片
D.反应完毕灭火后再从水中取出导管
解析:3 mol/L H2SO4为稀H2SO4;实验室制乙烯应控制温度为170℃;反应完毕应先从水中取导气管,再熄灭酒精灯。
答案:C
5.下列液体分别和溴水混合并振荡,静置后分为两层,水层和油层均为无色的是( )
A.己烷 B.CCl4
C.NaOH溶液 D.己烯
解析:己烯与溴加成,使溴褪色,且溶液分为上下两层
答案:D
6.下列物质不能使溴水褪色的是( )
A.C2H4 B.SO2
C.CH2==CHCH==CH2 D.CH3—CH2—CH3
解析:只要有机物分子中含C==C双键,就可以与溴发生加成反应,使溴水褪色;SO2具有还原性,能被溴氧化,使溴水褪色。
答案:D
7.某气态烃1体积只能与1体积氯气发生加成反应,生成氯代烷,此氯代烷1 mol可与 4 mol氯气发生完全的取代反应,则该烃的结构简式为( )
A. CH2==CH2
B. CH3CH==CH2
C. CH3CH3
D. CH2CHCH==CH2
解析:由题意可知,氯化烷分子中含4个氢原子。不饱和烃也含4个H,且含一个C==C双键。
答案:A
8.下列关于乙烯的说法,错误的是( )
A.乙烯的化学性质比乙烷活泼
B.可作香蕉等水果的催熟剂
C.燃烧时火焰明亮,同时发生黑烟
D.收集乙烯可用排空气法
解析:乙烯的密度与空气的接近,收集乙烯不可用排空气法。
答案:D
9.实验测得乙烯和氧气组成的混合气体的密度是相同条件下H2密度的14.5倍,可知其中乙烯的质量分数为( )
A.25% B.27.6%
C.72.4% D.75%
解析:二者的平均相对分子质量![]() =14.5×2=29,由十字交叉法可求得乙烯和氧气的物质的量比为3︰1,则乙烯质量分数比75%稍小些。
=14.5×2=29,由十字交叉法可求得乙烯和氧气的物质的量比为3︰1,则乙烯质量分数比75%稍小些。
答案:C
10.以乙烯和丙烯混合物为单体,发生加聚反应,不可能得到的是( )
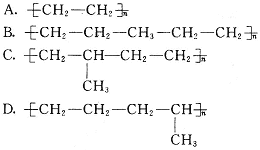
解析:若在乙烯单体间聚合,可得![]() ,若在乙烯和丙烯之间聚合,可得
,若在乙烯和丙烯之间聚合,可得
或
答案:B
二、填空题
11.写出下列反应的化学方程式
(1)实验室制乙烯_____________。
(2)丙烯通入溴水_____________。
(3)丙烯聚合_____________。
答案:(1)CH3CH2OH![]() CH2==CH2↑+H2O
CH2==CH2↑+H2O
(2)CH3CH==CH2+Br2—→CH3CHBrCH2Br
(3)nCH3CH===CH2![]()
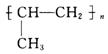 〖JG()
〖JG()
12.实验室制取乙烯的实验中:
(1)浓H2SO4的作用是_____________。
(2)浓H2SO4与酒精混合的先后顺序是__________________________。
(3)迅速升温至170 ℃的原因是__________________________。
(4)有效控制反应混合温度的方法是__________________________。
(5)反应后阶段的混合液体常变黑,并有刺激性气体生成,除去气体的方法是__________________________。
(6)在实验之前,首先应________,实验结束时,应先__________________________。
答案:(1)催化和脱水
(2)先加乙醇,再慢慢滴加浓H2SO4,并不断用玻璃棒搅拌
(3)防止副反应的发生
(4)使用温度计并插入反应混合液中
(5)使气体通过盛有NaOH溶液的洗气瓶
(6)检验装置的气密性;从水中取出导管再停止加热
13.相对分子质量为56,且含一个甲基支链的烃,该烃能使酸性KMnO4溶液或溴水褪色,写出它的结构简式________。
解析:![]() =4,
=4,
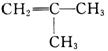 所以,烃的分子式为C4H8,符合条件的烃的结构简式为
所以,烃的分子式为C4H8,符合条件的烃的结构简式为
答案: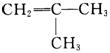
14.某烃A 0.2 mol在O2中充分燃烧时,生成化合物B、C各1.2 mol,试回答:
(1)烃A的分子式________,B、C的分子式分别是________、________。
(2)若取一定量的烃A燃烧后生成B、C各3 mol,则有________ g烃A参加了反应,燃烧时消耗标准状况下O2________L。
解析:0.2 mol A充分燃烧生成CO2 1.2 mol,H2O 1.2 mol,所以,A的分子式为C6H12
C6H12 + 9O2
![]() 6CO2 + 6H2O
6CO2 + 6H2O
1 9 6
0.5 mol 4.5 mol 3 mol
m(A)=0.5 mol×84 g·mol-1=42 g
V(O2)=4.5 mol×22.4 L·mol-1=100.8 L
答案:(1)C6H12,CO2,H2O
(2)42 100.8
三、计算题
15.当乙烯通过装有溴的试剂瓶时,试剂瓶的质量增加了16 g,有多少升乙烯(标况)被吸收?生成了多少克的二溴乙烷?
解析:m(C2H4)=16 g
n(C2H4)=![]() =0.57 mol
=0.57 mol
V(C2H4)=0.57 mol×22.4 L·mol-1=12.8 L
m(C2H4Br2)=0.57 mol×188 g·mol-1=107.2 g
答案:12.8 L,107.2 g