●高二化学素能培养
提升类
一、选择题
1.有关聚乙烯的说法正确的是( )
A.聚乙烯是通过加聚反应生成
B.聚乙烯具有固定的元素组成,因而有固定的熔沸点
C.聚乙烯塑料袋因有毒,故不能装食品
D.聚乙烯性质稳定,故不易造成污染
解析:聚乙烯属于高分子化合物,由于n值的不同,一般高分子化合物是混合物。虽然聚乙烯无毒,由于不易被微生物降解,大量使用也会造成污染。
答案:A
2.由乙烯推测丙烯的结构或性质正确的是( )
A.分子中三个碳原子在同一直线上
B.分子中所有原子都在同一平面上
C.与HCl加成只生成一种产物
D.能发生加聚反应
解析:丙烯可看作是乙烯分子中的一个氢原子被甲基取代的产物,因此,丙烯分子不是平面结构,三个碳原子不位于同一直线上。由于丙烯为非对称烯烃,与HCl加成的产物有两种可能。
答案:D
3.把m mol C2H4和n mol H2混合于密闭容器中,在适当的条件下生成了p mol C2H6,若将所得的混合气体完全燃烧生成CO2和H2O,则需O2( )
A.3.5 p mol
B.(3m+![]() )mol
)mol
C.(3m+n) mol
D.(3
m+![]() -3p)mol
-3p)mol
解析:混合物共含2m mol碳原子,(4m+2n) mol氢原子,则完全燃烧生成CO2和H2O,共需O2:
(2 m+![]() ) mol=(3 m+
) mol=(3 m+![]() ) mol
) mol
答案:B
 |
4.烷烃 是烯烃R和氢气发生加成反应后的产物,
则R可能的结构简式有( )
A.4种 B.5种
C.6种 D.7种
解析:由题意可知,相邻两个碳原子有氢原子,则加成之前可能存在碳碳双键。所以,R可能的结构有6种。
答案:C
 5.已知乙烯分子是平面结构,因此,1,2—二氯乙烯可以形成
和
5.已知乙烯分子是平面结构,因此,1,2—二氯乙烯可以形成
和
 |
两种不同的空间异构体。下列各物质中,能形成类似上述两种空间异构体
的是( )
A.1—丁烯 B.丙烯
C.2—甲基—2—丁烯 D.2—氯—2—丁烯
解析:由题意可知,只要C==C双键的碳原子上连接两个不同的取代基,就存在空间异构体。显然,只有2—氯—2—丁烯存在空间异构体。
答案:D
6.在120 ℃时,装有等物质的量CO和某烯烃的密闭容器中,充入足量O2点燃,充分燃烧,当恢复到原条件时,测知容器内反应前后压强相等,此烯烃是( )
A.乙烯 B.丙烯
C.丁烯 D.戊烯
解析:设烯烃的分子式为CnH2n
CO+CnH2n+![]() O2—→(n+1)CO2+nH2O
O2—→(n+1)CO2+nH2O
由题意可得:1+1+![]() =n+1+n n=3
=n+1+n n=3
答案:B
7.在相同状况下,下列混合气体的含碳量有可能比乙烯的含碳量低的是( )
A.C2H6、C3H6 B.C2H2、C4H8
C.C2H4、C3H6 D.C2H2、C6H6
解析:所有烯烃的含碳的质量分数是相等的,烷烃的含碳量比烯烃的低,炔烃的含碳量比烯烃的低。C2H6、C3H6组成的混合气体,含碳量比乙烯的低
答案:A
8.两种气态烃以任意比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状况,所得气体体积仍是10 L。下列各组符合此条件的是( )
A.CH4、C2H4 B.CH4、C3H6
C.C2H4、C3H6 D.C2H2、C3H6
解析:在题设条件下,平均氢原子数为4的符合要求,只有A组两种物质,无论以何种比例混合,平均氢原子数一定为4。
答案:A
9.一种气态烷烃和一种气态烯烃,它们的每个分子里的碳原子数相同。若1.0体积这种混合物在氧气中充分燃烧生成2.0体积的CO2和2.4体积的水蒸气(相同条件下测定),则混合烃中烷烃和烯烃的体积之比是( )
A.3∶1 B.1∶3
C.2∶3 D.3∶2
解析:该混合烃的平均分子式为:C2H4.8。则烷烃为C2H6,烯烃为C2H4。根据平均氢原子数,利用十字交叉法可求得二者体积比为2∶3。
答案:C
10.有氢气和乙烯的混合气体,其中乙烯的体积分数为x%,取此混合物1 L,用催化剂使两者反应完全,体积变为(同温同压下)( )
A.1 L
B.![]() L或
L或![]() L
L
C.0.5 L
D.![]() L
L
解析:若H2完全反应,气体体积变为![]() L;若乙烯完全反应,气体体积变为
L;若乙烯完全反应,气体体积变为![]() L。
L。
答案:B
二、填空题
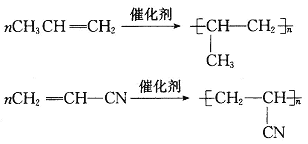
11.常用的塑料包扎绳的化学成分是聚丙烯,试写出合成它的化学方程式_____________________。腈纶(人造羊毛)的主要成分是聚丙烯腈(丙烯腈CH2==CH—CN),试写出合成它的化学方程式__________________________。
答案:
12.在120 ℃时分别进行如下四个反应:
A.2H2S+O2====2H2O+2S
B.2H2S+3O2====2H2O+2SO2
C.C2H4+3O2====2H2O+2CO2
D.C4H8+6O2====4H2O+4CO2
(1)若反应在容积固定的容器内进行,反应前后气体密度(d)和气体总压强(p)分别符合关系式d前=d后和p前>p后的是________;符合关系式d前=d后和p前=p后的是________(用反应的代号表示)。
(2)若反应在压强恒定、容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和V前<V后的是________;符合d前>d后和V前>V后的是________。
解析:(1)由于容器体积不变,所以,只要反应前后气体质量不变,其密度不变,显然,d前=d后的有B、C、D,又由p1/p2=n1/n2可得,同时符合p前>p后只有B;符合p前=p后的只有C。同理,可得第(2)问为C、D
答案:(1)B C (2)D A
13.通常情况下,烷烃可以由相应的烯烃经催化剂加氢得到。但是,有一种烷烃A,分子式C9H20,它却不能由任何C9H18的烯烃催化加氢得到。而另有A的三个同分异构体B1、B2、B3,却分别可由而且只能由1种自己相应的烯烃催化加氢得到。则A、B1、B2、B3的结构简式分别为:
A________、B1________、B2________、B3________。
解析:因A不能由相应的烯烃加氢得到,说明在A中,任意相邻的两个碳原子,至少有一个没有氢原子,所以,A的结构简式为:(CH3)3CCH2C(CH3)3
答案:A.(CH3)3CCH2C(CH3)3
B1.(CH3)3CC(CH3)2CH2CH3
B2.(CH3CH2)4C
B3.[(CH3)2CH]2C(CH3)2
14.实验室制取乙烯常因温度过高生成少量SO2,有人设计了下列实验以确证上述混合气体中含有乙烯和SO2。
(1)如图5—4A、B、C、D装置中可盛放的试剂是(填序号)
A、______________;B、______________;C、______________;D、______________。
①品红溶液
②NaOH溶液
③溴水
④KMnO4酸性溶液
(2)能说明SO2气体存在的现象是________________。
(3)使用装置B的目的是________________。
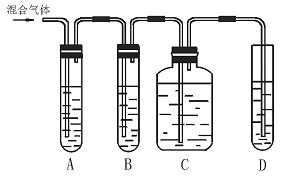
图5—4
(4)使用装置C的目的是________________。
(5)确证含有乙烯的现象是________________。
解析:乙烯和二氧化硫都能使溴水和酸性KMnO4溶液褪色,利用乙烯不与NaOH溶液反应而二氧化硫能跟NaOH溶液反应的性质可除去二氧化硫。用品红溶液是否褪色可检验二氧化硫的存在,除去二氧化硫后,可利用酸性KMnO4溶液来确定乙烯的存在。
答案:(1)① ② ① ④(或③)
(2)装置A中品红溶液褪色
(3)除去SO2气体,以免干扰乙烯的性质实验
(4)检验SO2是否除尽
(5)装置C中的品红溶液不褪色,装置D中的酸性KMnO4溶液褪色
三、计算题
15.在温度为150℃条件下,向密闭容器中充入1 mol丙烯和甲烷混合气体,再充入足量氧气点燃。待反应完全后,再恢复到150℃。欲使丙烯和甲烷混合气体对氢气的相对密度 ρ≥15.8,且反应后气体增加的总物质的量n≤0.4 mol,通过计算说明丙烯和甲烷的物质的量之比应满足的条件。
解析:
C3H6+4.5 O2—→3CO2+3H2O Δn
1 0.5
n(C3H6)
![]() n(C3H6)
n(C3H6)
CH4+2O2—→CO2+2H2O Δn
1 0
所以,![]() n(C3H6)≤0.4 mol
n(C3H6)≤0.4 mol
n(C3H6)≤0.8 mol
![]() ≥15.8×2
≥15.8×2
解得:![]() ≤
≤![]()
答案:![]() ≤
≤![]() ,且n(C3H6)≤0.8
,且n(C3H6)≤0.8