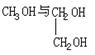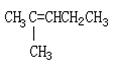高中学生学科素质训练
高二化学期中测试题
本试卷分第一卷(选择题)和第二卷(非选择题)两部分,共150分,考试时间为120分钟。
第Ⅰ卷(选择题,共72分)
可能用到的原子量H―1 C―12 N―14 O―16
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意。)
1.1828年,德国化学家Wohler曾将一种无机盐直接转变为有机物尿素,这一成果称为有机化学发展史上的里程碑,Wohler使用的无机盐是 ( )
A.(NH4)2CO3 B.NH4CNO C.CH3COONH4 D.NH4NO3
2.将1molCH4与Cl2发生取代反应,待反应完全后,测得四种取代物的物质的量相等,则消耗的Cl2为 ( )
A.0.5mol B.2mol C.2.5mol D.4mol
3.m mol C2H2跟nmolH2在密闭容器中反应,当该可逆反应进行到一定程度时,生成pmolC2H4,将反应后的混合气体完全燃烧,生成CO2和H2O,所需氧气的物质的量是 ( )
A.(3m+n)mol B.![]()
C.![]() D.
D.![]()
|
[![]() 是苯基,环用键线表示,C、H原子都未画出]
是苯基,环用键线表示,C、H原子都未画出]
据此,可判断1,2,3,4,5―五氯环戊烷(假定5个碳原子也处于同一个平面上)的异构体数是 ( )
A.4 B.5 C.6 D.7
5.已知二氯苯的同分异构体有三种,从而可推知四氯苯的同分异构体数目是 ( )
A.1种 B.2种 C.3种 D.4种
6.工业上用煤干馏可得煤焦油,再将煤焦油分馏,可得到有机合成原料是 ( )
①苯、甲苯、二甲苯 ②苯酚 ③萘 ④沥青 ⑤焦炭
A.① B.①② C.①②③ D.全部都是
7.欲从苯酚的乙醇溶液中回收苯酚,有下列操作:①蒸馏;②过滤;③分液;④加入足量的金属钠;⑤通入过量的CO2;⑥加入足量的NaOH溶液;⑦加入足量的FeCl3溶液;⑧加入乙酸与浓硫酸混合液;⑨加入足量的浓溴水;⑩加入适量盐酸。合理的步骤是 ( )
A.④⑤⑩ B.⑥①⑤③ C.⑨②⑧① D.⑦①③⑩
8.甲醇、乙二醇、甘油分别与足量金属钠作用,产生等量的H2,则这三种醇的物质的量之比为 ( )
A.6:3:2 B.1:2:3 C.3:2:1 D.4:3:2
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。)
9.以M原子为中心形成的MX2Y2分子中,X、Y分别只以单键与M结合,下列说法正确的是 ( )
A.若MX2Y2分子为平面四边形就有2种同分异构体
B.若MX2Y2分子为平面四边形则无同分异构体
C.若MX2Y2分子为四面体形就有2种同分异构体
D.若MX2Y2分子为四面体形则无同分异构体
10.有关实验室制乙烯的说法中,不正确的是 ( )
A.温度计要插入到反应物的液面以下
B.反应过程中溶液的颜色会逐渐变黑
C.生成的乙烯中混有刺激性气味的气体
D.加热时要注意使温度缓慢上升至170℃
11.下列说法错误的是 ( )
A.石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油
B.含C18以上烷烃的重油经过催化裂化可以得到汽油
C.煤是由有机物和无机物组成的复杂的混合物
D.煤中含有苯和甲苯,可用先干馏后分馏的方法把它们分离出来
12.两种烃的混合物完全燃烧后生成的二氧化碳的物质的量比水的物质的量多,该混合烃的的组成不可能是 ( )
A.两种烯烃 B.一种烷烃和一种烯烃
C.一种烯烃和一种炔烃 D.一种烷烃和一种炔烃
|
A.CH4和C4H10 B.
|
C. D.C6H12与C4H8
|
15.下列说法正确的是 ( )
A.羟基直接跟碳原子结合的物质是醇
B.苯酚溶液可与纯碱反应,并生成CO2
|
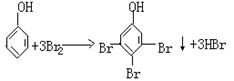
C.苯酚与浓溴水反应的方程式为
D.苯酚有毒,使用时不小心沾到皮肤上,应立即用酒精洗涤;苯酚有杀菌作用,故药皂中常掺入少量的苯酚。
16.下列有机物化合物中,既可作防冻剂又可制造炸药的是 ( )
A.三硝基甲苯 B.甲苯 C.丙三醇 D.乙二醇
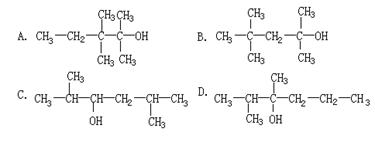
|
|
A. B.
C.CH3CH=C(CH3)CH2CH3 D.CH2=CHCH(CH3)2
18.含碳原子数为10或小于10的烷烃分子中,其中一卤代烃不存在同分异构体的共有 ( )
A.2种 B.3种 C.4种 D.5种
第Ⅱ卷(非选择题,共78分)
三、(本题包括2小题22分)
19.(12分)(1)区分下列各组有机物(填“操作―现象―判断”)
①1―丙醇和丙三醇
②苯甲醇和苯酚
③乙醇和乙醚
④乙烯、苯、苯酚
(2)除去下物质中的少量杂质(括号内的物质),加入的试剂及操作方法分别为
①乙醇(水) ②溴乙烷(乙醇)
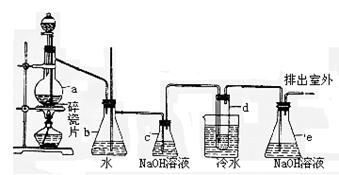
20.(10分)
|
(1)写出本题中制备1,2―二溴乙烷的两个化学反应方程式: ,
。
(2)安全瓶 b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象: 。
(3)容器c中NaOH溶液的作用是 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因。
|
|
|
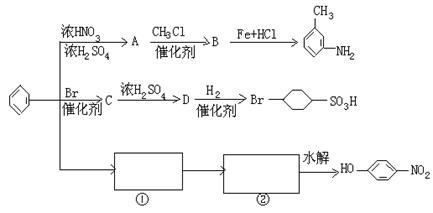
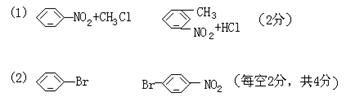
(2)图中 ①→②省略了反应条件,请在①和②上方的方框里填写对应物质的
结构简式。
(3)B分子苯环上的任意两个氢原子被溴原子取代后,得到的二溴代物有 种同分异构体。
22.(5分)某液态烃的分子式为CmHn,相对分子质量为氢气的46倍,它能使酸性高锰酸钾溶液褪色,但不能使溴水褪色。在催化剂镍存在下,9.2g该烃能与0.3mol氢气发生加成反应,生成饱和烃CmHp。则m、n、p的值分别为 、 、
,CmHn的结构简式是 ,CmHp的名称是 。
五、(本题包括2小题,共17分)
23.(10分)有A、B、C、D、E五种气态烃,其中A、B、C能使酸性KMnO4溶液褪色;1molC能与2mol溴完全加成,生成物分子中每个碳原子上都有一个溴原子;A与C具有相同的通式,A与H2加成得B,B与相同条件下氮气的密度相等;D是最简单的有机物,E是D的同系物,完全燃烧相同物质的量的B、E,生成相同物质的量的CO2,试写出A、B、C、D、E五种烃的名称:
A 、B 、C 、D 、E 。
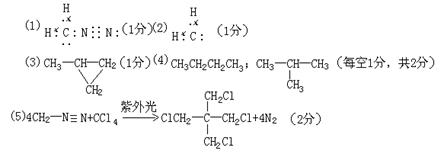
24.(7分)重氮甲烷(CH2N![]() N)在有机合成中有着重要应用。它的分子中碳原子和氮原子之间的共用电子对是由氮原子一方提供的。
N)在有机合成中有着重要应用。它的分子中碳原子和氮原子之间的共用电子对是由氮原子一方提供的。
(1)重氮甲烷的电子式是 。
(2)重氮甲烷在受热或光照时容易分解放出N2,同时生成一个极活泼的缺电子基团碳烯(:CH2),碳烯的电子式是 。
(3)碳烯很容易以它的一对未成键电子对与不饱和的烯、炔发生加成,形成三元环状化合物。它与丙烯发生加成反应后所得产物的结构简式为 。
(4)碳烯还可以插入C―H键之间,使碳链加长。它插入丙烷分子中C―H键之间,碳链增长后的化合物的结构简式是 或 。
(5)重氮甲烷的CCl4溶液用紫外光照射时发生反应,生成一种相对分子质量为210的有机物和N2,写出反应的化学方程式(有机物用结构简式表示)
。
六、(本题包括2小题,共26分)
25.(6分)某工业反应混合液中仅可能含有的组分是:乙醚(C4H10O)、乙醇和水,经分析,液体中C、H、O的原子数之比为16:42:5。
(1)若混合液中只含2种组分,则所有可能的组合是 。
(2)若混合液中含有3种组分,在628g混合液中有1mol H2O,此时乙醇和乙醚的物质的量各是多少?
26.(20分)饱和链烃A和不饱和链烃B在常温下均为气体,其中A含有的碳原子数多于B。
(1)将A和B按一定比例混合,1L混合气体完全燃烧后得到3.6LCO2气体,试推断混合气体A和B所有可能的组合及A、B的体积比,并将结果填入下表:
| 编号 | A的分子式 | B的分子式 | VA/VB |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
(2)1mol该混合气体恰好能使含0.4mol溴的四氯化碳溶液完全褪色,推断上表中符合该条件的A、B的分子式,填入下表:
| A的分子式 | |||
| B的分子式 |
(3)120℃时,1LA、1LB与足量O2混合点燃后,在同温、同压下总体积增大2L,试通过计算确定A和B的分子式。
高 二 化 学(下)期 中 测 试 题 答 案
1.B 2.C 3.D 4.A 5.C 6.C 7.B 8.A 9.AD 10.D 11.D 12.AB 13.A 14.D
15.D 16.C 17.CD 18.C
19.(12分)①分别加入新制的Cu(OH)2悬浊液,充分振荡,出现绛蓝色的为丙三醇。
②加水溶解,分别滴入FeCl3溶液,出现紫色的为苯酚(或加入过量浓溴水,出现白色沉淀的为苯酚。)
③分别加入金属钠,发生反应放出气体的是乙醇。
④分别加入浓溴水,充分振荡能使溴水褪色的为乙烯;出现白色沉淀的为苯酚;溶液出现分层,上层为橙红色,下层为无色的为苯。(2分)
|
20.(10分)
|
![]() CH2=CH2+Br2
CH2Br―CH2Br(1分)
CH2=CH2+Br2
CH2Br―CH2Br(1分)
(2)b中水面下降,玻璃管中水柱上升,甚至溢出。(2分)
(3)除去乙烯中带出的酸性气体(或除去CO2、SO2)
(4)①乙烯发生(或通过液溴)速度过快。
②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(2分)
|
|
(3)6(2分)
|
22.(5分)7;8;14; ;甲基环乙烷(每空1分)
23.(10分)
|
24.(7分)
25.(6分)提示:乙醚可写成(CH2)4(H2O)、乙醇可写成(CH2)2(H2O)、水可写成(CH2)0(H2O)
混合液可写成(CH2)16(H2O)5。
答案:(1)乙醚和乙醇、乙醚和水(每组1分,共2分)
(2)乙醇2mol;乙醚7mol(每个数据2分,共4分)
26.(20分)(1)
| 编 号 | A的分子式 | B的分子式 | VA/VB |
| ① | C4H10 | C2H2 | 4:1 |
| ② | C4H10 | C2H4 | 4:1 |
| ③ | C4H10 | C3H4 | 3:2 |
| ④ | C4H10 | C3H6 | 3:2 |
(2) (每空1分,共12分)
| A的分子式 | C4H10 | C4H10 |
| B的分子式 | C2H2 | C3H6 |
(3)由下列反应式分析1L烃燃烧后的体积增加△V。
![]() △V1=1.5(L)
△V1=1.5(L)
![]() △V2=-0.5(L)
△V2=-0.5(L)
![]() △V3=0(L)
△V3=0(L)
![]() △V4=0
△V4=0
![]() △V5=0.5(L)
△V5=0.5(L)
因△V1+△V5=2.0L
故混合烃中A是C4H10,B是C3H6(每种物质2分,共4分)