�߶���ѧ�ڶ�ѧ�����п��Ծ�4
�����֢����ѡ���⣩�͢������ѡ���⣩�����֣�����100�֣�������ʱ90���ӣ�
�ڢ����ѡ���⣬��50�֣�
һ��ѡ���⣨�������25С�⣬ÿС��2�֣���50�֣�ÿС��ֻһ��ѡ��������⡣��
1��2005��1�£�ŷ����ֵĻݸ�˹��̽�����״γɹ���½���ǵ�������ǡ�������������ѧ�Ҷ�̽�������ص����ݽ����˷����������������Ĵ������к���95%�ĵ�����ʣ�������Ϊ���������̼�⻯������й���̼�⻯�����������ȷ���ǡ������������������������� (���� )
A��̼�⻯�����ͨʽΪCnH2n+2���������� B��ʯ�͵���Ҫ�ɷ���̼�⻯����
C���л��ﶼ��̼�⻯����������������� D��̼�⻯�����еĻ�ѧ�����Ǽ��Լ�
2�����������ᵼ��ʳƷ�������к����ǡ����������� ��������������������������������
�����������·�Ϸ�ɹ��ʳ �����������������������㳦�мӹ������������Ա�����������
������������úֱ���տ�����Ѽ�������������������� ���á����⾫��(һ�ֺ����ص�����)ι������
��������С�մ������ͷ�������������������������� ������ϩ����ˮ��
����A���٢ڢۢݡ����� B���٢ڢۢܡ������� C���ڢۢܢݡ��� D���٢ڢۢܢ�
3����������Ϊ��������ǡ��������������������������������������������������������������������������������������� �� ��
������ A�����ۡ���������������������������������������������������B��������ϩ��
C��CH4��Cl2���շ�Ӧ��������� ����D��������
![]()
![]() 4��������������ͬϵ���һ���ǡ��� ������������������������������������������ �� ��
4��������������ͬϵ���һ���ǡ��� ������������������������������������������ �� ��
A��CH3Cl��CH2Cl2������ B����������������
C��C10H22��CH4���������� ����D�����ۺ���ά��
5��������ϩ���ӽṹ��˵���У�������ǡ����������������������������� ������ ��������
A����ϩ�����ﺬ��C=C˫��������
B����ϩ����������ԭ�ӹ�ƽ��
����C����ϩ������C=C˫�������ͼ��������C-C�����ļ������
����D����ϩ����������ۼ�֮��н�ԼΪ120O
6������ʵ�鲻������������ǡ����������������������������������������������������������������������������� ��������
A�����屽���� ������ B�����ѻ��������� C������ϩ������ �� D��������Ӧ
7�����л�����е�Ƚϴ�����ǡ������������������������������������������������������������������������� ��������
������ A�������飾�����飾�����顡���������������� B�� I2��Br2��Cl2
������ C�����飾���飾���顡�������������������������� D��һ�ȶ��飾һ�����飾һ�ȼ���
8��ij�л���Ľṹ��ʽΪ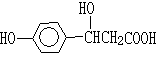 �������Է����ķ�Ӧ�����С�(���� )
�������Է����ķ�Ӧ�����С�(���� )
(a)ȡ����(b)�ӳɡ�(c)��ȥ��(d)������(e)ˮ�⡡(f)�к͡�(g)�Ӿ�
A��(a)(c)(d)(f)�� ��B��(b)(e)(f)(h)�� �� C��(a)(b)(c)(d)(f)���� D����(e)��
9���ܷ���������Ӧ��������ụΪͬ���칹����ǡ����������������������� (���� )
A��������� ������B������������ ������ C����ȩ ��������D���������
10�����淢�ڵĺ���ͭ˿���뵽���д��У�ͭ˿���ָܻ��������ǡ����������� (���� )
����A��(CH3)3CCH2OH��B��(CH3) 2CHOH�� C��(CH3)3COH������D��CH3OH
11������Ȼ�����Һ��������ж����������нⶾ�����У���ȷ���ǡ��������� (���� )
A������ϡ������ͭ��Һ��ʹBa2�����BaSO4������
B������С�մ���Һ��ʹBa2�����BaCO3������
C�����ô���������Ba2����ʹ�����ʱ���
D�����ô�����ˮ��ʹѪҺ�����۵ĵ����������ܽ�
12�������л������������ԭ��һ����ͬһƽ���ڵ��ǡ��������������������� (���� )
![]()
![]()
13��
������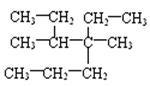 ��������ȷ���ǡ�����������������������
������ ��
��������ȷ���ǡ�����������������������
������ ��
�� A��4������4��5�����һ����顡����B��3������2��3�����һ�����
�� C��4��5��������4���һ����顡����D��3��4��������4���һ����顡
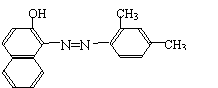 14���յ�����������ҽ�ֹ����ʳƷ�����ĺϳ�ɫ�أ����С��յ����š��Ľṹ��ʽ��ͼ��ʾ�����й��ڡ��յ����š�˵���������
14���յ�����������ҽ�ֹ����ʳƷ�����ĺϳ�ɫ�أ����С��յ����š��Ľṹ��ʽ��ͼ��ʾ�����й��ڡ��յ����š�˵���������
A�������ڱ�������������
B����ѧʽΪC18H16N2O
C�� ���ڼױ���ͬϵ��
D������ʹ���Ը��������Һ��ɫ
15��1mol��������40g���д���Ӧ���ų��������ٵ��ǡ������������������������������������������� ��
������ A���Ҵ���������������������������������������������������B���Ҷ�������������������
������ C������������������������������������������������������ D���״�
16������������ϩ���ױ�������������������Һ��һ���Լ��ǡ����������� ������ ��
A���Ȼ�����Һ����ˮ��������B��̼������Һ����ˮ
C�����Ը��������Һ����ˮ��D�����Ը��������Һ���Ȼ�����Һ
17���л���������������ᣬҲ�ɻ�ԭ���ɴ����ɼ����ɵ�����ʹ���һ�������£��������ɻ������ң������ʽΪC2H4O2�����������в���ȷ���ǡ������������������� ��������
A��������C����������Ϊ40%����B�����ڳ��³�ѹ��Ϊ��ɫҺ��
C���ұȼķе�ߡ��������������� D���Һͼ����ʽ��ͬ
18�����и��������и�������ݣ�����ݸ�ȡ1Ħ������������������ȫȼ�գ�����CO2 ��H2O �����ߺ���������ͬ���ǡ��������������������������� ��������������������������
A������ͼ��顡��B����ϩ���Ҵ��� C����ϩ�������ǡ�D����Ȳ�ͼ������
19�������йس����ʣ�������Ϊ���ʣ��IJ����У�������ǡ��������������� ��������
A���������֣����ᣩ��������������̼������Һ����������ռ������
B���Ҵ���ˮ��������������ʯ�ң������ռ������
C���������ӣ�������ˮ�������˳�ȥ����
D���������������ᣩ���ӱ���̼������Һ���������Һ����ˮ��
20��ij�л������������ң�����ʽΪ![]() ��������ˮ��ɵñ���1 mol����2 mol�ҷ�Ӧ�õ�һ�ֺ��ȵ�����
��������ˮ��ɵñ���1 mol����2 mol�ҷ�Ӧ�õ�һ�ֺ��ȵ�����![]() �����ɴ��ƶϼĽṹ��ʽΪ����������������������
�����ɴ��ƶϼĽṹ��ʽΪ����������������������
����A��![]() ��������������B��
��������������B��![]()
C��![]() ���������������� D��
���������������� D��![]()
21��������̬�����ʵ��������,��105��ʱ1 L�û������9 L�������,���ȼ�պ�ָ���ԭ״̬,�������������11 L.���и��������в����ϴ��������ǡ����������������� ��������
A��CH4��C3H8����B��C2H4��C4H10����C��C4H10��C3H6����D�� C4H8��C3H8
22��3.42��������3.24�˵��ۻ�ϲ���ȫˮ�⣬������m�������Ǻ�n�˹��ǣ���m�Un��ֵ�ǡ�����������������������������������������������������������
A��1�U3����B��1�U5����C��5�U1����D��3�U1
23����1molCH4���������������ܱ������е�ȼ����ַ�Ӧ�������������ʣ�࣬�Ҳ����Ϊ���壨101kPa��120�棩����������Ϊ72g,�����й���������ȷ���ǡ���������������������������������������
������ A����������ͨ����ʯ�ң��ܱ���ȫ���գ���ͨ��Ũ���ᣬ���ܱ���ȫ����
������ B�������ƽ��Ħ������Ϊ24g/mol
������ C����������ͨ��Ũ���������պ�ָ�����101kPa��120�棩����ѹǿ��Ϊԭ���������1/3
������ D����Ӧ�����ĵ�����Ϊ56g
24����֪������A��![]() ���������飨
���������飨![]() ���ķ��ӽṹ���ƣ�����ͼ��
���ķ��ӽṹ���ƣ�����ͼ��

��![]() �Ķ��ȴ����ͬ���칹����ĿΪ��������
������������������ ��������
�Ķ��ȴ����ͬ���칹����ĿΪ��������
������������������ ��������
A��3��������B��4��������C��5����������D��6
25����ƷһֱӰ����ᰲ������Ⱥͺ������DZ��ϸ����Ķ�Ʒ����֪��ȵķ���ʽ��
C17H19NO3������������ȵĶ���������������ķ���ʽ�ǡ���������������������
A��C21H22NO5������B��C21H27NO7������C��C21H23NO5������D��C21H23NO3��
�ڢ������ѡ���⣬��50�֣�
��������⣨��12�֡�����ȷ����д�����еĺ����ϡ���
26����4�֣���Ҫ����գ� ��CH3_________������ʽ������NO2_____________�����ƣ���
��OH_____________�����ƣ��� �Ȼ�_______________���ṹʽ��
27����8�֣�2006��3��27������9ʱ40�����ң����������������������廯��ó������˾����2�Ż�ϱ����ޣ���ְ���������������¹�װ�ܵ�����й¶��������ը������119ָ�����Ľӵ������绰����������13���������� 80����ָսԱ�����˾Ȼ��֡�����2�Ŵ�������4�ֻ�ϱ����û�ϱ���95%�Ķ��ױ���4%�ļױ���
(1)���ڼ�λ�ò�ͬ�����ױ�������ͬ���칹�壬��д�����ǵĽṹ��ʽ��������������������������
(2) ���ױ����ױ�Ϊ��ȼҺ�壬������������ǿ�Ⱦͻ�����ȼ�ձ�ը����д���ױ�ȼ�յĻ�ѧ����ʽ����������������������������������������������ȼ������������������������������
(3)�������ױ���һ������ըҩ�������ɼױ���Ũ���ᡢŨ����Ļ����Һ���ȵõ��ģ���д���÷�Ӧ�Ļ�ѧ����ʽ����������������������������������������������������������
����ʵ���⣨��10�֡�����ȷ����д�����еĺ����ϡ���
28����10�֣�ijҺ̬±����RX(R�������X��ij��±��ԭ��)���ܶ���a g��cm-3����RX���Ը�ϡ���ˮ�ⷴӦ����ROH���ܸ�ˮ���ܣ���HX��Ϊ�˲ⶨRX�ķ��������ⶨ��ʵ�鲽�����£�
�١� ȷ��ȡ��±����b mL��������ƿ�С�
�ڡ� ����ƿ�м������ϡNaOH��Һ�����ϴ��г������ܵ����ӣ����ȣ�������Ӧ��
�ۡ� ��Ӧ��ɺ���ȴ��Һ����ϡHNO3�ữ���μӹ���AgNO3��Һ�õ���ɫ������
�ܡ� ���ˡ�ϴ�ӡ��������أ��õ�����c g��
�ش����⣺(1)װ���г������ܵ�������________________��
(2)������У�ϴ�ӵ�Ŀ����Ϊ�˳�ȥ������������________���ӡ�
(3)��±����������±�ص�������____________���жϵ�������_____________��
(4)��±����ķ�������_____________���г���ʽ����
(5)����ڲ��ۢ��У���HNO3�������㣬û�н���Һ�ữ��������в�õ�
cֵ��������ѡ����룩_______��
A��ƫ������ B.ƫС�������� C.���� ������D.��С����
�ġ��ƶ��⣨��22�֡�����ȷ����д�����еĺ����ϡ���
29����10�֣���ѧ�ҷ���ijҩ��M��������Ѫ�ܼ�������Ϊ�������������ͷų�һ�֡���ʹ���ӡ�D����������D�������ڵ�����ԭ����Ϊ�����ǻ����1998��ŵ��������ѧ��ҽѧ������ش����⣺
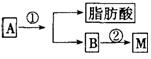 (1)��֪M�ķ�����Ϊ227����C��H��O��N����Ԫ����ɣ�C��H��N��������������Ϊ15.86����2.20����18.50����������C��N��Oԭ�Ӹ�����Ϊ1��1��3����M�ķ���ʽ��________��D��˫ԭ�ӷ��ӣ�������Ϊ30����D�ķ���ʽΪ_________��
(1)��֪M�ķ�����Ϊ227����C��H��O��N����Ԫ����ɣ�C��H��N��������������Ϊ15.86����2.20����18.50����������C��N��Oԭ�Ӹ�����Ϊ1��1��3����M�ķ���ʽ��________��D��˫ԭ�ӷ��ӣ�������Ϊ30����D�ķ���ʽΪ_________��
(2)��֬A������;���ɵõ�M��
ͼ�Тڵ���ʾ��C2H5OH+HO-NO2![]() C2H5O-NO2+H2O
C2H5O-NO2+H2O
������������������������ ���ᡡ������ ��������
��Ӧ�ڵĻ�ѧ����ʽ������������������������������������������������ ��
(3)C��B��������һ�������·�Ӧ���ɵĻ����������Ϊ134��д��C���п��ܵĽṹ��ʽ���������������������������� ��
(4)����0��1molB�������Ľ�����Ӧ��������_______g�����ơ�
 30����12�֣�����Ҫ�Ļ�ʽԭ�ϣ�ͨ���������̿ɺϳɰ�˾ƥ�֡����Ϻ�һЩ�߷��ӻ����
30����12�֣�����Ҫ�Ļ�ʽԭ�ϣ�ͨ���������̿ɺϳɰ�˾ƥ�֡����Ϻ�һЩ�߷��ӻ����
��֪��
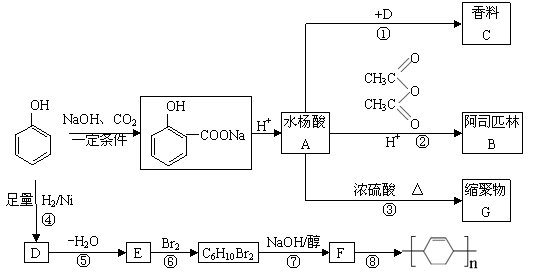 |
����������������+ ��+ CH3COOH
��1��д��C�Ľṹ��ʽ������������������������������������������
��2��д����Ӧ�۵Ļ�ѧ����ʽ���������������������������������������������������������������� ��
��3��д��B�Ľṹ��ʽ������������������������������������������ ��
��4��д����Ӧ�ݵĻ�ѧ����ʽ���������������������������������������������������������������� ��
��5��д����Ӧ���ͣ����������������������������������� ���������������������������������� ��
�塢�����⣨��6�֣�
31���л���A�����ĺ������������ͬ�����£�A������������ͬ����Ҵ�������1.61����1.11��A��ȫȼ�պ�IJ����ͨ����ʯ�ң����ʯ����������2.79�ˣ���ͨ�����������ף���������������������0.81�ˡ���֪A��������Ʒ�Ӧ�ų�������Ҳ��������������ͭ�����ȣ���Ӧ���ɺ�ɫ������
(1)ͨ������д��A�Ľṹ��ʽ��
(2)��1.11��A����������������ͭ���ȣ����ú�ɫ������������
�߶���ѧ�ڶ�ѧ�����п��Դ��
�༶�� ������ ���������������� ����������������
ԭ������H:1��C:12��N:14��O:16��Na:23��Mg:24��Al:27��S:32��Cl:35.5��Cu:64
�ڢ����ѡ���⣬��50�֣�
һ��ѡ���⣨�������25С�⣬ÿС��2�֣���50�֣�ÿС��ֻһ��ѡ��������⡣��
�뽫��ȷ��Ϳ�ڴ����
�ڢ������ѡ���⣬��50�֣�
��������⣨��12�֡�����ȷ����д�����еĺ����ϡ���
26����4�֣���CH3�������������������� ������ʽ������NO2������������������ �����ƣ���
��OH������������������������ �����ƣ��� �Ȼ����������������������������� ���ṹʽ��
27����8�֣�
(1)�������������������������������� �������������������������������� ��������3�֣�
(2)��ѧ����ʽ���������������������������������������������������� ��������
ȼ��������������������������������1�֣�
(3)��ѧ����ʽ��������������������������������������������������������������
����ʵ���⣨��10�֡�����ȷ����д�����еĺ����ϡ���
28����10�֣�
(1)װ���г������ܵ����������������������������������� �������������������������� ��
(2)��ȥ������������������������������������������������ ���ӡ�
(3)±�ص�������____________��
�жϵ��������������������������������������������������������������������������� ��
(4)��±����ķ��������������������������������������������� ���г���ʽ����
(5)������в�õ�cֵ��������ѡ����룩���������������� ��
A��ƫ������ B.ƫС�������� C.���䡡���� D.��С����
�ġ��ƶ��⣨��22�֡�����ȷ����д�����еĺ����ϡ���
29����10�֣�(1) M�ķ���ʽ�������������������� ��D�ķ���ʽΪ������������������ ��
(2) ��Ӧ�ڵĻ�ѧ����ʽ������������������������������������������������������ ��
(3)д��C���п��ܵĽṹ��ʽ������ ������������������������������������������ ��
(4)����0��1molB�������Ľ�����Ӧ��������_______g�����ơ�
30����12�֣���1��C�Ľṹ��ʽ���������������������������������������������� �������������������� ��
��2����Ӧ�۵Ļ�ѧ����ʽ������������������������������ ���������������������������������������������������� ��
��3��B�Ľṹ��ʽ�������������������������� �������������������������������������� �������� �� ��
��4����Ӧ�ݵĻ�ѧ����ʽ�������� ������������������������������������������������ ����������������������������
��5����Ӧ���ͣ������������� ����������������������������������������
�塢�����⣨��6�֣�
31�� (1)
(2)
������ ��