高二化学《烃》测试题
班级 姓名 成绩
A 卷 (满分100分)
可能用到的元素的相对原子质量:
H—1 C—12 O—16
一、选择题(每小题3分,共60分。每小题只有一个选项符合题意。)
1.下列有机物的命名正确的是 ( )
A. 1,2─二甲基戊烷 B. 2─乙基戊烷
C. 3,4─二甲基戊烷 D. 3─甲基己烷
2.不能使酸性KMnO4溶液褪色的是 ( )
A. 乙烯 B. 聚乙烯 C. 甲苯 D. 乙炔
3.下列反应的生成物为纯净物的是 ( )
A. CH4和Cl2光照 B. 氯乙烯加成
C. 乙醇和浓H2SO4共热 D. 乙烯和氯化氢加成
4.有三种不同的基团,分别为-X、―Y、―Z,若同时分别取代苯环上的三个氢原子,能生成的同分异构体数目是 ( )
A. 10 B. 8 C. 6 D. 4
5.下列实验室制取气体的方案中,正确的是 ( )
A. 用食盐水和浓硫酸制取氯化氢
B. 将氯化铵晶体加热分解制取氨气
C. 将酒精和浓硫酸按1∶3混合,加热至170℃制取乙烯
D. 用二氧化锰和稀盐酸制取氯气
6.下列反应属于置换反应的是 ( )
A. Cu+2FeCl3=CuCl2+2FeCl2 B. SO2+2H2S=2H2O+3S
C. Cl2+C2H4![]() C2H5Cl+HCl D. 2KClO3+I2
C2H5Cl+HCl D. 2KClO3+I2![]() Cl2+2KIO3
Cl2+2KIO3
7.分子式为C8H10的芳香烃,苯环上的一硝基取代物只有一种,该芳香烃的名称是
( )
A. 乙苯 B. 邻二甲苯 C. 间二甲苯 D. 对二甲苯
8.二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟里昂”产品,用作空调、冰箱和冷冻库等中的致冷剂。试判断二氟甲烷的结构简式 ( )
A. 有4种 B. 有3种 C. 有2种 D. 只有1种 MCE01
9.在标准状况下,C2H4和CO混合气体100 L,充分燃烧时耗用等体积的O2,则CO与C2H4的体积比是 ( )
A. 1∶4 B. 4∶1 C. 2∶1 D. 1∶2
10.下列各组混合气体中,比乙烯含碳量高的是 ( )
A. 甲烷和丙烯 B. 乙烷和丁烯
C. 环丙烷与丙烯 D. 丙烯与丙炔
11.已知天然气的主要成份CH4是一种会产生温室效应的气体,等物质的量的CH4和CO2产生的温室效应,前者大。下面是有关天然气的几种叙述:① 天然气与煤、柴油相比是较清洁的能源;② 等质量的CH4和CO2产生的温室效应也是前者大;③ 燃烧天然气也是酸雨的成因之一。其中正确的 (MCE01) ( )
A. 是①、②、③ B. 只有① C. 是①和② D. 只有③
12.甲烷和乙炔的混合气体20 mL,完全燃烧需45 mL氧气(同温同压下),则此混合气体中甲烷和乙炔的体积比是 ( )
A. 2∶1 B. 1∶1 C. 3∶2 D. 3∶1
13.萘环上的碳原子的编号如(Ⅰ)式,根据系统命名法,(Ⅱ)式可称为2-硝基萘,则化合物(Ⅲ)的名称应是 ( )

(Ⅰ) (Ⅱ) (Ⅲ)
A. 2,6 - 二甲基萘 B. 1,4 - 二甲基萘
C. 4,7 - 二甲基萘 D. 1,6 - 二甲基萘
14.某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个![]() 和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体) ( )
和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体) ( )
A. 2 B. 3 C. 4 D. 5 02春
15.据报道,1995年化学家合成了一种分子式为C200H202含多个碳碳叁键(-C≡C-)的链状烃,则分子中含碳碳叁键最多可以是 ( )
A. 49个 B. 50个 C. 51个 D. 不能确定
16.环状有机物的组成是C8H8,它不能使溴的CCl4溶液褪色,但能发生取代反应,这种有机物可能含有的结构是 ( )
A. ![]() B.
B. 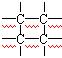
C. ![]() D.
D.
![]()
17.在烧杯中加入水和苯(密度:0.88 g / cm3)各50 mL。将一小粒金属钠(密度:0.97 g / cm3)投入烧杯中。观察到的现象可能是 ( )
A 钠在水层中反应并四处游动
B 钠停留在苯层中不发生反应 (02春上海19)
C 钠在苯的液面上反应并四处游动
D.钠在苯与水的界面处反应并可能作上、下跳动
18.两种气态烃以任意比混合,在105℃时,1 L该混合烃与9 L氧气混合,充分反应后恢复到原状态,所得氧化仍为10 L。下列各组混合烃不符合此条件的是 ( )
A. CH4 C2H4 B. CH4 C3H4
C. C2H4 C3H4 D. CH4 C4H4
19.充分燃烧3 L由甲烷、乙烯和丙炔组成的混合气体,生成7 L CO2和4.82 g水(气体体积均在标准状况下测定),则原混合气体中甲烷、乙烯和乙炔的体积比可能是 ( )
A. 1∶1∶1 B. 1∶2∶3 C. 3∶2∶1 D. 3∶1∶2
20.某气态烃10 mL与50 mL氧气在一定条件下作用,刚好耗尽反应物,生成水蒸气40 mL、一氧化碳和二氧化碳各20 mL(各体积都是在同温同压下测得)。该气态烃为 ( )
A. C3H8 B. C4H6 C. C3H6 D. C4H8
二、(本题包括4小题,共21分)
21.(4分)X、Y是苯环上的两种不同取代基。现有下列一些萘衍生物的结构简式
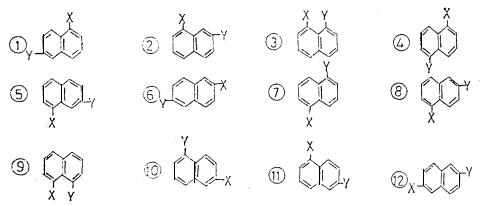
上述化合物中,跟③属于同一种物质的分子式是(用编号回答)___________________;跟①属于同一种物质的分子式是(用编号回答)___________________。
22.(6分)在一定条件下,某些不饱和烃分子可以进行自身加成反应。例如:
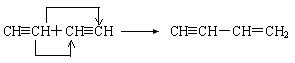
有机物甲的结构简式为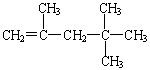 ,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,还同时得到另一种产量更多的有机物丙,其最长碳链仍为5个碳原子,丙是甲的同分异构体。
,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,还同时得到另一种产量更多的有机物丙,其最长碳链仍为5个碳原子,丙是甲的同分异构体。
(1). 乙的结构简式是_____________________。
(2). 丙的结构简式是_____________________。
23.(6分). “立方烷”是新合成的一种烃,其分子为正立方体结构。
(1) 该“立方烷”的分子式为
(2) 该“立方烷”的二氯取代物有 种同分异构体
(3) 芳香烃中有一种化合物与“立方烷”互为同分异构体,则该芳香烃的结构为
24.(5分)1—丁炔的最简式是 ,它与过量溴加成后产物的名称是
;有机物A的分子式与1—丁炔相同,而且属于同一类别,A与过量溴加成后产物的名称是
;与1—丁炔属于同系物的且所含碳原子数最少的有机物是
,它能发生
反应(填反应类别)制成导电塑料![]() ,这是21世纪具有广阔前景的合成材料。
,这是21世纪具有广阔前景的合成材料。
三、(本题包括2小题,共13分)
25.(5分)有5种烃:甲烷、乙炔、苯、环己烷、甲苯,分别取一定量的这些烃,完全燃烧后生成m mol CO2和n mol HO。则
(1) 当m=n时,该烃是
(2) 当m=2n时,该烃是
(3) 当2m=n时,该烃是
(4) 当4m=7n时,该烃是
26.(8分)电石中的碳化钙和水能完全反应:
CaC2+2H2O=C2H2+Ca(OH)2
使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积比,从而可测定电石中碳化钙的含量。
 (1)
若用下列仪器和导管组装实验装置:
(1)
若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是______接_______接______接______接_______接_______。
(2) 仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
① 称取一定量电石,置于仪器3中,塞紧橡皮塞。
② 检查装置的气密性。
③ 在仪器6和5中注入适量水。
④ 待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤ 慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是 。
(3) 若实验产生的气体有难闻的味,且测定结果偏大,这是因为电石中含有__________杂质。
(4) 若实验时称取的电石为1.60 g,测量排出水的体积后,折算成标准状况乙炔的体积为448 mL,此电石中碳化钙的百分含量是________%。
四、计算题(6分)
27.(6分)将100 mL H2、C2H6和CO2的混合气体与300 mL O2混合点燃,经充分反应并干燥后,总体积减少100 mL。再将剩余的气体通过碱石灰吸收,体积又减少100 mL。( 上 述体积均在同温同压下测定)求原混合气体中各组分的体积。
答 案
一、1. D 2. B 3. D 4. A 5. C 6. D 7. D 8. D 9. B 10. D 11. C 12. B 13. D
14. C 15. B 16. B 17. D 18. B 19. B 20. D
二、21. 9;8、11
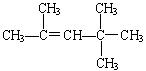
22. (1) ![]() (2)
(2)
23. (1) C8H8 (2) 3 (3) ![]()
24. CH3CH2CºCH;1,1,2,2—四溴丁烷;2,2,3,3—四溴丁烷;HCºCH;加聚;
三、25. (1) 环己烷 (2) 乙炔、苯 (3) 甲烷 (4) 甲苯
26. (1) (6)(3)(1)(5)(2)(4) (2) ②①③⑤④或①③②⑤④ (3) 其它可与水反应产生气体的(若答磷化物或砷化物或硫化物等固态物质名称都给分,答其它如磷化氢、硫化氢等都不给分) (4) 80%
四、27. 设H2、C2H6和CO2的体积分别为2x、2y和z
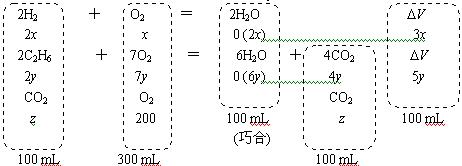
![]() 2x+2y+z = 100
2x+2y+z = 100
x+7y+200 = 300 (或 2x+6y = 100)
4y+z = 100 (或 3x+5y = 100)
解得:2x = 2y = 25 mL,z = 50 mL
答:H2为25 mL,C2H6为25 mL,CO2为50 mL。