高二第二学期开学考试化学试卷
相对原子质量:N―14 O―16 Mg―24 Al―27 Fe―56 Ag--108
Na―23 Cl―35.5 S―32 H―1 Cu―64 Zn―65 K--39
一、单选题(每小题只有一个正确答案,3分×16=48分)
1、下列酸的酸酐中,不能由单质和![]() 直接反应制得的是
直接反应制得的是
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
2、将纯净的![]() 放入一密闭容器中,在一定温度下发生
放入一密闭容器中,在一定温度下发生![]() ,达到平衡后,测得
,达到平衡后,测得![]() 的转化率为20%,则此混合气体的平均分子量是
的转化率为20%,则此混合气体的平均分子量是
A、36.8 B、41.4 C、51.1 D、93
3、常温下![]() 的碱溶液的PH为
的碱溶液的PH为
A、![]() 2 B、12 C、
2 B、12 C、![]() 12
D、无法确定
12
D、无法确定
4、将等质量的![]() 、
、![]() 合金(组分相同),分别投入到下列四种过量溶液中,放出
合金(组分相同),分别投入到下列四种过量溶液中,放出![]() 最多的是
最多的是
A、![]()
![]() B、
B、![]()
![]()
C、![]()
![]() D、
D、![]()
![]()
5、在标准状况下,在250![]() 的烧瓶里充满
的烧瓶里充满![]() 后倒置于水槽中,假设溶解后的溶质不向外扩散,则烧瓶中氨水的物质的量浓度最接近于
后倒置于水槽中,假设溶解后的溶质不向外扩散,则烧瓶中氨水的物质的量浓度最接近于
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
6、一定条件下将等体积![]() 和
和![]() 的混和气体置于试管中,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的
的混和气体置于试管中,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
7、在一个密闭固定体积的容器中加入![]() 和
和![]() 发生反应
发生反应![]() 达到平衡时,C的浓度为
达到平衡时,C的浓度为![]() ,若维持容器体积和温度不变,以下配比作为起始物质达到平衡后C的浓度仍为
,若维持容器体积和温度不变,以下配比作为起始物质达到平衡后C的浓度仍为![]() 的是
的是
A、![]() +
+![]() B、
B、![]() +
+![]() +
+![]() +
+![]()
C、![]() +
+![]() +
+![]() D、
D、![]() +
+![]()
8、对于![]() ,能提高
,能提高![]() 转化率的是
转化率的是
A、加入C B、加入![]() C、加压 D、减小CO
C、加压 D、减小CO
9、下列各组离子,因发生双水解反应而不能大量共存的是
A、![]() 、
、![]() 、
、![]() 、
、![]() B、
B、![]() 、
、![]() 、
、![]() 、
、![]()
C、![]() 、
、![]() 、
、![]() 、
、![]() D、
D、![]() 、
、![]() 、
、![]() 、
、![]()
10、同物质的量浓度的![]() 、
、![]() 、
、![]() 三种正盐溶液,测得溶液的PH分别是9、7、10,则相对应的酸:
三种正盐溶液,测得溶液的PH分别是9、7、10,则相对应的酸:![]() 、
、![]() 、
、![]() 酸性的比较正确的是
酸性的比较正确的是
A、![]() B、
B、![]()
C、![]() D、
D、![]()
11、等体积的![]() 溶液和
溶液和![]() 溶液混合充分反应后,沉淀物和溶液中所含
溶液混合充分反应后,沉淀物和溶液中所含![]() 元素的物质的量相等,则
元素的物质的量相等,则![]() 与
与![]() 的溶液的物质的量浓度之比为
的溶液的物质的量浓度之比为
A、2:7 B、2:5 C、2:6 D、1:2
12、在浓度均为![]() 的
的![]() 和
和![]() 各100
各100![]() 溶液中,分别加入等质量的
溶液中,分别加入等质量的![]() 粉,充分反应后生成气体质量之比为3:4,则加入
粉,充分反应后生成气体质量之比为3:4,则加入![]() 粉质量为
粉质量为
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
13、将![]()
![]() 投入到一定量的
投入到一定量的![]() 中,
中,![]() 全部溶解,且收集到标况下的气体
全部溶解,且收集到标况下的气体![]() (
(![]() 和
和![]() ),则参加反应的
),则参加反应的![]() 为
为
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
14、据报道,美国正在研究用锌电池取代目前广泛使用的铅蓄电池,它具有容量大的特点,其电池反应为![]() ,其原料为
,其原料为![]() 粉,电解质溶液和空气,下列有关叙述中正确的是
粉,电解质溶液和空气,下列有关叙述中正确的是
A、![]() 为正极空气进入负极反应
B、正极反应为:
为正极空气进入负极反应
B、正极反应为:![]()
C、电解质溶液肯定不含强酸 D、负极发生还原反应
15、用惰性电极电解下列溶液,溶质质量不变但溶质质量分数增大的溶液是
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
16、将![]()
![]() 、
、![]()
![]() 和
和![]()
![]() 溶于水,配成100
溶于水,配成100![]() 混合液,用惰性电极电解一段时间后,在一极上析出
混合液,用惰性电极电解一段时间后,在一极上析出![]()
![]() ,此时另一极上收集到的气体的体积为(标况)
,此时另一极上收集到的气体的体积为(标况)
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
二、填空题(44分)
17、(8分)浓![]() 呈黄色原因是其中含 ,浓
呈黄色原因是其中含 ,浓![]() 呈黄色的原因是其中含
呈黄色的原因是其中含
;实验室在保存![]() 溶液时,需在溶液中加
溶液时,需在溶液中加![]() 屑,目的是 ,实验室在保存
屑,目的是 ,实验室在保存![]() 溶液时,需在溶液中加少量
溶液时,需在溶液中加少量![]() ,目的是
。
,目的是
。
18、(8分)把盛有48![]()
![]() 、
、![]() 混合气体的容器,倒置于水面上(同温,同压),液面稳定后容器内气体体积变为24
混合气体的容器,倒置于水面上(同温,同压),液面稳定后容器内气体体积变为24![]() ,则
,则
(1)原混合气体中,![]() 是
是 ![]() 。
。
(2)若在剩余的24![]() 气体中,通入6
气体中,通入6![]()
![]() ,待液面稳定后,容器内气体体积变为
,待液面稳定后,容器内气体体积变为
![]() 。
。
(3)若在24![]() 气体中,通入24
气体中,通入24![]()
![]() ,待液面稳定后,容器内气体体积变为
,待液面稳定后,容器内气体体积变为 ![]() 。
。
(4)若在原48![]() 的
的![]() 、
、![]() 气体中,通入
气体中,通入 ![]()
![]() ,倒置于水面上,气体会全部吸收。
,倒置于水面上,气体会全部吸收。
19、(4分)除去各组混合物中括号内的杂质
| 混合物 | 应加入的试剂 |
| (1) | |
| (2) |
20、(12分)某学生用标准![]() 滴定未知浓度氨水,下列操作会引起怎样的实验误差?(填“偏高”、“偏低”或“不变”)
滴定未知浓度氨水,下列操作会引起怎样的实验误差?(填“偏高”、“偏低”或“不变”)
(1)用酚酞作指示剂
(2)滴定前未用标准![]() 润洗酸式滴定管
润洗酸式滴定管
(3)中和过程中往锥形瓶中加一些水
(4)滴定前用氨水润洗锥形瓶
(5)滴定前标准![]() 是敞口放置的
是敞口放置的
(6)滴定结束时俯视滴定管刻度
21、(6分)近年我国首创铝――空气――海水为能源的新型电池。其电池总反应式为
![]()
(1)该电池的负极是 ,电极反应是 。
(2)电池工作时,正极附近PH (填“增大”、“减小”或“不变”)
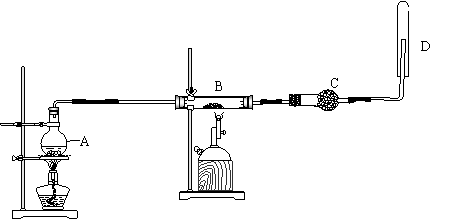 22、(6分)
22、(6分)![]() 与
与![]() 反应实验装置下图,实验时,在玻璃管B中放入还原性
反应实验装置下图,实验时,在玻璃管B中放入还原性![]() 粉和石棉绒的混合物,加热,并通入水蒸气,回答:
粉和石棉绒的混合物,加热,并通入水蒸气,回答:
(1)A仪器的名称 ,
在本实验中其作用是 。
(2)B处发生反应的化学方程式为 。
(3)C装置的作用是 。
(4)检验试管D中气体的方法是 。(填序号)
A、将带用余烬的木条伸入试管D中,木条复燃
B、将D试管口靠近火焰点火,发出爆鸣声
C、把氯气通入试管D中,发生爆炸
D、往试管D中加澄清石灰水,变浑浊
三、计算题(8分)
23、向![]() 铁粉和氧化铁的混合物中,加入稀
铁粉和氧化铁的混合物中,加入稀![]() 稀
稀![]() ,恰好反应并得到
,恰好反应并得到![]()
![]() (标态)。此时向反应后的溶液中滴入
(标态)。此时向反应后的溶液中滴入![]() 溶液,未见红色出现,求:
溶液,未见红色出现,求:
(1)原混合物中铁粉和氧化铁的的质量。
(2)原![]() 溶液的物质的量浓度。
溶液的物质的量浓度。
 高二第二学期开学考试化学答卷
高二第二学期开学考试化学答卷
一、选择题(16×3分=48分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | A | C | D | A | B | C | D | D |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | B | D | A | C | D | C | B | B |
二、填空题(44分)
17、(8分) Fe3+ 、 NO2 、
防止Fe2+被氧化 、 防止Fe3+水解
18、(8分)
(1) 12 (2) 16
(3) 6 (4) 18
19、(4分)
混合物 应加入的试剂
(1)![]() : 足量的Cl2
: 足量的Cl2
(2)![]() : 过量的NaOH溶液
: 过量的NaOH溶液
20、(12分)
(1) 偏低 (2) 偏高
(3) 不变 (4) 偏高
(5) 偏高 (6) 偏低
21、(6分)
(1) 园底烧瓶 、 生成水蒸气
(2) 3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
(3) 干燥H2
(4) B
三、计算题(8分)
23、
(1) m(Fe)=16.8g
m(Fe2O3)=32g
(2) c(H2SO4)=1mol・L-1