苹中2005―2006学年度第二学期期中考试
化 学(必修)试 卷
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32
第I卷(机读卷 共50分)
一、选择题(共25小题,每小题2分,每题均有四个选项,其中只有一个符合题意)
1、下列各组物质中,只用水就能鉴别的是
A.乙醇、乙酸 B.乙醛、乙酸 C.苯、己烯 D.苯、乙酸
2、可以用分液漏斗分离的混合液是
A.乙酸乙酯和水 B.乙醇和乙酸 C.苯和溴苯 D. 四氯化碳和溴
3、本世纪我国正在建设或即将动工的重大工程很多,其中“南水北调”、“西气东输”等重大工程与人们的生活密切相关,这里的“气”指的是天然气,天然气的产要成分是
A.CO B.石油气 C.H2 D.CH4
4、下列反应中,不属于取代反应的是
A.乙醇在一定条件下生成乙烯 B.甲烷跟氯气反应生成一氯甲烷
C.苯的硝化反应 D.乙酸乙酯的水解
5、做乙醛被Cu(OH)2氧化实验时,有以下步骤:①加入0.5mL乙醛溶液;②加入2%硫酸铜溶液4到5滴;③加入10% NaOH溶液2mL;④加热至沸腾。正确的操作顺序是
A.①②③④ B.③②①④ C.②③①④ D.①③②④
6、进行化学实验必须注意安全,下列说法正确的是
A.如果苯酚浓溶液沾到皮肤上,应立即用NaOH溶液洗涤
B.在点燃H2、CH4等易燃性气体前,必须检验气体的纯度
C.实验室制取乙烯时,直接加热烧瓶使液体温度迅速上升到170 ℃
D.不慎将浓硫酸沾到皮肤上,要立即用大量水冲洗
7、下列物质能使淀粉溶液变为蓝色的是
A.碘化钾溶液 B.碘酒 C.氯水 D.溴水
8、下列过程不可逆的是
A.蛋白质的盐析 B.蛋白质的变性 C.氯化铁的水解 D.酯的酸催化水解
9、某有机物的结构为CH2=CH―COOH,该有机物不可能发生的化学反应是
A.银镜反应 B.加聚反应 C.加成反应 D.酯化反应
10、人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,主要由于维生素C具有
A.酸性 B.碱性 C.氧化性 D.还原性
11、变质的油脂有难闻的哈喇味,这是因为发生了
A.氧化反应 B.加成反应 C.取代反应 D.水解反应
12、下列物质在一定条件下能发生水解的是
①淀粉 ②葡萄糖 ③蔗糖 ④纤维素 ⑤油脂 ⑥蛋白质 ⑦麦芽糖
A.全部 B.①②③④⑤⑥ C.①③④⑤⑥ D.①③④⑤⑥⑦
苹中2005―2006学年度第二学期期中考试
化 学(必修)试 卷
第II卷(非机读卷 共50分)
二、填空题(共29分)
26、(3分)已知①C60,②13C,③CH3-CH2-CH3,④ ![]() ,⑤12C,⑥金刚石,其中互为同位素的是 (填序号,下同),互为同系物的是 ,互为同素异形体的是 。
,⑤12C,⑥金刚石,其中互为同位素的是 (填序号,下同),互为同系物的是 ,互为同素异形体的是 。
27、(4分)乙醇俗称 ,其分子中的官能团是 基,官能团的电子式是 。 体积分数为75%的乙醇溶液常作医用消毒剂,其消毒原理是它能使细菌的蛋白质 而杀死细菌。
28、(4分)浓H2SO4具有①酸性,②强氧化性,③吸水性,④脱水性。根据题意填空(填序号):
(1) 将盛有浓硫酸的容器敞口放在空气中一段时间后,其质量会 (填“增加”、“减少”或“没有变化”),是因为它具有________;
(2)加热乙醇和浓H2SO4的混合物可制得乙烯,是利用了浓硫酸的_____和催化作用;
(3)常温下可以用铁制容器贮运浓H2SO4,是因为浓H2SO4有___________。
29、(5分)现有5种有机物:①CH2=CH2 ②CH3CH2OH ③CH3CHO ④CH3COOH ⑤CH3COOCH2CH3,请按下列要求填空(填序号)。
(1)既能发生加成反应,又能发生聚合反应的是 。
(2)能发生消去反应的是 。 (3) 能发生银镜反应的是 。
(4)能发生水解反应的是 。 (5) 具有酸性且能发生酯化反应的是 。
30、(5分)蛋白质、淀粉、脂肪是三种重要的营养物质,其中 不是天然有机高分子化合物;这三种物质水解的最终产物分别是:蛋白质 、淀粉 、脂肪 和 。
31、(3分)写出下列反应的化学方程式:
(1)实验室制乙烯
(2)蔗糖水解
(3)用硬脂酸甘油酯制取硬脂酸
32、(5分)现有甲、乙、丙三种中学化学常见物质,均由X、Y、Z元素中的两种或三种组成。请回答:
(1)甲物质含有两种元素,在标准状况下为气态,实验测知甲在标准状况下的密度为0.714g/L。甲的分子式为 。
(2)乙物质含有三种元素,常温下为无色液体,能跟金属反应放出氢气。经测定,乙中X、Y、Z三种元素的质量比为3∶12∶8。乙的结构简式为 。乙与钠反应的方程式为 。
(3)在一定条件下,乙可转化为丙,丙和新制氢氧化铜共热,有红色沉淀生成。乙转化为丙的化学方程式 ,丙和新制氢氧化铜共热的化学方程式 。
三、实验题(共17分)
33、(4分)写出鉴别下列各组物质所用的试剂:
① CH3COOH和CH3COOC2H5________________; ② 己烯和苯____________________;
 ③ 煤油中含水_____________________ ;④ 乙烷和乙炔__________________。
③ 煤油中含水_____________________ ;④ 乙烷和乙炔__________________。
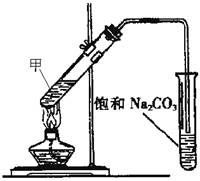
34、(5分)实验室用右图所示装置制取乙酸乙酯。
(1) 试管甲中装入的是 、浓硫酸和冰醋酸。
(2)装置中通有蒸气的导管要插在饱和Na2CO3溶液的液面上,不能插入溶液中,目的是: _____ ______;
(3)饱和Na2CO3溶液的作用是:___ __。
(4)实验生成的乙酸乙酯,其密度比水_______(填“大”或“小”);
(5)分离乙酸乙酯和饱和Na2CO3溶液所需要的主要仪器是:_______ _。
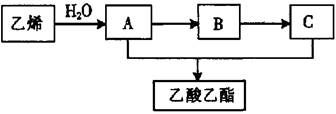 |
35、(8分)以乙烯为原料制取乙酸乙酯的过程如下图所示:
回答下列问题:
(1)A的结构简式为_________________,B的名称为________________。
(2)写出实现下列转化的化学方程式,并注明反应类型。
乙烯制取A, B→C, A+C→乙酸乙酯。
四、计算题(4分)
36、L-多巴是一种有机物,它可用于帕金森综合症的治疗。这种药物的研制获得了近两年的诺贝尔化学奖、生理医学奖。经分析,该物质的相对分子质量约为甲烷的12.3倍,其组成元素C、H、O、N的质量比为108∶11∶64∶14。试通过计算求出L-多巴的分子式。