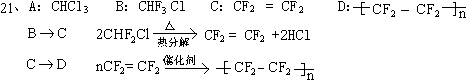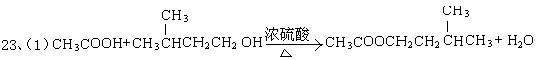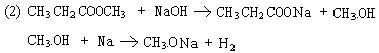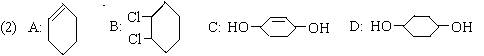| 第二学期中段考试 高二化学试卷 第一卷 (共67分) 一. 选择题(本题包括5小题,每小题3分,共15分。每小题只有一个选项符合题意) 1、下列有机物的说法中正确的是( ) A、 A、 凡是含碳元素的化合物都属于有机物 B、 B、 易溶于汽油、酒精、苯等有机溶剂中的物质一定是有机物 C、 C、 所有的有机物都很容易燃烧 D、D、 大多数有机物聚集时形成分子晶体 2、CH3CH(C2H5)CH(CH3)2 的名称是( ) A、1,3―二甲基戊烷 B、2―甲基―3―乙基丁烷 C、3,4―二甲基戊烷 D、2,3―二甲基戊烷 3、下列变化过程中,不包含化学变化的是( ) ①煤的干馏 ②纯碱晶体风化 ③用P2O5干燥潮湿的氢气 ④将重油减压分馏得凡士林 A、①②③ B、①②④ C、②④ D、④ 4、下列变化肯定属于不可逆的是( ) A、电离 B、水解 C、盐析 D、蛋白质变性 5、下列有机物各取1moL完全燃烧,消耗O2最少的是( ) A、乙烯 B、乙炔 C、乙醛 D、乙酸 二.选择题(本题包括13小题,每小题4分,共52分。每小题有一个或两个选项符合题意。 若正确答案只包括一个选项,多选时该题为0分,若正确答案包括两个选项,只选了一个且 正确的给2分,选两个都正确的给4分,但只要选错一个,该小题就为0分。) 6、 两种气态烃组成的混合气体0.1mol完全燃烧得到7.04g CO2和3.6g H2O,下列说法正确的是( ) A、一定有甲烷 B、一定是甲烷和乙烯 C、一定没有乙烷 D、一定有乙炔 7、 下列关于蛋白质的叙述中,不正确的是 A、 蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,如再加水也不溶解 B、 蛋白质燃烧时有烧焦羽毛气味 C、 重金属盐能使蛋白质变性,所以吞服“钡餐”会引起中毒 D、 浓硝酸溅在皮肤上,能使皮肤呈黄色是由于蛋白质和浓硝酸发生了颜色反应
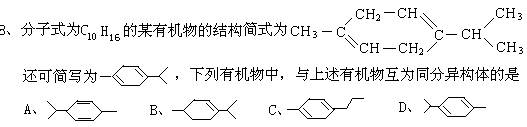
A、维生素A的一个分子中含有三个双键 B、维生素A在一定条件下可发生加成反应 C、维生素A的一个分子中含有30个氢原子 D、维生素A具有环己烷的结构单元 10、能说明苯分子苯环的平面正六边形结构中碳碳键不是单双键交替排列的事实是 A、 苯的一元取代物没有同分异构体 B、苯的邻位二元取代物没有同分异构体 C、苯的间位二元取代物没有同分异构体 D、苯的对位二元取代物没有同分异构体 11、下列试剂中,能将乙醇、淀粉溶液和苯三种无色液体鉴别开来的是 A、钠 B、新制氢氧化铜 C、溴水 D、碘水 12、由以下五种官能团两两结合而形成的化合物,能与NaOH溶液反应的共有 ①―CH3 ②―OH ③―C6H5 ④―CHO ⑤―COOH A、3种 B、4种 C、5种 D、6种 13、分子式为C4H8O2的酯,水解后得到醇A和羧酸B,将A氧化最终可得羧酸C,若C可以 发生银镜反应,则分子式为C4H8O2的酯的结构简式为 A、 HCOOCH2CH2CH3 B、CH3OOC CH2 CH3 C、CH3COOCH2CH3 D、HCOOCH(CH3)2 14、两种气态烃的混合气体,在同温同压下占有的体积是等质量H2体积的1/12,此两种烃可能是 A、C2H6和C3H6 B、CH4和C2H2 C、C2H6和C3H6 D、CH4和C4H8 15、有下列物质:①碘水 ②银氨溶液 ③NaOH溶液 ④稀硫酸 ⑤浓硫酸,在进行淀粉的水解实验(包括水解产物及水解是否完全的检验)时,除淀粉外,还需使用上述试剂或其中的一部分,判断使用的试剂及其先后顺序为: A、①④②③ B、④①③② C、⑤①③② D、①⑤②③ 16、下列物质,既能和稀H2SO4又能和NaOH溶液反应的是
A、①②③ B、④⑤ C、①④ D、①②③④
A、消去、加聚 B、水解、缩聚 C、氧化、缩聚 D、水解、加聚
A、①④ B、②⑤ C、②⑥ D、③④
第二卷(共83分) 三. 三. 填空题 19、(16分)为了除去下列物质中所含的杂质(括号内),将所加试剂和分离方法填入下表。
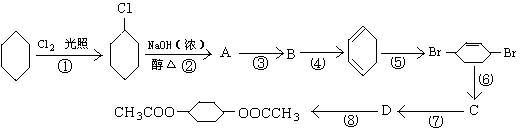
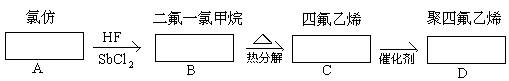
20、(12分)今有下列有机物:A、C2H5OH B、C6H5OH C、C2H5ONO2 D、葡萄糖 E、CH2=CH―CH=CH2 F、淀粉 G、蔗糖 H、麦芽糖 I、CH3COOCH3 J、CH2=CH―CH2―COOH (1) 能用来杀菌的是____________(填编号,以下同) (2) 能和NaOH溶液反应的是______________________ (3) 常温下和溴水反应的是_______________________ (4) 能和银氨溶液反应的是_________________________ (5) 属于高分子化合物的是______________________ (6) 能水解最终生成一种有机物的是___________________ 21、(10分)聚四氟乙烯的耐热性和化学稳定性都超过了一切塑料,甚至在王水中也不发生变化,故号称“塑料王”,在工业上有着广泛、重要的用途。按照下面所示的合成路线,试在方框中填写合适的化合物的结构简式: 写出下列化学方程式:
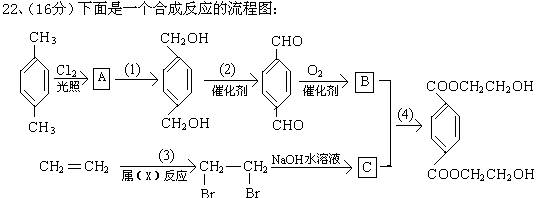
写出: ① 中间产物的结构简式 A___________ B_____________ C______________ ② 反应试剂(1)__________ (2)__________ (3)__________ (4)_____________ ③ 反应类型X是_____________反应
合成乙酸异戊酯,其实验装置示意图(见右图)。操作过程如下: 异戊醇和20Ml(0.35 m01)冰醋酸,最后小心加入5mL浓H2S04, 振荡,使其不再分层。②:在烧瓶上安装水冷凝管,后加热装置 1小时冷却至室温。③:把烧瓶内混合液倒人盛有饱和Na2C03溶液 的锥形瓶中,振荡后静置。④:把③中水层分离出后,再用蒸馏水 洗涤有机层,并将洗涤后的水层分离出。⑤将分离的有机层转移到 另一锥形瓶内,加入无水MgS04或Mg(N03)2处理。最后将处理后的 有机层经135℃―143℃蒸馏,即得乙酸异戊酯产品。试回答以下问题: (1) 写出乙酸和异戊醇合成乙酸异戊酯的化学方程式_____________________________ _________________________________。其中浓H2SO4作用是_______________________, 烧瓶内碎瓷片的作用是_________________________。 (2) 水冷凝器的作用是_____________________,冷凝管的a口是冷却水的__________(进口、 出口) (3) 乙酸和异戊醇物质的量之比为0.35:0.14大于1:1,其原因是__________________________ __________________________。 (4) ③中饱和碳酸钠的作用________________________________________, ⑤中无水MgS04或Mg(N03)2的作用是:_____________________________。
四、计算题 24、(3分)某烃的含氧衍生物R为4.6g ,完全燃烧后生成0.2mol CO2和0.3mol水。并已知它的蒸汽密度是相同 条件下H2密度的23倍;它能跟金属钠反应产生H2。通过计算填空:(不需写出计算过程) (1) (1) R的分子量是______________ (2) (2) R的分子式是_______________ (3) R的结构简式是__________________ 25、(10分)有饱和一元脂肪酸和一元脂肪醇形成的酯A。已知:①燃烧2.2g A可生成4.4g CO2和1.8g水; ②1.76g A与50mL0.5mol/L的NaOH溶液共热后,为了中和剩余的碱液,消耗0.2mol/L的盐酸25mL;③取A水 解后所得的醇B 0.64g,跟足量钠反应时,标准状况下放出224mL氢气。求: (1)(1) A的相对分子质量、分子式、结构简式(要求写出计算过程) (2)(2) 写出下列反应的化学方程式: 五、附加题 26、(12分)从环己烷可制备1,4―环己二醇的二醋酸酯。下面是有关的8步反应(其中所有无机产物都已略去):
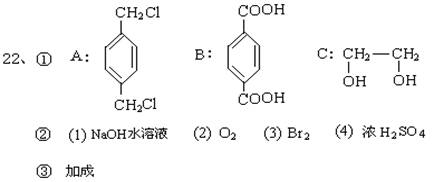
(1) (1) 其中有3步属于取代反应、2步属于消去反应、3步属于加成反应。反应①、____和_____属于 (2) 取代反应。 (3) (2) 写出下列化合物的结构简式: A______________ B_____________ C______________ D______________
(3) 反应④所用试剂和条件是___________________________
南海一中2000―2001学年度第二学期中段考试 高二化学试卷(参考答案) 一、一、 选择题
二、二、 填空题 19、
20、(1)AB (2)BCIJ (3)BEJ (4)DH (5)F (6)FH
催化剂、吸水剂:防止爆沸
(2)冷凝蒸气;进口 (3)保证乙酸过量,使平衡向右移动,反应更加彻底 (4)除去乙醇和异戊醇、减小乙酸异戊酯的溶解度; 吸水、干燥 24、(1)46 (2)C2H6O (3)CH3CH2OH 25、(1)88、 C4H8O2、 CH3CH2COOCH3 26、(1)①⑥⑦ (3)NaOH(浓)、醇、加热 |
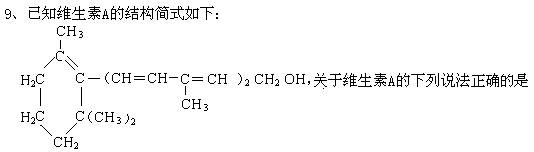
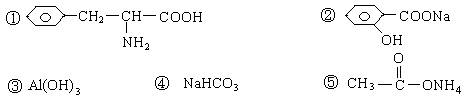
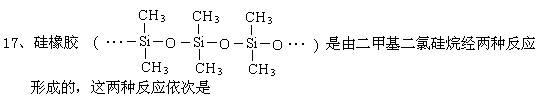


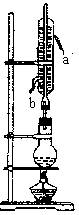 23、(16分)实验室可用冰醋酸 (CH3COOH)和异戊醇
23、(16分)实验室可用冰醋酸 (CH3COOH)和异戊醇