九校联合体2005-2006学年度第二学期期中联考
高二年级化学试题
第I卷
已知元素的相对原子质量:Ag-108 C-12 H-1 O-16 N-14
| 一、选择题(单选题,每一小题3分,共60分) | ||||||||
| 1、下列说法不正确的是( ) ①有机物与无机物无明显的界限,但在组成和性质上有些不同之处。 ②有机物中不一定含有碳元素。 ③有机物中不一定含有氢元素。 ④科学家最早由尿素合成了氰酸铵,实现了有机物与无机物之间的相互转化。 ⑤有机物中的碳原子与碳原子之间不仅能形成C-C、C=C、C≡C,还能形成更复杂的共价键。 ⑥碳原子间可通过形成离子键、共价键等形成有机化合物 | ||||||||
| A、①②③ | B、②④⑥ | C、⑤⑥ | D、④⑤⑥ | |||||
| 2、下列反应中属于取代反应的是( ) | ||||||||
| A、甲烷燃烧 | B、用甲烷制氯仿 | C、用甲烷制炭黑 | D、庚烷裂化 | |||||
| 3、下列物质的主要成份属于烃类的是( ) | ||||||||
| A、石蜡 | B、福尔马林 | C、氯仿 | D、煤 | |||||
| 4、某有机物分子式为C5H4F3Cl,就其结构来说,除C-C外该有机物不可能是( ) | ||||||||
| A、只含一个双键的链状化合物 | B、含有两个双键的链状化合物 | |||||||
| C、含一个双键的单环化合物 | D、含一个三键的链状化合物 | |||||||
| 5、a mol | ||||||||
| A、1:1 | B、1:2 | C、2:3 | D、3:2 | |||||
| 6、已知氯元素有两种稳定的同位素35Cl、37Cl,由此判断氯气与乙烷取代反应形成的二氯乙烷有( )种 | ||||||||
| A、2 | B、4 | C、6 | D、8 | |||||
| 7、在相同温度下,甲酸和乙酸都是弱酸,当它们的浓度均为0.10mol・L-1时,甲酸中的c(H+)约为乙酸中c(H+)的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10mol・L-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知( ) | ||||||||
| A、a的浓度必小于乙酸的浓度 | B、a的浓度必大于乙酸的浓度 | |||||||
| C、b的浓度必小于乙酸的浓度 | D、b的浓度必大于乙酸的浓度 | |||||||
| 8、草酸是二元弱酸,草酸氢钾溶液呈酸性,在0.1 mol・L-1KHC2O4溶液中,下列关系正确的是( ) | ||||||||
| A、c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-) | ||||||||
| B、c(HC2O4-)+c(C2O42-)=0.1mol・L-1 | ||||||||
| C、c(C2O42-)< c(H2C2O4) | ||||||||
| D、c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-) | ||||||||
| 9、某中草药一种成份的结构简式如下:
下列说法错误的是( ) | ||||||||
| A、1mol此物质与溴水和H2反应的最大用量分别是6mol、10mol。 | ||||||||
| B、此物质可以与金属钠反应。 | ||||||||
| C、此物质可以与Na2CO3溶液反应放出CO2 | ||||||||
| D、此物质能发生加聚反应 | ||||||||
| 10、下列除杂的方法正确的是( ) | ||||||||
| A、除去NaCl固体中少量的I2,加入CCl4后静置分液 | ||||||||
| B、除去苯中少量的苯酚,加入足量的NaOH溶液,充分反应后静置分液 | ||||||||
| C、除去KCl溶液中少量AlCl3,加入足量KOH溶液过滤 | ||||||||
| D、除去苯中的少量苯酚,加入足量溴水后振荡、静置、过滤 | ||||||||
| 11、 | ||||||||
| A、此反应属于氧化-还原反应 | B、此反应属非氧化-还原反应 | |||||||
| C、反应后溶液pH不变 | D、反应后溶液pH变大 | |||||||
| 12、关于苯酚的叙述正确的是( ) | ||||||||
| A、苯酚的水溶液能使石蕊试液变红 | ||||||||
| B、苯酚的浓溶液对皮肤有很强的腐蚀性 | ||||||||
| C、苯酚溶液中加少量稀溴水,很快就生成白色沉淀 | ||||||||
| D、苯酚不能参加聚合反应形成高分子化合物 | ||||||||
| 13、能一次鉴别CH3COOH、C2H5OH、 | ||||||||
| A、H2O | B、Na2CO3溶液 | C、pH试纸 | D、石蕊试纸 | |||||
| 14、分子式为C8H16O2的有机物A在酸性条件下,水解生成有机物B、C,且C在一定条件下氧化成B,则有机物A的可能结构有( ) | ||||||||
| A、2种 | B、3种 | C、4种 | D、5种 | |||||
| 15、甲苯和甘油组成的混合物中,若碳元素的质量分数为60%,则氢元素的质量分数( ) | ||||||||
| A、5% | B、8.7% | C、17.4% | D、无法计算 | |||||
| 16、已知碳、碳单键可以绕键轴自由旋转,某烃结构简式如下图所示,下列说法正确的是( ) | ||||||||
| A、该烃的分子式为C16H24 | ||||||||
|
| ||||||||
| C、该烃属于苯的同系物 | ||||||||
| D、该烃苯环上只有一种一氯代烃 | ||||||||
| 17、下列每组物质能用分液漏斗分离的是( ) | ||||||||
| A、甘油和水 | B、已烷和水 | C、乙醇和乙酸 | D、硝基苯和苯 | |||||
| 18、化合物A为 | ||||||||
| A、NaOH | B、NaHSO4 | C、NaHCO3 | D、Na2CO3 | |||||
| 19、某饱和一元醛和酮的混合物共3克,跟足量的银氨溶液反应后可还原出16.2克银。下列说法正确的是( ) | ||||||||
| A、混合物中一定有甲醛 | B、混合物中可能有乙醛 | |||||||
| C、醛、酮质量之比为4:5 | D、酮一定为丙酮 | |||||||
| 20、已知乙二醇脱水形成一系列链状高分子化合物H | ||||||||
| A、此反应是加聚反应 | ||||||||
| B、此类化合物分子都是直线型分子 | ||||||||
| C、此类分子的相对分子质量的通式为44n+18 | ||||||||
| D、此类化合物跟乙二醇互为同系物 | ||||||||
 九校联合体2005-2006学年度第二学期期中联考
九校联合体2005-2006学年度第二学期期中联考
高二年级化学试题
请将第I卷选择题的答案填入下列对应的空格内。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
第II卷
二、填空:
21、(2分)有6种微粒①Cl- ②OH- ③-OH ④-NO2 ⑤NO2 ⑥CH3+
(1)其中能和CH3CH2- 结合形成有机物分子的微粒有 (填序号)
(2)其中能和C6H5+结合生成有机物分子的微粒有 (填序号)
22、(6分)已知聚乙炔薄膜是由乙炔加聚得到
(1)聚乙炔的结构简式
(2)一种与聚乙炔具有相同最简式的有机物A、其相对分子质量为52,且分子具有多种同分异构体。
① 它的一种链式结构的同分异构体结构简式为CH2=CH-C≡CH,该分子
中所有原子是否在同一平面上 ,所有碳原子是否在一条直线
上 。(填“是”或“否”)
② 它的另一种同分异构体的每个碳原子均达到饱和,空间构型中碳碳键之间夹角都相等,每个碳都直接跟其它三个碳原子相连,则碳碳键之间夹角是 ,它跟Cl2发生取代反应能得到的有机取代产物有__________种(填数字)。
(3)另一种有机物芳香烃B跟A最简式相同,相对分子质量是A的两倍,该分
子的结构简式为 。
23、(4分)已知温度一定时,下列各微粒的电离能力,H2SO3>H2CO3>HSO![]() >
>![]() >HCO
>HCO![]() 。(1)写出将少量SO2通入苯酚钠溶液中,发生反应的离子方程式
。(1)写出将少量SO2通入苯酚钠溶液中,发生反应的离子方程式
(2)现有温度、浓度均相同的①Na2CO3 ②Na2SO3 ③NaHSO3 ④![]() ⑤NaHCO3溶液,其PH从大到小顺序为 (填序号)。
⑤NaHCO3溶液,其PH从大到小顺序为 (填序号)。
24、(4分)高分子化合物单体为O=C=N-R-N=C=O和多元醇,其高聚物结构如图
![]()
(1)由上述二异氰酸酯和多元醇的反应属于 反应。(填“加聚”或“缩聚”)
(2)写出由 和1,3-丙二醇,生成的高聚物的结构简式为
________________________________________________________。
25、(8分)分别取等质量甲烷,A(某饱和一元醇),B(某饱和一元醛),C(饱和一元酸),若它们完全燃烧分别生成物质的量相同的CO2,则
(1)A的分子式为 ,B的分子式为 ,C的分子式
为 。
(2)试推导出符合上述条件时,CH4、A、B、C等分子中,氢原子数与碳、氧原子数的关系式为________________(用n表示碳原子数,m表示氧原子数,x表示氢原子数)。
26、(10分)某芳香烃A有如下转化关系:

按要求填空:
(1)写出反应①的反应类型_____________;
(2)写出A和F的结构简式:A 、F ;
(3)写出反应③和⑤的化学方程式:
③________________________________________________________
⑤________________________________________________________
三、实验题(8分)
27、为了验证苯与液溴反应的原理,并检验产物的性质,设计了某实验方案如图所示。
 已知苯在铁作催化剂的条件下与液溴反应剧烈并放出大量热,根据题意,试填写下列空白。
已知苯在铁作催化剂的条件下与液溴反应剧烈并放出大量热,根据题意,试填写下列空白。
(1)实验开始时,先关闭K2,开启K1以及分液漏斗活塞,滴加苯和液溴的混合液,
反应开始后,I中出现的现象是__________________________________。
(2)图中冷凝管左低右高的原因是_________________________________________。
(3) II中小试管的作用是_______________________________________,III中球形管
的作用___________________________________________。
(4) 反应一段时间后,关K1和漏斗活塞,开启K2,IV中的水会自动流进I中,产
生此种现象的原因是_______________________________________,将I中反应
后的混合物倒入水槽中,用________________溶液洗涤,然后经分液操作后得到较纯净的溴苯。
(5) 苯跟溴的反应属于____________________________(填反应类型)反应的化学方程
式为___________________________________________。
四、计算题:(8分)
28、平均摩尔质量为9.6g/mol的C2H4、C2H2、H2的混合气体,一定条件下充分反应后,所得混合气体的平均摩尔质量为16g/mol.
求:①反应后的气体的组成,以及各气体体积分数。
②原混合气体中各组分的体积分数。
答案及评分标准
一、选择题(每小题3分共60分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | B | B | A | A | B | C | A | D | C | B |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | B | B | B | A | B | B | B | C | A | C |
二、填空题:
21、(2') (1) ③④ (1分)
![]() (2) ①② (1分)
(2) ①② (1分)
22、(6') .(1) (1分)
![]() (2) ① 是 否
(各1分,共2分)
(2) ① 是 否
(各1分,共2分)
② 60° 4 (各1分,共2分)
![]() (3)
(3) ![]() (1分)
(1分)
23、(4') (1) (2分)
(2)①>④>②>⑤>③
24、(4') (1)加聚 (2分)
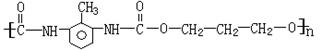 |
(2) (2分)
25、(8') (1)A:C9H20O B:C8H16O C:C16H32O2 (各2分,共6分)
(2)x=4m-16n (2分)
26、(10分)(1)加成 (2分)
(2)A:![]() F:
F: (4分)
(4分)
(3)③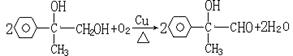 (2分)
(2分)
 |
⑤ (2分)
27、(1)大量红棕色气体出现 (1分)
(2)冷凝回流挥发的溴和苯 (1分)
(3)除去HBr中Br2; 防止倒吸 (各1分,共2分)
(4)HBr极易溶于水,使I中压强低于大气压; (1分)
NaOH (1分)
![]() (5)取代
(1分)
(5)取代
(1分)
(1分)
28、①该反应后气体为C2H6、H2 (2分)
C2H6 50% H2 50% (各1分,共2分)
②C2H4 20% C2H2 10% H2 70% (共4分,过程2分,结果2分)
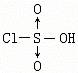 即Cl-SO3H称为氯磺酸是一种强酸,它和甲酸能发生如下反应:HCOOH+ClSO3H=CO↑+HCl+H2SO4,下列说法正确的是( )
即Cl-SO3H称为氯磺酸是一种强酸,它和甲酸能发生如下反应:HCOOH+ClSO3H=CO↑+HCl+H2SO4,下列说法正确的是( )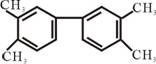 B、分子中至少有11个碳原子处于同一平面上
B、分子中至少有11个碳原子处于同一平面上