华南师大附中第一学期期末考试
高二化学试题
(时间:90min)
相对原子质量:O:16 H:1 Fe:56 N:14 Mg:24 Al:27
Cl:35.5 Na:23 C:12 Si:28
第Ⅰ卷(共17题)
一、选择题(每小题只有一个正确答案,每小题3分,共36分)
1、下列物质属于混合物的是
①石油 ②煤 ③ 聚丙烯 ④电石气
A、①④ B、①②③ C、②④ D、①②③④
2、可将苯与甲苯区分开的试剂是
A、酸性KMnO4溶液 B、溴水
C、NaOH溶液 D、水
3、下列各组物质中为同分异构体的是
A、1H与2H B、O2与O3 C、乙烯与丙烯 D、正丁烷与异丁烷
4、下列属于物理变化的是
A、干馏 B、分馏 C、裂化 D、裂解
5、下列各组物质中一定互为同系物的是
A、CH4、C3H8 B、C2H4、C3H6 C、C2H2、苯 D、C2H2、C4H6
6、不用其它试剂则不能鉴别的溶液是
A、AlCl3、NaOH B、Na2CO3、HCl
C、MgCl2、FeCl3 D、KAl(SO4)2、MgSO4
![]()
![]()
![]()
![]()
![]()
![]() 7、合成高聚物[CH―CH2―CH2―CH=CH―CH2]
n的单体是
7、合成高聚物[CH―CH2―CH2―CH=CH―CH2]
n的单体是
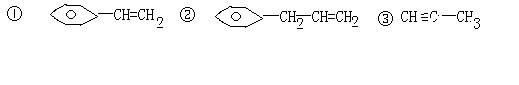 |
④ CH3―CH=CH―CH3 ⑤ CH2=CH―CH=CH2
A、①⑤ B、①④ C、②③ D、②⑤
8、下列物质的分子中所有原子不可能共面的是
A、丙烯 B、乙烯 C、乙炔 D、苯
9、下列离子在溶液中能大量共存在是
A、Fe3+、S2―、H+ B、SiO32―、OH―
C、Fe2+、H+、NO3― D、AlO2―、H+
10、下列离子方程式正确的是
A、FeCl2溶液中通入Cl2:Fe2++ Cl2=2Cl― + Fe3+
B、Al投入NaOH溶液中:Al+ OH― +H2O= AlO2― + H2↑
C、Fe投入盐酸中:2 Fe+6 H+=2 Fe3++3 H2↑
D、Na2 SiO3溶液中加入盐酸:SiO32― +2 H+ + H2O= H4SiO4↓
11、常温下把Na、Mg、Al各0.1mol分别投入到100mL0.1mol/L的盐酸中,在相同条件下产生H2最多的是:
A、Na B、Mg C、Al D、一样多
12、56克Fe粉投入500g稀HNO3中,两者恰好反应,溶液增重26克,则反应后溶液中的金属阳离子是:
A、只有Fe3+ B、只有Fe2+ C、Fe2+和Fe3+ D、无法确定
二、选择题(每小题有一个或两个选项符合题意,每小题4分,共20分)
13、下列物质中属于苯的同系物的是:
![]()
14、下列各组物质中分别滴入过量的NaOH溶液,现象相同的是:
A、AlCl3溶液与MgCl2溶液 B、FeCl2溶液与FeCl3溶液
C、SiO2粉末与Al2O3粉末 D、NH4Cl浓溶液与水玻璃
15、分子式为C8H10的芳香烃,其苯环上的一氯代物有三种,则该烃的结构简
式可能是:
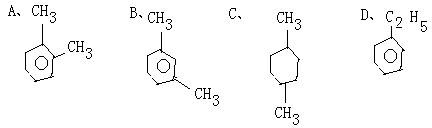
16、某气态烷烃和气态烯烃以2:3混合共50mL,完全燃烧恰好需205mLO2,
则该烷烃和烯烃分别为:
A、甲烷与乙烯 B、乙烷与丙烯 C、丙烷与丙烯 D、正戊烷与1―戊烯
17、下列各组物质以任意比例混和,只要混和物的物质的量一定,则充分燃烧
产生CO2的量也为定值的是:
A、C2H2与苯蒸气 B、C2H2与C2H4
C、CH4与C3H4 D、已烷与1―已烯
第Ⅱ卷(共10题)
一、二、选择题(共56分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | ||||||||||||
| 题号 | 13 | 14 | 15 | 16 | 17 | |||||||
| 答案 |
三、填空题(共17分)
18、现有(a)已烷(b)乙烯(c)苯(d)甲苯(e)乙炔六种物质,其中:(填
字母序号)
(1)常温下呈液态的烃为____________________________________________;
(2)既不能与溴水反应,也不能使酸性KMnO4溶液褪色的烃为___________;
(3)不能和H2发生加成反应的是__________________________。
19、向FeCl3溶液中加入适量碘化钾,振荡后再加入苯,再振荡后静置,苯层显_________色,反应的离子方程式为______________________________。
![]()
![]() 20、有机物CH3―CH―CH2―CH―CH3的名称是__________________________.
20、有机物CH3―CH―CH2―CH―CH3的名称是__________________________.
CH3 CH2―CH3
21、下列反应属于取代反应的是___________,属于加成反应的是__________.
(1)实验室制乙烯;(2)苯的溴代;(3)苯的硝化;(4)炔烃使溴水褪色.
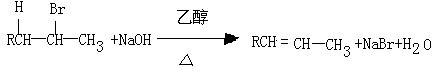
22、在有机反应中,反应物相同而条件不同得到不同的主要产物,下式中的R代表烃基:
如:
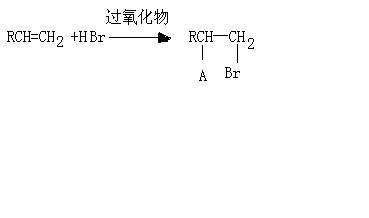
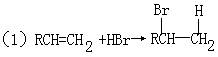
(请注意:H和Br所加成的位置)
(2)
写出实现下列转变的各步反应的化学方程式,特别注意写明反应条件:
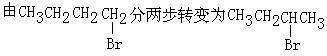
反应方程式:
①___________________________________________________;
②___________________________________________________。
23、有A、B、C、D、E五种烃,具有下列性质:①各取0.1mol分别充分燃烧,其中B、C、E燃烧所得的CO2均为4.48L(标准状况),A和D燃烧所得的CO2都是前三者的3倍;②在适宜条件下,A、B、C都能跟氢气发生加成反应,其中A可以转化为D、B可以转化为C,C可以转化为E;③B和C都能使溴水或酸性KmnO4溶液褪色,而A、D、E无此性质;④用铁屑作催化剂时,A可与溴发生取代反应。判断A、B、C、D、E各是什么物质,写出结构简式.
A__________B___________C___________D____________E___________。
四、实验题(共15分)
24、用化学方法除去下列物质中混有的杂质(括号内),分别填入将选用的试剂和反应方程式:
(1)FeCl2溶液(FeCl3):______________,________________________________:
(2)乙炔(硫化氢):_________,_______________________________________。
25、(1)实验室制取甲烷时使用的实验装置与制取_________________气体的实验装置相同。制甲烷的化学方程式为____________________________________。
(2)实验室制取乙烯时,浓硫酸的作用是_______________________________,
反应装置中要放入碎瓷片,原因是______________________________________。
(3)实验室蒸馏石油的装置中,温度计水银球的位置应在____________________处,冷凝管的_____________端注入冷水。
 (4)选用下图所示装置做苯的硝化实验,回答下列问题:
(4)选用下图所示装置做苯的硝化实验,回答下列问题:
a. 写出反应方程式:
_____________________________________________;
b. 此反应在50~600C下发生,在图中画出温度计的正确位置.
c. 长玻璃管的作用____________________________________。
五、计算题(共12分)
26、某气态烷烃和一气态单烯烃组成的混合气体,在同温同压下对氢气的相对密度为13。标准状况下,此混合气体112L,通入足量溴水中,溴水增重70g 。求:
(1)混合气体中的气态烷烃是什么?
(2)混合气体中两种气体的物质的量之比是多少?
(3)混合气体中单烯烃的分子式是什么?写出其结构简式。
27、由铁、硅、铝组成的混合物a mol,与足量稀H2SO4反应,在标准状况时可产生22.4bL氢气;若再将a mol上述混合物与足量NaOH溶液反应,在标准状况时也产生等量的氢气,问a mol混合物中铝有多少mol?
1999――2000学年第一学期期末考试化学答案
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| B | A | D | B | A | D | A | A | B | D | A | A |
| 13 | 14 | 15 | 16 | 17 | |||||||
| A | C | BD | B | BD |
18.(1)a c d
(2)a c
(3)a
19.紫红 2Fe3++2I― =2Fe2+ +I2
20.2.4- = 甲基已烷
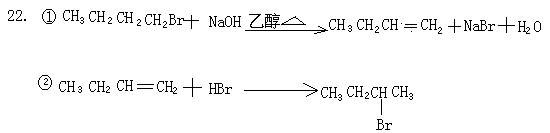
21.2 . 3;4
 |
24.(1)Fe Fe+2FeCl3=2FeCl2
(2)NaOH H2S+2NaOH=Na2S+2H2O

(2)催化剂、脱水剂;防止混合液受热爆沸
(3)蒸镏烧瓶支管口; 下
b 温度计水银球没入烧杯内热水中
c 冷凝、回流
26.(1)甲烷 (2)3∶1
(3)CH2=CHCH2CH3 CH3-CH=CH-CH3 CH3-C= CH2
27.![]()