高三化学上学期第三阶段考卷
考试时间:120分钟 满分:100分 命题:郑少林
第Ⅰ卷(共46分)
相对原子质量: H—1 C—12 O—16
一、选择题(本题共46分,每小题2分,每题只有一个正确选项)
1、以下反应最符合绿色化学原子经济性要求的是 ( )
A、乙烯聚合为聚乙烯高分子材料 B、甲烷与氯气制备一氯甲烷
C、以铜和浓硝酸为原料生产硝酸铜 D、用SiO2制备高纯硅
2.根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是 ( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A、3 B、4 C、5 D、6
3.下列叙述不正确的是( )
A.石油主要是由各种烷烃、环烷烃、芳香烃组成的混合物,没有固定的熔点
B.聚乙烯是有机高分子化合物,加热至某一温度,则可全部熔化
C.同质量的乙烯和聚乙烯燃烧后生成的CO2质量相等
D.油脂不是天然高分子化合物
4.下列四组数据,代表烃的相邻四种同系物式量的是( )
A.14 28 42 56 B.16 30 44 58
C.16 17 18 19 D.50.5 64.5 78.5 92.5
5.结构简式为CH3CH(CH2CH3)CH(CH2CH3)CH2CH(CH3)2的化合物的正确命名是( )
A. 3,6-二甲基-4-乙基庚烷 B. 5-甲基-2,3-二乙基己烷
C. 1,1,4-三甲基-3-乙基己烷 D. 2,5-二甲基-4-乙基庚烷
6.下列各组中的实验现象能用相似的原理解释的是( )
A.苯酚、乙烯都能使溴水褪色
B.SO2和O3都能使品红溶液褪色
C.葡萄糖和福尔马林与新制氢氧化铜悬浊液共热,都产生砖红色沉淀
D.将SO2通入氯化钡溶液至饱和,再加入足量稀硝酸或苛性钠溶液,都产生白色沉淀
7.下列物质中既不能发生水解反应也不能发生还原反应的是( )
A.葡萄糖 B.纤维素 C.乙醇 D.蔗糖
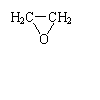 8.2001年11月,美军为打击躲藏在阿富汗山洞中的恐怖分子,使用了一种名为BLU-82的高能燃料空气炸弹,该炸弹的成分之一是环氧乙烷( )下列有关说法中,正确的是( )
8.2001年11月,美军为打击躲藏在阿富汗山洞中的恐怖分子,使用了一种名为BLU-82的高能燃料空气炸弹,该炸弹的成分之一是环氧乙烷( )下列有关说法中,正确的是( )
A.环氧乙烷是甲醛的同系物
B.等质量的环氧乙烷与乙酸乙酯分别完全燃烧时耗氧量相同
C.环氧乙烷是乙醛的同分异构体,肯定能发生银镜反应
D.环氧乙烷性质非常稳定,不易燃烧
9.下列实验所采取的方法正确的是( )
A.除去苯中苯酚,加入浓溴水后过滤
B.分离苯和溴苯,加水后分液
C.除去乙酸乙酯中乙酸,加入饱和Na2CO3溶液,振荡静置后过滤
D.区别乙酸、乙醛、乙醇,加入Cu(OH)2悬浊液后加热
10.氢核磁共振谱是根据不同化学环境的氢原子在谱中给出的信号不同来确定有机物分子中氢原子种类的。下列有机物分子中,在氢核磁共振谱中只给出一种信号的是( )
A.丙烷 B.新戊烷 C.正丁烷 D.己烷
11.下列物质水解时最难断裂的化学键是( )
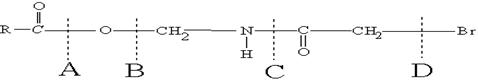
12.下列实验中,仪器的下端必须插入液面下的是 ( )
①制备氢气的简易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗;
③制备Fe(OH)2操作中的胶头滴管; ④将氯化氢气体溶于水时的导管;
⑤用乙醇制取乙烯时的温度计; ⑥分馏石油时的温度计。
A.①③⑤ B.②④⑥ C.①③④⑤ D.全部
13.下列关于蛋白质的叙述中错误的是( )
A.天然蛋白质经水解生成α—氨基酸
B.蛋白质溶于水时,加少量的Na2SO4 能促进蛋白质溶解,加大量Na2SO4时则会使蛋白质溶解度降低
C.蛋白质溶液中加入甲醛可以使蛋白质从溶液中析出,加水又溶解
D.硫酸铜溶液能使蛋白质变性
14.已知乙烯能被酸性高锰酸钾溶液氧化成CO2。既可用来鉴别乙烷和乙烯,又可用来除去乙烷中混有的乙烯的方法是( )
A.通入足量溴水中 B.分别在空气中燃烧
C.通入酸性高锰酸钾溶液中 D.在一定条件下通入氢气
15.下列各组混合物中的物质以任意物质的量比例相混合,只要总物质的量一定,则完全燃烧时消耗氧气的量不变的是( )
A. 甲烷、甲醇和甲醛 B. 甲醇、甲醛和甲酸
C. 乙醇、乙烯和丙烯酸 D. 甲酸、乙二酸和乙二醇
16.下列实验的失败是因为缺少必需的实验步骤造成的是 ( )
①锌与稀硫酸反应制取氢气,用排水法收集不到氢气 ②实验室用无水乙醇和浓硫酸共热140℃制取乙烯时得不到乙烯 ③验证RX是碘代烷,把RX与NaOH水溶液混合后,加入AgNO3溶液出现褐色沉淀 ④做醛的还原性实验时,当加入新制的Cu(OH)2悬浊液后,未出现红色沉淀 ⑤检验淀粉己水解,将淀粉与少量稀H2SO4加热一段时间后,加入银氨溶液后未出现银镜
A.①②③④⑤ B.①③④⑤
C.③④⑤ D.③⑤
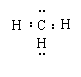 17.下列化学表达形式正确的是 ( )
17.下列化学表达形式正确的是 ( )
 A、甲基的电子式是
A、甲基的电子式是
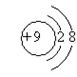
B、F—的结构示意图
![]()
![]() C、CO2分子的比例模型
C、CO2分子的比例模型
D、N2的结构式是
18.要设计实验证明:某种盐的水解是吸热的,有四位学生分别作出如下回答,其中正确的是( )
A.甲学生:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
B.乙学生:在盐酸中加入相同温度的氨水,若实验过程中混合液温度下降,说明盐类水解是吸热的
C.丙学生:在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的
D.丁学生:在醋酸钠溶液中滴入酚酞试液,加热后若红色加深,说明盐类水解是吸热的
19.某有机物能发生银镜反应,加入石蕊试剂不变色,取少量此有机物加入少量NaOH的酚酞溶液共煮,红色变浅,则原有机物是( )
A.葡萄糖溶液 B.甲酸乙酯 C.蔗糖溶液 D.乙酸甲酯
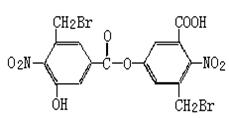 20.某有机物的结构简式如图,则下列说法正确的是 ( )
20.某有机物的结构简式如图,则下列说法正确的是 ( )
| |
B.向该有机物溶液中加入FeCl3溶液,振荡后有紫色沉淀产生
C.该有机物能发生消去反应
D.该有机物在稀硫酸中加热水解,有机产物只有一种
21.某链状有机物分子中含m 个-CH3,n 个-CH2-, a 个![]() 其余为羟基(-OH),则羟基(-OH)的数目可能是(
)
其余为羟基(-OH),则羟基(-OH)的数目可能是(
)
A.2n+3a-m B.a+2-m C.n+m+a D.a+2n+2-m
22.甲醛、乙酸和丙醛组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为( )
A、 27% B、28% C、 54% D、 无法计算
23.下列各组离子在溶液中不能大量共存,但混合后加入过量NaOH溶液或过量稀盐酸后,均能得到澄清溶液的是( )
A.Fe3+、Cl-、Na+、SO42- B.Al3+、Na+、HCO3-、NO3-
C.Ag+、Na+、SO42-、NO3- D.AlO2-、CO32-、K+、Na+
第Ⅱ卷(共54分)
![]() 二、(填空题,本题共40分)
二、(填空题,本题共40分)
24.(8分)邻羟基苯甲酸(俗名水杨酸)其结构简式如右式:
⑴ 羟基(-OH)的电子式为 _ _ 。
⑵ 将其与 _溶液作用生成物的化学式为C7H5O3Na;
将其与_ 溶液作用生成物的化学式为C7H4O3Na2。
⑶ 比水杨酸多一个CH2原子团,且与水杨酸不属于同系物的;取代基数目相同;并含有苯环的两类物质的结构简式分别为___________ 、 _________ 。
25.(12分)(1)在相同温度下,物质的量浓度相同的下列溶液:
a、HNO3 b、CH3COOH c、NH4NO3 d、(NH4)2SO4
①溶液的PH由小到大的顺序是 ﹝填序号﹞。
②水的电离程度由大到小的顺序是 ﹝填序号﹞。
(2)在Na2S溶液中,硫离子发生水解的离子方程式为:
为了使溶液中的C﹝Na+﹞︰C﹝S2-﹞接近2︰1,可向溶液中加入少量的 ﹝填序号﹞
A、Na2S B、K2S C、KHS D、KOH
(3)室温下,如果将0.1mol CH3COONa和0.05mol HCl全部溶于水,配成1L混合溶液
①________和________两种粒子的物质的量之和等于0.1mol。
②________和________两种粒子的物质的量之和比H+多0.05mol。
26.(12分)已知:
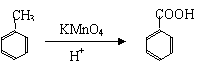
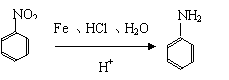 I:
I:
,
Ⅱ:当苯环上先引入 -R、-OH 、-NH2基团时,再引入基团一般进入该基团的邻或对位。若先引入的基团为-NO2、-COOH、-COOR等时,再引入的基团一般进入该基团的间位。
根据下面的合成路线及上述信息填空:
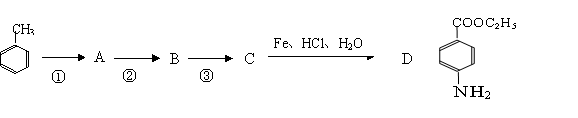 |
(1)反应①所加的试剂为所加的试剂为 。②的反应类型为 。
(2)A的结构简式为 。
(3)反应③的化学方程式为 。
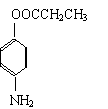
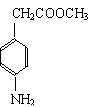 (4)物质D有多种同分异构体,其中属于酯类,苯环上含有两个取代基(其中之一是“-NH2”),且苯环上一氯代物只有2种的同分异构体共有6种,其中两种的结构简式为
(4)物质D有多种同分异构体,其中属于酯类,苯环上含有两个取代基(其中之一是“-NH2”),且苯环上一氯代物只有2种的同分异构体共有6种,其中两种的结构简式为
除D外,余下三种物质的结构简式为: ; ;
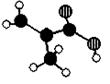 27. (8分)某化工厂生产的某产品M只含C、H、O三种元素,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等)
27. (8分)某化工厂生产的某产品M只含C、H、O三种元素,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等)
(1)该M的结构简式为 。
(2)M的某种同分异构体A,可发生下列反应:
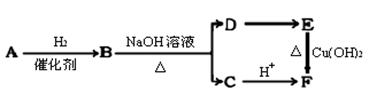
写出下列两个反应的化学方程式(有机物用结构简式表示)。
①B→C+D 。
②E→F 。
(3)在一定条件下,该产品M跟乙二醇反应可得到分子式为C6H10O3的物质,该物质发生加聚反应可得到用来制作隐形眼镜的高分子材料,这种高聚物的结构简式为: 。
三.(实验题,共8分)
28.(8分)某课外研究性学习小组用下图所示装置制备少量溴苯并验证溴与苯的反应是取代反应。
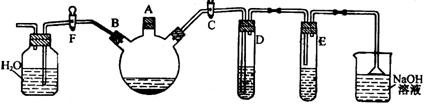
实验时,关闭F活塞,打开C活塞,在装有少量苯的三口烧瓶中由A口加入少量溴,再加入少量铁屑,塞住A口。
回答下列问题:
(1) 三口烧瓶中发生反应的化学方程式为:
(2) D试管内装的是 ,其作用是 。
(3) E试管内装的是 。
(4) 根据什么现象可证明验证溴与苯的反应是取代反应 。
四.(计算题,共6分)
29. (6分)乙烯与乙烷混合气体共 a mol ,与 b mol 的氧气共存于一密闭容器中,点燃后充分反应,乙烯、乙烷和氧气恰好完全消耗,得到 CO2 气体和 45 g 水。试求:
(1)当 a = 1 ,消耗的氧气为________ mol
(2)当 a = 1 时,乙烯与乙烷的物质的量之比 n(C2H4):n(C2H6)= ________
(3)a 的取值范围是 ______________
 化学试卷答案卷
化学试卷答案卷
第Ⅰ卷(选择题)
一、选择题(本题共46分,每小题2分,每题只有一个正确选项)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| A | A | B | B | D | C | C | B |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| D | B | B | A | C | A | C | B |
| 17 | 18 | 19 | 20 | 21 | 22 | 23 |
|
| B | D | B | A | B | C | B |
|
第Ⅱ卷(非选择题)
二、(填空题,本题共40分)
24.(8分)⑴ 羟基(-OH)的电子式为 _ _ 。
⑵ _;_ 。
⑶ ___________ 、 _________ 。
25.(12分)
(1)① 。② 。
(2) ; ﹝填序号﹞
(3) ①________和________。 ②________和________。
26.(12分)
(1)①的试剂为 。②的反应类型为 。
(2)A的结构简式为 。
(3)反应③的化学方程式为 。
(4)除D外,余下三种物质的结构简式为:
; ;
27. (8分)
(1)该M的结构简式为 。
(2)①B→C+D 。
②E→F 。
(3)高聚物的结构简式为: 。
三.(实验题,共8分)
28.(8分)
(1)
(2) D试管内装的是 ,其作用是 。
(3) E试管内装的是 。
(4) 。
四.(计算题,共6分)
29. (6分)
(1)当 a = 1 ,消耗的氧气为________ mol
(2)当 a = 1 时,乙烯与乙烷的物质的量之比 n(C2H4):n(C2H6)= ________
(3)a 的取值范围是 ______________