��![]()

![]()

������������ѧ��ѧ����������ϰ�⣨����������λ��
| ��� | һ | �� | �� | �� | �ܷ� |
| �÷� |
|
|
|
|
|
�����õ������ԭ��������H:1 C:12 N:14 O:16 S:32��Cl:35.5 Br:80 Na:23 Mg:24��Al:27��Fe:56 K:39��Cu:64��Ag:108��
��������ѡ���� ��54�֣�
һ��ѡ�������������18С�⣬ÿС��ֻ��һ��ѡ��������� ÿС��3�֣���54�֣���
1����Ϣ�����ϡ���Դ����Ϊ�¿Ƽ������ġ�����֧�����������й���Ѷ�������
�� A���ڼ�������������Դʱ�������ܡ�̫���ܡ����ܽ���Ϊ��Ҫ��Դ
�� B��Ŀǰ���С������յȹ����յ��մɷ������������ܽϴ�̶ȵؽ����ܺģ���Լ��Դ
�� C����������Ϣ��ҵ���й㷺Ӧ�ã�������µ���Ҫ�����ǵ��ʹ�
�� D���ṹ�մ�̼����B4C3�������������������ߣ�����һ���������ǽ������ϣ�����ԭ�Ӿ���
2����ȷ���ջ�ѧ����ͻ�ѧ����������ѧ�û�ѧ�Ļ����������йر�������ȷ��һ����
A����������(CH3COOOH)���ǻ�����(HOCH2COOH)������������ͬ������Ϊͬ���칹��
B��16O��18O��Ϊͬλ�أ�H216O��D216O��H218O��D218O��Ϊͬ��������
C��P4��CH4��NH4�����ӵĿռ乹�;�Ϊ���������ͣ�CO2��C2H2��Ϊֱ���ͷ���
D��Ca2���Ľṹʾ��ͼΪ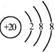 ��NH4Cl�ĵ���ʽΪ
��NH4Cl�ĵ���ʽΪ![]()
3�������ӵ�����ԼΪ6.02��1023 mol��1������˵������ȷ����
A�����³�ѹ�£�22g������26g����������ԭ������Ϊ3 NA
B��6.2g����P4��������P��P���ĸ���Ϊ0.3 NA
C���ڱ�״���£�V L CH2O�к��е���ԭ�Ӹ���Ϊ![]()
D��1L 0.5 mol/L CH3COONa��Һ�к��е�CH3COO������Ϊ0.5 NA
4������ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ������ȷ����
| X | Y |
| |
| �� | ������ | ������ | ������ |
| A | ����ͬϵ�� | ������ | �����廯���� |
| B | ���� | ��ɢϵ | ����� |
| C | ����� | ���ӻ����� | ������ |
| D | ���������� | ���������� | ������ |
 5��ij����ʽΪC10H20O2��������һ�������¿ɷ�������ͼ��ת�����̣�
5��ij����ʽΪC10H20O2��������һ�������¿ɷ�������ͼ��ת�����̣�
��������������������Ľṹ����
A��2�֡�B��4�֡���C��6�֡� D��8��
6��X��Y��Z��WΪ���ֶ���������Ԫ�ء�����X��Zͬ�壬Y��Zͬ���ڣ�W��X��Y�Ȳ�ͬ��Ҳ��ͬ���ڣ�Xԭ�������������Ǻ�����Ӳ�����3����Y���������������۵Ĵ�����Ϊ6������˵����ȷ����
A��X��W�����γ�W2X��W2X2���ֻ�����
B��YԪ������������Ӧˮ����Ļ�ѧʽΪH2YO4
C��ԭ��������С�����˳��ΪW��X��Y��Z
D��Y��Z��Ԫ�صļ����ӵİ뾶Y��Z
7�����и��������ڼ����������ܴ������棬����ǿ�����������ܷ���������ԭ��Ӧ����
A��Ca2+��AlO2����SO42����Cl������������ B��K����ClO-��Cl����NO3��
C��Na+��K����NO3����SO42�������������� D�� NH4+��Na+��F����CO32��
8. �������ӷ���ʽ��ȷ���ǡ�������������
A�������������Һ�м�������������Һ��pH��7��Ba2����OH����H����SO42����BaSO4����H2O
B��������SO2����ͨ��NaClO��Һ�С�SO2��2ClO����H2O��SO32����2HClO
C������������Һ�м����������ữ�Ĺ���������Һ 2Fe2+ + 2H+ + H2O2 =2 Fe3+ + 2H2O
D����NaHCO3 ��Һ�мӹ���Ca(OH)2 ��Һ2HCO3����Ca2++2OH-=2H2O+CaCO3��+CO32��
9��һ�������£����Ϊ10L���ܱ������У�1mol X��1mol Y���з�Ӧ��
2X(g)��Y(g)![]() Z(g)����60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ����
Z(g)����60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ����
A��������ѹǿ��������Y��ת���ʼ�С
B�������������Ϊ20 L��Z��ƽ��Ũ�ȱ�Ϊԭ����![]()
C����XŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.001mol/(L��S)
D���������¶ȣ�X���������������÷�Ӧ�ġ�H��0
10���Ӻ�ˮ����ȡþ���ɰ����²�����У�
�ٰѱ����Ƴ�ʯ���飻 ��������ĺ�ˮ�м���ʯ���飬���������ˡ�ϴ�ӳ���� �۽������������ᷴӦ���ᾧ���ˡ���HCl�����Χ�и����� �ܽ��õ��IJ������ڵ��õ�þ������˵������ȷ����
A���˷����ŵ�֮һ��ԭ����Դ�ḻ��������B���٢ڢ۲����Ŀ���ǴӺ�ˮ����ȡMgCl2
C��������ȡþ�Ĺ������漰���ϡ��ֽ���ֽⷴӦ��D���ڢܲ����ʱ������������
11���ڽ����������ʱ仯���������ʽṹ��������ϵʱ����������ı仯������
A��F2��Cl2��Br2��I2�ķе������ߡ� B��HF��HCl��HBr��HIˮ��Һ������������ǿ
C��HF��HCl��HBr��HI���ȶ������μ����� D�������ȣ����ʯ�ģ��۵��
12�����и���Һ�У������ӿ��ܴ����������
A�����д���Ba2������Һ�У�HCO3����Fe3����Ag����SO42����SCN��
B���μ�ʯ����Һ���Ժ�ɫ����Һ�У�Na����CO32����K����ClO����AlO2��
C����ˮ�����c(OH��)=10��14mol��L��1 ����Һ�У�CH3COO����C6H5O����Na����K��
D���������ۺ������������Һ�У�NH4����Na����NO3����Cl����HS��
13����(Sb)����Ȼ��һ�����������ʽ���ڣ��ҹ�����̲���ռ�����һ������������ȡ������һ�������ڸ����½�����ת��Ϊ���������̼��ԭ��
2Sb2S3��3O2��6Fe��Sb4O6��6FeS ��������������������
Sb4O6��6C��4Sb��6CO�� �����������ڡ��� ���ڷ�Ӧ�١���Ӧ�ڵ�˵����ȷ���ǣ�
A�� ��Ӧ�٢��е��������ֱ���Sb2S3��Sb4O6��B����Ӧ����ÿ����3 mol FeSʱ����ת��6 mol����
C����Ӧ��˵��������Sb�Ļ�ԭ�Ա�Cǿ
D��ÿ����4 mol Sbʱ����Ӧ���뷴Ӧ���л�ԭ�������ʵ���֮��Ϊ4�U3
14������ͼ��ʾ��������M�м��ۻ������أ������㶹������Ȼ�������M������������ȷ����
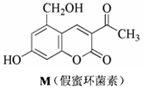 A��M������FeCl3������Ӧ��������CH3COOH������Ӧ
A��M������FeCl3������Ӧ��������CH3COOH������Ӧ
B��M��Br2ֻ�ܷ���ȡ����Ӧ�����ܷ����ӳɷ�Ӧ
C��M������NaOHϡ��Һ��1molM�������3mol NaOH
D��1molM�ڴ����������������4molH2�����ӳɷ�Ӧ
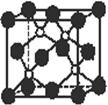 15��������һ�ֳ�Ӳ��ĥͿ����ϡ���ͼΪ�侧��ṹ����С���ظ����� �ṹ��Ԫ�����е�ÿ��ԭ�Ӿ�����8�����ȶ��ṹ�������й�˵����ȷ ����
15��������һ�ֳ�Ӳ��ĥͿ����ϡ���ͼΪ�侧��ṹ����С���ظ����� �ṹ��Ԫ�����е�ÿ��ԭ�Ӿ�����8�����ȶ��ṹ�������й�˵����ȷ ����
A��������Ļ�ѧʽΪBP���������Ӿ���
B����������۵�ߣ�������״̬���ܵ���
C����������ÿ��ԭ�Ӿ��γ�4�����ۼ�
D��������ṹ���Ŀռ�ѻ���ʽ���Ȼ�����ͬ
16������ͼ��ʾ��a��b�Ƕ��ʯī�缫��ijͬѧ��ͼʾװ�ý������¡�ʵ�飺�Ͽ�K2���պ�K1һ��ʱ�䣬�۲쵽��ֻ�������ڶ������ݽ��缫��Χ����ʱ�Ͽ�K1���պ�K2���۲쵽������A��ָ����ƫת������˵������ȷ����
A���Ͽ�K2���պ�K1һ��ʱ�䣬��Һ��pHҪ���
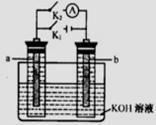 B���Ͽ�K1���պ�K2ʱ��b���ϵĵ缫��ӦʽΪ�� 2H����2e��=== H2��
B���Ͽ�K1���պ�K2ʱ��b���ϵĵ缫��ӦʽΪ�� 2H����2e��=== H2��
C���Ͽ�K2���պ�K1ʱ��a���ϵĵ缫��ӦʽΪ��4OH���D4e��=== O2��ʮ2H2O
D���Ͽ�K1���պ�K2ʱ��OH����b���ƶ�
17�������£����и���Һ����������ȷ����
A��0.1mol/L�Ĵ�������Һ20mL��0.1mol/L����10mL��Ϻ���Һ������
c (Ac��)��c (Cl��)��c (H��)��c (HAc)
B��pH=7�Ĵ����ƺʹ�����Һ�У�c��Na������ c��CH3COO����
C��0.1mol/L�Ĵ����pH��a��0. 1mol/L�������pH��b����a<b
D����֪����HF��CH3COOH��pH��ȵ�NaF��CH3COOK��Һ�У�
[c(Na��)��c(F��)]< [c(K��)��c(CH3COO��)]
18������100 mL ����ΪMgCl2��AlCl3�Ļ����Һ������c(Cl��)��1.0 mol��L��1��c(Mg2��)��0.2mol��L��1����������ˮ�����أ���Ҫʹ���е�Mg2��ȫ��ת��ΪMg(OH)2���������������������Ҫ4mol��L��1��NaOH��Һ�������
A��25mL���������� B��5mL���������� C��30mL���������� D��100mL
�ڢ������ѡ���� ��54�֣�
��������⣨���������С�⡡��23�֣�
19.��13�֣�X��Y��Z��W����ԭ������������������ֶ�����Ԫ�أ���������������������Ԫ�����ڱ��У�Z��Y���ڣ�Z��WҲ���ڣ���Y��Z��W����Ԫ�ص�ԭ�����������֮��Ϊ17.����գ�
��Y��Z��W�Ƿ�λ��ͬһ���ڣ���ǡ��������������� �������� ����������������������������
��Y�������������� ��Z�������������� �� W����������������
��X��Y��Z��W�����һ�������ԭ�Ӹ�����Ϊ8��2��4��1��д���û���������Ƽ���ѧʽ������������������������
20����10�֣��������п�ͼ��ϵ��գ���֪��Ӧ�١������ҹ���ҵ�����е���Ҫ��Ӧ��X������Ϊ��ɫ��ζ��Һ�壻C��ɫ��Ӧ����ʻ�ɫ��JΪ���ɫ������D��E������Ϊ���壬��E��ʹƷ����Һ��ɫ��A�����н�������Ԫ�أ����н���Ԫ�ص���������ԼΪ46.7%��
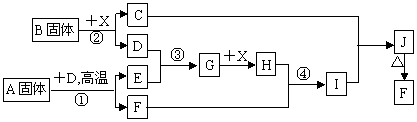 |
��1��G�Ļ�ѧʽΪ�������� ��
��2������A���������Ļ�ѧ�������B���ƣ���A�ĵ���ʽΪ�� ���������� ��
��3����Ӧ�ڵ����ӷ���ʽ���������������������������������������������� ��
��4����Ӧ�ܵ����ӷ���ʽ�������������������������������� ����������������
��5����֪ÿ����16 g E���ų�106.5 kJ��������Ӧ�ٵ��Ȼ�ѧ����ʽΪ��
������������������������������������������������������������������ ��
����ʵ���⣨��12�֣� 21����12�֣��ҹ�����ר�Һ�°�ġ������Ƽ����Ϊ�����Ƽҵ������ͻ�����ס�����NaCl��NH3��CO2��Ϊԭ�����Ƶ�NaHCO3����������������йط�Ӧ�Ļ�ѧ����ʽΪ��NH3��CO2��H2O �� NH4HCO3 ����NH4HCO3��NaCl �� NaHCO3����NH4Cl ��
![]() 2NaHCO3������ Na2CO3��CO2����H2O
2NaHCO3������ Na2CO3��CO2����H2O
��1��̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ������������ ������ĸ��ţ���
a��̼������������ˮ������������ b��̼�����������ֽ�
c��̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
��2��ij̽���С����������Ƽ�ԭ��������̼�����Ƶ��Ʊ�ʵ�飬ͬѧ�ǰ�������Ƶķ���ʵ�顣
�� һλͬѧ��������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ������ͼ��ʾ��ͼ�мг֡��̶��õ�����δ��������
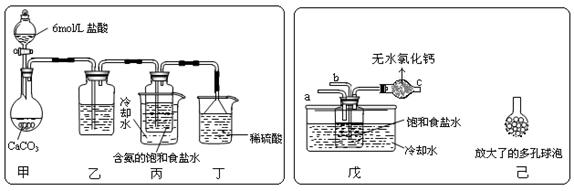
�Իش������й����⣺
![]() ������װ���е��Լ��������������� ������װ����ϡ���������������������������
��
������װ���е��Լ��������������� ������װ����ϡ���������������������������
��
����ʵ����������NaHCO3 ����IJ��������������������������������ƣ���
�� ��һλͬѧ��ͼ����װ�ã�����װ��δ����������ʵ�顣
����ʵ��ʱ�����ȴ������� ��ͨ�������� ���壬�ٴ��� �� ����ͨ�������������壻
������ͬѧ��������װ�õ�b���¶����Ӽ�װ�ã��������������� ������������������
��3��������д��һ��ʵ������ȡ����̼�����Ƶķ��������������������������������� ��
�ġ��л��ƶ��⣨��19�֣�
22����19�֣���������һ��ֻ��C��H��O�Ļ�����A ��A���������ϣ�����Է�������Ϊ88��������C��H��Oԭ�Ӹ�����Ϊ2:4:1 ��
��.�� A�ķ���ʽΪ___________��
��.�� д����A����ʽ��ͬ���������Ľṹ��ʽ�� ___________________________________��
����֪��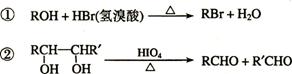
��A�к���̼��˫������A��صķ�Ӧ���£�
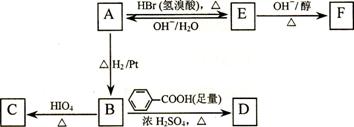
��.д��A �� E��E �� F�ķ�Ӧ���ͣ�A �� E ___________��E �� F ___________��
��.д��A��C��F�Ľṹ��ʽ��A _____________��C ____________��F ___________��
��.д��B �� D��Ӧ�Ļ�ѧ����ʽ��_________________________________________��
��.�ڿ����г�ʱ��������ͣ�A��ת��Ϊ��Է�������Ϊ86�Ļ�����G��G��һ�ȴ���ֻ��һ�֣�д��G�Ľṹ��ʽ��________________��A �� G�ķ�Ӧ����Ϊ_________��
��ѧ�������
һ��ѡ����(�������10С�⣬ÿС��5�֣���50��)
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� | C | C | D | C | B | A | B | C | C | D |
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| �� | A | C | B | C | C | B | B | C |
��������⣨���������С�⡡��23�֣�
19.��13�֣�
��Y��Z��W�Ƿ�λ��ͬһ���ڣ���ǡ����� ������������ ������ ��λ��ͬһ������Y�������������������������� Z��W������������ְ�Ͳ�����Ϊ17��
��Y���� ���������� ��Z���������������� �� W������ ������������
��X��Y��Z��W�����һ�������ԭ�Ӹ�����Ϊ8��2��4��1��д���û���������Ƽ���ѧʽ��
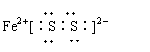 �������(NH4)2SO4��������������������
�������(NH4)2SO4��������������������
20����1��G�Ļ�ѧʽΪ��SO3 ��������
��2������A���������Ļ�ѧ�������B���ƣ���A�ĵ���ʽΪ�� ���������� ��
��3����Ӧ�ڵ����ӷ�2Na2O2+2H2O=4Na++4OH-+O2��
��4����Ӧ�ܵ����ӷ���ʽ�� Fe2O3+6H+=2Fe3++3H2O���� ��
��5����֪ÿ����16 g E���ų�106.5 kJ��������Ӧ�ٵ��Ȼ�ѧ����ʽΪ��
4FeS2(S)+11O2(g)=2Fe2O3(S)+8SO2(g);��H=-3408 kJ��mol-1
21.��12�֣��� ��1��c ��1�֣���2���٣�����̼��������Һ��������������δ��Ӧ��NH3���𡰷�ֹ������������CO2�������֣����������� ��ÿ��1�֣���3�֣��ڣ���a��NH3�� b��CO2�� �� ��ÿ��1�֣���4�֣���2��������������Һ�Ӵ���������CO2�����ʣ�����2�֣�
��3����̼���������������ʳ��ˮ��Ӧ���������ռ���Һ��ͨ�����CO2 ��������Na2CO3 ��Һ��ͨ�����CO2 �ȡ����������������ɣ�����2�֣�
22. ��A�ķ���ʽΪ_C4H8O2__________��
��д����A����ʽ��ͬ���������Ľṹ��ʽ�� HCOOCH2CH2CH3; HCOOCH(CH3)CH3; CH3COOCH2CH3;�� CH3CH2COOCH3
��.д��A �� E��E �� F�ķ�Ӧ���ͣ�A �� E __ȡ����Ӧ_________��E �� F _��ȥ��Ӧ__________��
��.д��A��C��F�Ľṹ��ʽ�� 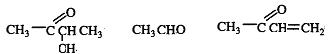
��.д��B �� D��Ӧ�Ļ�ѧ����ʽ��
CH3CH(OH)
CH(OH)CH3+2C6H5COOH![]() CH3CH(OOCC6H5)
CH(OOCC6H5)CH3+2H2O
CH3CH(OOCC6H5)
CH(OOCC6H5)CH3+2H2O
��.�ڿ����г�ʱ��������ͣ�A��ת��Ϊ��Է�������Ϊ86�Ļ�����G��G��һ�ȴ���ֻ��һ�֣�д��G�Ľṹ��ʽ��CH3COCOCH3�� A �� G�ķ�Ӧ����Ϊ__������Ӧ_______��
 Z
Z