高三化学上册期末模拟试题
第Ⅰ卷(选择题,共48分)
一:选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意)
1.下列关于蛋白质的叙述中,不正确的是
A.蛋白质溶液里加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不溶解
B.人工合成具有生命活力的蛋白质—结晶牛胰岛素是我国科学家1965年首次合成的
C.重金属盐能使蛋白质凝结,所以误食重金属盐会中毒
D.浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生颜色反应
2.下列各组变化中,前者是物理变化,后者是化学变化的是
A.风化 裂化 B.水解 电解
C.分馏 干馏 D.渗析 盐析
3.某酒精厂由于管理不善,酒精滴漏到某种化学品上而酿成火灾。该化学品可能是
A.KMnO4 B.NaCl
C.(NH4)2SO4 D.CH3COOH
4.下列各组物质中不易用物理性质区分的是
A.苯和四氯化碳 B.酒精和汽油
C.碘和高锰酸钾固体 D.氯化铵和硝酸铵晶体
5.下列物质中最难电离出H+ 的是
A. CH3COOH B.C2H5OH
C.H2O D.C6H5OH
6.下图是2008奥运吉祥物,其外材料为纯羊毛,内充聚酯纤维,该聚酯纤维的化学式为 (COC6H4COOCH2CH2O)n。下列说法中不正确的是





A.羊毛与聚酯纤维的化学成分不相同
B.由单体合成聚酯纤维的反应属加聚反应
C.该聚酯纤维单体为对苯二甲酸和乙二醇
D.聚酯纤维和羊毛一定条件下均能水解
7.某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种,则这种烃可能是
①分子具有7个碳原子的芳香烃 ②分子中具有4个碳原子的烷烃
③分子中具有12个氢原子的烷烃 ④分子中具有8个碳原子的烷烃
A.①② B.②③
C.③④ D.②④
8.将a mol纯铁粉投入含HNO3 b mol的稀溶液里,恰好完全反应并放出NO气体,则a和b的关系是
A.a/b=1/4 B.a/b=3/8
C.1/4≤a/b≤3/8 D.a/b的值无法确定
二:选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意)
9.下列离子方程式不正确的是
A.100mL0.1mol·L-1的Na2CO3溶液中加入0.01molCH3COOH
CO32—+ 2CH3COOH = CO2↑+ 2CH3COO—+ H2O
B.4mol·L-1的NaAlO2溶液和7mol·L-1的HCl等体积互相均匀混合
4AlO2—+ 7H+ + H2O = 3Al(OH)3↓+ Al3+
C.在含有Mn2+的溶液中加入HNO3再加入PbO2,则反应体系显紫红色
5PbO2 + 2Mn2+ + 4H+ = 5Pb2+ + 2MnO4— + 2H2O
D.甲醛溶液中加入足量的银氨溶液并加热
HCHO+2[Ag (NH3)2]++2OH—![]() HCOO—+NH4++2Ag↓+3NH3+H2O
HCOO—+NH4++2Ag↓+3NH3+H2O
10.设NA为阿伏加德罗常数,下列叙述合理的是
A.通常状况下,1molNaHCO3投入足量稀盐酸中,反应完后,可逸出NA个CO2分子
B.在含有1mol CH3COO—的醋酸钠溶液中, Na+数目略大于NA
C.46gNO2和N2O4混合气体中含有原子数为3NA
D.22.4L的O3和O2的混合气体所含原子数为3NA
11.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是
A.K+、Na+、HCO3—、NO3— B.Na+、SO42—、Cl—、 ClO—
C.H+、Mg2+、SO42—、NO3— D.Ag+、K+、NO3—、Na+
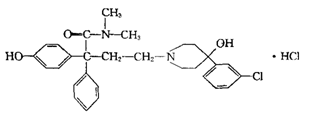
12.盐酸洛派丁胺俗称易蒙停,它是一种新型的止泻药,适用于各种急慢性腹泻的治疗,其结构简式如图: 下列说法不正确的是
A.易蒙停的分子式为C29H34Cl2N2O3
B.向易蒙停溶液中加入FeCl3溶液,溶液显紫色
C.1mol易蒙停只能与lmolNaOH发生反应
D.lmol易蒙停最多能与3mol溴水发生反应
13.据最新报道,科学家发现了如下反应:O2 + PtF6 = O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列说法正确的是
A.在此反应中,O2氧化剂,PtF6是还原剂
B.O2(PtF6)中氧元素的化合价为+1价
C.在此反应中,每生成1 mol O2(PtF6) 则转移1 mol电子
D.在O2(PtF6)中不存在共价键
14.有机物A和B只由C、H、O三种元素中的两种或三种组成,相等物质的量的A和B分别燃烧时,消耗相等物质的量的氧气。则A和B的相对分子质量的差值不可能是(n为小于5的正整数)
A.44n B.18n C.14n D.0
第Ⅱ卷(非选择题,共72分)
三:(本题包括1小题,共22分)
15.Ⅰ、(1)称取8.8g固体样品(1g以下使用游码)时,将样品放在了托盘天平的右盘,则所称样品的实际质量为 g。
(2)由于错误操作,使得到的数据比正确数据偏大的是 。
A.用量筒量取一定量液体时,仰视液面读数
B.使用容量瓶配制溶液时,仰视液面进行定容,所得溶液的浓度
C.中和滴定达到终点时,仰视滴定管液面的读数
(3)有下列实验:①制硝基苯 ②乙烯的制取 ③石油的分馏 ④乙酸乙酯的制取⑤乙酸乙酯的水解 ⑥酚醛树脂的制取,其中不需要温度计的有 (填写编号)。
Ⅱ、乙醛是一种常用的有机试剂,也象葡萄糖一样在碱性和加热条件下,能与银氨溶液反应析出银。如果条件控制适当,析出的银会均匀地分布在试管壁上,形成光亮的银镜,因此这个反应又叫银镜反应。银镜的光亮程度与反应条件有关。同学们在课外活动中对乙醛的银镜反应进行了探究。
a、探究银镜反应的最佳实验条件(部分实验数据如下表):
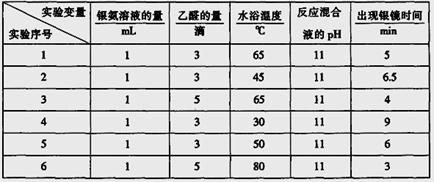
请回答下列问题:
(1)试写出乙醛和银氨溶液反应的离子方程式: 。
(2)读表 若只进行实验1和实验3,其探究目的是 。
(3)推理 当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间是 ;要探索不同水浴温度下乙醛进行银镜反应的最佳条件,除了测量银镜出现的时间外,还需要比较不同条件下形成的银镜的 。
(4)进一步实验 若还要探索银氨溶液的用量对出现银镜快慢的影响,
如何进行实验?
。
b、探究对废液的回收处理
银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费。通过查找资料,已知从银氨溶液中提取银的一种实验流程为:
![]()
(5)操作④的方法是:把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,同时有臭鸡蛋气味的气体生成,试写出此反应的化学方程式: 。
(6)若获得的银粉中含有少量没有反应完的铁粉,除去铁的反应的离子方程式为: ,需要用到的玻璃仪器有 (填编号)。
四:(本题包括3小题,共26分)
16.(8分)已知下图每一方框中的字母代表一种反应物或生成物(图中部分反应物或生成物没有列出)。其中,化合物石灰氮是由Ca、N、C等三种元素组成的盐,它以前是一种常用的肥料,其含钙、碳的质量分数分别为50%、15%。反应①是石灰氮的完全水解,其产物之一可方便地制成一种氮肥。通常状况下,C为气体。
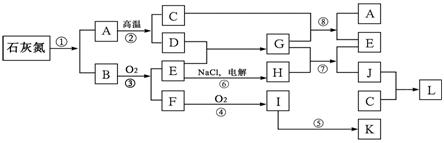 请按要求回答:
请按要求回答:
⑴写出石灰化氮的化学式 ______;
⑵写出反应①的化学方程式 ___________________________________;
⑶除反应②、③、④、⑤是应用于工业生产外,还有两个反应是运用于工业生产的反应,它们的化学方程式分别是 ____________和 _________。
17.(8分)A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含有一种官能团,且每个碳原子上最多只连一个官能团:A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请填空:
⑴ A的分子式是 ,其结构简式是 。
⑵ 写出A与乙酸反应的化学方程式: 。
⑶ 写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是
______________________。
![]() 18.(10分)快乐是什么?精神病学专家通过实验发现:在大脑的相应部位—“奖赏中心”给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺的结构为:
18.(10分)快乐是什么?精神病学专家通过实验发现:在大脑的相应部位—“奖赏中心”给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺的结构为:
回答下列问题:
I、多巴胺的分子式为 。
II、写出多巴胺与浓溴水反应的化学方程式: 。
III、多巴胺可由香兰素与硝基甲烷反应后再经锌汞齐还原水解制得。合成过程可表示如下:
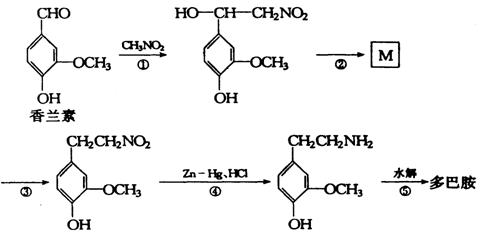
(1) 反应①属于 反应(填反应类型)。
(2)写出M的结构简式 。
(3)多巴胺分子中羟基处于苯环上不同位置时的同分异构体共有 种(苯环上的其它结构不变)。
五:(本题包括2小题,共16分)
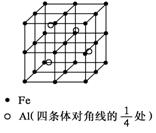 19.(6分)晶体是质点(分子、离子或原子等)在空间有规则地排列、具有整齐外形、以多面体出现的固体物质。在空间里无限地周期性的重复能形成晶体的、具有代表性的最小单元,称为晶胞。一种Al-Fe合金的立体晶胞如下图所示。
19.(6分)晶体是质点(分子、离子或原子等)在空间有规则地排列、具有整齐外形、以多面体出现的固体物质。在空间里无限地周期性的重复能形成晶体的、具有代表性的最小单元,称为晶胞。一种Al-Fe合金的立体晶胞如下图所示。
请据此回答下列问题:
(1)确定该合金的化学式____________。
(2) 取2.78 g的该合金粉末溶于100 mL某稀硝酸溶液中,待反应完全后得到1.12 L NO气体(标准状况,设两者恰好完全反应),则原硝酸溶液的物质的量浓度为______mol/L,反应后溶液中Fe3+离子的物质的量浓度为______mol/L。
20.(10分)I、几年前,科学家用NaNO3和Na2O在573 K反应制得了离子化合物Na3NO4。⑴ 经测定Na3NO4中的各原子的最外层电子都达到了8电子稳定结构,则NO43-的电子式为 。
⑵ Na3NO4与二氧化碳或水都能剧烈反应而转化为两种常见物质,试写出这两个反应的化学方程式: , _________ 。
II、甲酸在浓硫酸作用下脱水可制得CO,碳酸可分解为H2O和CO2,目前已有文献报道,碳还能形成其他一些氧化物,如:丙二酸在减压下用P4O10于140℃脱水可制得C3O2,它的熔点—120℃,沸点6.7℃,室温下聚合成黄色液体。根据以上信息可推知:C3O2的结构简式为____________ ,C3O2是____________分子(填“极性”或“非极性”)
六:(本题包括1小题,共8分)
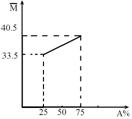 21.由A、B两种物质组成的混合气体,其平均相对分子质量随A的物质的量分数变化关系如右图所示。
21.由A、B两种物质组成的混合气体,其平均相对分子质量随A的物质的量分数变化关系如右图所示。
⑴A的相对分子质量为__________。
⑵若测得混合气体中仅含两种元素,
A、B都是无机物时,化学式分别为_________、________,
A、B都是有机物时,化学式分别为_________、________。
⑶某混合气由A、B等体积混合而成,将其与适量氧气混合,引燃后反应物均无剩余,将产物依次通过足量浓H2SO4(减少的体积恰好等于消耗氧气的体积)、足量碱石灰(体积减半),又知通过浓H2SO4与通过碱石灰所减少的气体体积之比为5∶2。气体体积均在105℃和1.01×105Pa条件下测定的,据此确定混合气体的组成为 。
1~8 ACADBBCC 9~14 AD、BC、B、CD、C、C
15.Ⅰ:7.2 \ C \ ④⑥
Ⅱ:(1)
(2)比较乙醛用量不同时生成银镜的时间(速度或质量均可)
(3)在6.5~9min之间;光亮程度(或亮度、外观、效果等 )
(4)保持其他的实验条件不变,改变银氨溶液的用量,测量生成银镜的时间。
(5)Ag2S+Fe+2HCl2 Ag+ FeCl2+H2S↑
(6)Fe+2H+==Fe2++H2↑ (或Fe+2 Fe3+==3Fe2+);bef
16.⑴CaCN2 ⑵ CaCN2 + 3H2O = CaCO3 + 2NH3↑ ⑶ ⑥ ⑦
2NaCl + 2H2O
![]() 2NaOH + Cl2↑+ H2↑
2NaOH + Cl2↑+ H2↑
2Cl2 + 2Ca(OH)2=CaCl2 + Ca(ClO)2 + 2H2O
17.⑴ C5H12O4 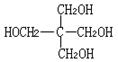
⑵ C(CH2OH)4+4CH3COOH![]() C(CH2OCCH3)4+4H2O
C(CH2OCCH3)4+4H2O
⑶ CH3![]()
![]()
![]() CH2OH HOCH2CH2
CH2OH HOCH2CH2![]()
![]() CH2OH HOCH2
CH2OH HOCH2![]() CH2
CH2![]() CH2OH
CH2OH
18.(1)C8H11NO2 (2)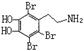
![]()
![]() +3Br2→
+3HBr
+3Br2→
+3HBr
(3)I、加成反应 II、 。 III、 6
19.⑴ Fe2Al ⑶ 2 mol/L 0.1 mol/L
20.I、
⑵Na3NO4+CO2====NaNO3+Na2CO3 Na3NO4+H2O====NaNO3+2NaOH
II、⑴①O=C=C=C=O(1分),非极性(1分)
21、(1) 44(2分)
(2)__N2O______ NO C3H8 C2H6 (2分)
(3)___ C3H8和CH2O _____ C2H4O和C2H6_____(6分)______