08届高三理科综合之化学测试试题
6.下列单质中,最容易跟氢气发生反应的是
A.O2 B.N2 C.F2 D.Cl2
7.下列有关实验的现象描述正确的是 ( )
A.氢气在氯气中燃烧,火焰呈苍白色,产生大量白雾,剧烈放热。
B.硫在空气中燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体,剧烈放热。
C.铜在氯气中燃烧,产生白烟,加水溶解后可得绿色溶液。
D.用洁净的铂丝沾取碳酸钾粉末在酒精灯火焰上灼烧,可观察到明亮的紫色火焰。
8.小华家中有如下生活用品:碘酒、食盐、食醋、84消毒液(内含NaClO),小华利用上述用品不能完成的任务是
A.检验买来的奶粉中是否加有淀粉 B.检验自来水中是否含有Cl-
C.除去保温瓶中的水垢 D.洗去白色衣服上的番茄汁
9.下列物质能直接用金属和氯气反应得到的是 ( )
① CuCl2 ②FeCl2 ③FeBr2 ④MgCl2 ⑤FeI3 ⑥ FeI2
A.①③⑥ B. ①④⑥ C.①②③④⑥ D.①③④⑥
10.设NA表示阿伏加德罗常数,下列说法中不正确的是
A.一定量的Fe与含1mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA
B.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
C.0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA
D.125gCuSO4・5H2O晶体中含有0.5NA个Cu2+
![]()
![]()
![]() 11.在实验室进行物质制备,下列从原料及试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合理的是
11.在实验室进行物质制备,下列从原料及试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合理的是
![]()
![]() A.C
CO
CO2
Na2CO3
A.C
CO
CO2
Na2CO3
![]()
![]() B.Cu Cu(NO3)2溶液 Cu(OH)2
B.Cu Cu(NO3)2溶液 Cu(OH)2
![]()
![]() C.Fe Fe2O3 Fe2(SO4)3溶液
C.Fe Fe2O3 Fe2(SO4)3溶液
D.CaO Ca(OH)2溶液 NaOH溶液
12.下列各组离子,能大量共存且在加入铝粉后能放出氢气的是,
A.NO3- CO32- Na+ H+ B.Na+ Ba2+ Mg2+ HCO3- OH-
C.NO3- Ca2+ K+ Cl- H+ D.Na+ K+ AlO2- Cl- OH-
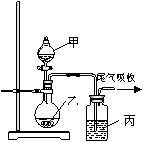 13.用右图所示装置进行实验,表中叙述的结论不正确的是:B
13.用右图所示装置进行实验,表中叙述的结论不正确的是:B
| 甲 | 乙 | 丙 | 结论 | |
| A | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| B | 盐酸 | FeS | 溴水 | 还原性:S2->Cl->Br- |
| C | 浓盐酸 | KMnO4 | KBr溶液 | 氧化性:KMnO4>Cl2>Br2 |
| D | 水 | 电石 | 溴水 | 乙炔可与溴水反应 |
26.(10分)下图是中学中常见的物质间化学反应关系图,其中A的焰色呈黄色,E、F为有刺激性气味的气体,G为含两种强酸的溶液,H为既难溶于水也难溶于酸的白色固体。
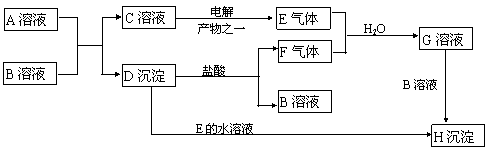 |
请回答:
(1) 写出下列物质的化学式:A H
(2) 写出C→E的化学方程式:
(3) 写出下列反应的离子反应方程式:
D→F+B:
E+F+H2O→G:
21、(1) A 、Na2SO3 H、BaSO4
电解
(2) 2NaCl + 2H2O===== 2NaOH +H2↑+Cl2↑
(3) BaSO3 + 2H+ ==== Ba2+ +SO2↑+ H2O
SO2 +Cl2+ 2H2O === 4H+ +SO42-+2Cl-
27.(12分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,确定一定存在的离子是 ;可能存在的离子是 ;一定不存在的离子是 。
13、(12分)一定存在NH4+ 、K+ 、CO32-、SO42- ;
可能存在Cl-; 一定不存在Ba2+、Mg2+(每空4分)
28.(10分)某化学兴趣小组以含铁的废铝为原料制备硫酸铝晶体,设计如下的实验方案:
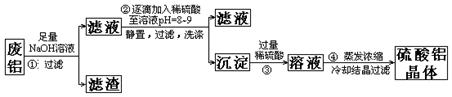
请回答以下问题:
(1)上述实验中多次用到过滤操作,该操作中要用到的玻璃仪器有 ;
(2)步骤②中有洗涤沉淀的操作,如何判断沉淀已洗涤干净:
;
(3)评价步骤②的操作中难以控制之处 ,请你提出一个合理而比较容易操作的实验方案(药品可任选)
;
(4)步骤①中使用的NaOH溶液以4mol/L为宜。某同学称量mgNaOH固体配制
V m L 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号) 。
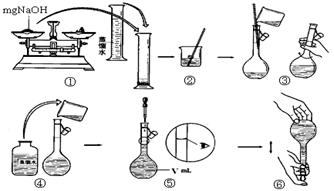
22.(10分)
(1)烧杯、漏斗、玻璃棒;
(2)取最后一次洗涤液,加入几滴BaCl2溶液,若无白色沉淀生成则洗涤干净;
(3)使溶液的p H=8~9难以控制,通入过量CO2气体;
(4)①④⑤(每空各2分)
29.某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
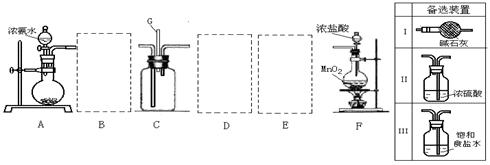
请回答下列问题:
(1)装置F中发生反应的离子方程式 。
(2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择。并将编号填入下列空格。
B__________ D__________ E__________(均填编号)
(4)氯气和氨气在常温下相混就会反应生成氯化铵和氮气,装置C内出现浓厚的白烟并在容器内壁凝结,请设计实验方案鉴定该固体就是氯化铵: 。
(5)从装置C的出气管口处逸出的尾气可能含有污染环境的气体,如何处理? 。
3.答案(共10分)(1)![]() (2分)
(2分)
(2)ABE (2分)
(3)Ⅰ、Ⅱ、Ⅲ (3分)
(4) 取适量该白色固体与浓的氢氧化钠溶液共热,产生能使湿润的红色石蕊试纸变蓝的无色气体;另取适量该白色固体溶于水后加硝酸银溶液,产生不溶于稀硝酸的白色沉淀。(2分)
(5)可将尾气通过装有足量稀氢氧化钠溶液的洗气瓶后再排空。(1分)
附加题欣赏(暂不做):
12.(2007年高考海南化学卷,物质的量浓度)有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)/mol・L-1为( )
(A)(y-2x)/a (B)(y-x)/a (C)(2y-2x)/a (D)(2y-4x)/a
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。2005年的《化学教育》报道了如下实验研究:
实验一、定性研究:
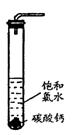 ①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性增强的原因
(2)写出步骤③中第一份及第三份滤液发生的离子方程式:
第一份:
第三份:
(3)依据上述实验可推知,②的滤液中的溶质除CaCl2、HCIO外,还含有______ __ ___;
实验二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加。
请回答:
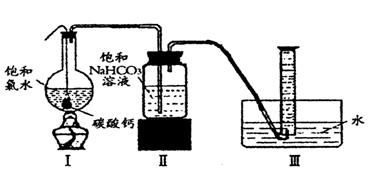 |
(4)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是
22.(1)CaCO3消耗了氯水中的HCl,使Cl2+H2O![]() HCl+HClO平衡向右移动,HClO浓度增大
HCl+HClO平衡向右移动,HClO浓度增大
(2)Ca2+ + HCO3-+ OH-=== CaCO3↓+H2O
Ca2+ + HCO3-=== CaCO3 + CO2↑+ H2O
(3)Ca(HCO3)2(写名称正确同样得分)
(4)在导管末端再连接长导管,使导管的出口接近量筒底部
(5)碳酸钙与氯水反应生成的Ca(HCO3)2再受热时,除生成CO2外,还生成了CaCO3
(6) 从圆底烧瓶蒸出的水蒸气在广口瓶中冷凝、聚集