08届高三级化学上学期模拟考试试题
2008. 2
本试卷分选择题和非选择题两部分,共11页,满分150分;考试用时120分钟。
注意事项:
1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名和考生号填写在答题卡上。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答。答案必须写在答题卡各题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:H:1 C:12 N:14 O:16 S:32 Cl:35.5
Na:23 Mg:24 Al:27 Ca:40 Fe:56 Cu:64
第一部分 选择题 (共70分)
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意。)
1.下列叙述不正确的是( )
A.金刚砂的成分是Al2O3,可用作砂纸、砂轮的磨料
B.水晶和玛瑙的主要成分都是SiO2
C.含硅的钢具有良好的导磁性
D.太阳能电池可用硅材料制作,其应用有利于环保、节能
2. NA代表阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,22.4LCHCl3中含有氯原子数目为3NA
B.18 g D2O中含有的质子数目为10NA
C.7gCnH2n中含有的氢原子数目为NA
D.1 L0.5mol/LNa2CO3 溶液中含有的CO32-数目为0.5NA
3.下列说法正确的是( )
A.乙烯的结构简式可以表示为CH2CH2 B.苯、乙醇和乙酸都能发生取代反应
C.油脂都不能使溴的四氯化碳溶液褪色 D.液化石油气和天然气的主要成分都是甲烷
4. 金属钛对体液无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关![]() 和
和![]() 的说法中正确的是( )
的说法中正确的是( )
A. ![]() 和
和![]() 原子中均含有22个中子
原子中均含有22个中子
B. ![]() 和
和![]() 在周期表中位置相同,都在第4纵行
在周期表中位置相同,都在第4纵行
C. 分别由![]() 和
和![]() 组成的金属钛单质互称为同分异构体
组成的金属钛单质互称为同分异构体
D. ![]() 与
与![]() 为同一核素
为同一核素
5. 巴豆酸的结构简式为CH3CH=CHCOOH ,现有:①水、②溴的四氯化碳溶液、③丁醇、④纯碱溶液、⑤酸性KMnO4溶液。在一定条件下,能与巴豆酸反应的物质组合是( )
A.只有②④⑤ B.只有②③⑤
C.只有②③④⑤ D.①②③④⑤
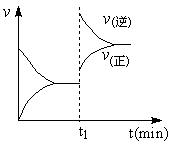
6. 下图为某化学反应速率—时间图。在t1时刻升高温度或增大压强,都符合右图所示变化的反应是( )
A.2SO2 (g)+O2 (g) ![]() 2SO3 (g) ;△H<0
2SO3 (g) ;△H<0
B.4NH3 (g)+O2 (g)
![]() 4NO(g)+6H2O (g) ;△H<0
4NO(g)+6H2O (g) ;△H<0
C.H2 (g)+I2 (g) ![]() 2HI (g) ;△H>0
2HI (g) ;△H>0
D.C (s)+H2O
(g) ![]() CO (g)+H2 (g) ;△H>0
CO (g)+H2 (g) ;△H>0
7. 肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气。已知:N2(g) + 2O2(g)=N2O4(g) △H=+ 8.7kJ/mol
N2H4(g) + O2(g)=N2(g) + 2H2O(g) △H=–534 kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
A. 2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–1076.7 kJ/mol
B. N2H4(g) + ![]() N2O4(g)
=
N2O4(g)
=![]() N2(g)
+ 2H2O(g) △H=–1076.7 kJ/mol
N2(g)
+ 2H2O(g) △H=–1076.7 kJ/mol
C. 2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–542.7 kJ/mol
D. 2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–1059.3 kJ/mol
8.下列说法中正确的是
A. ⅠA、ⅡA族元素的原子,其半径越大,越难失去电子
B. 所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等
C. 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
D. 原子及其离子的核外电子层数等于该元素所在的周期数
9. 在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g) ![]()
![]() N2(g)+CO2(g) △H=-373.2kJ·mol-1 ,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g) △H=-373.2kJ·mol-1 ,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时增大压强
10. 化学实验设计和操作中必须十分重视安全问题和环境保护问题。下列实验问题处理方法不正确的是
① 制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
② 在气体发生装置上直接点燃一氧化碳气体时,必需要先检验一氧化碳气体的纯度。最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声。
③ 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
④ 给试管中的液体加热时不时移动试管或加入碎瓷片,以免暴沸伤人
⑤ 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
⑥ 配制浓硫酸时,可先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
A. ①② B. ②⑥ C. ③⑤ D. ②③
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分。)
11. 禽流感是一种由甲型流感病毒(H5N1)的一种亚型引起的传染性疾病,被国际兽疫局定为甲类传染病。2005年10月25日国家根据禽流感疫情,在疫区到处洒上了石灰,甚至在树上也洒上了石灰,很是醒目。根据有关的化学知识判断下列说法中不正确的是( )
A.石灰之所以可以杀灭H5N1亚型高致病性禽流感病毒,是由于石灰与水反应产生的氢氧化钙显强碱性,病毒为蛋白质,可以使蛋白质变性,而使病毒失去活性
B.饱和石灰水中加入生石灰,在温度不变的情况下,pH不变
C.饱和石灰水中加入生石灰,在温度不变的情况下,Ca2+的物质的量不变
D.给饱和石灰水溶液升高温度,c(Ca2+)的浓度不变
12. X、Y是元素周期表ⅦA族中的两种元素。下列叙述能说明X的非金属性比Y强的是( )
A.X原子的电子层数比Y原子的电子层数多
B.Y的单质能将X从NaX的溶液中置换出来
C.X的单质比Y的单质更容易与氢气反应
D.同浓度下X的氢化物水溶液比Y的氢化物水溶液的酸性强
13.下列溶液中,有关离子一定能大量共存的是( )
A.能使石蕊呈蓝色的溶液中: Na+、I-、Cl-、NO3-
B.能使甲基橙呈黄色的溶液中:K+、SO32-、SO42-、ClO-
C.能使pH试纸变红色的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+
D.能跟金属铝反应生成氢气的溶液中:NH4+、Al3+、Cl-、SO42-
14. 相等物质的量的KClO3分别发生下述反应:①有MnO2催化剂存在时,受热分解得到氧气;②若不使用催化剂,加热至470℃左右,得到KClO4和KCl。下列关于①和②的说法正确的是( )
A. 都属于氧化还原反应 B. 发生还原反应的元素不同
C. 发生氧化反应的元素相同 D. 生成KCl的物质的量不同
15. 下列反应的离子方程式正确的是
A. 溴化亚铁溶液中通入过量氯气: Fe2+ + 2Br- + 2Cl2= Fe3+ + Br2 + 4Cl-
B. 碳酸氢钙溶液中加入过量氢氧化钠溶液 Ca2+ + HCO3-+ OH-= CaCO3↓+ H2O
C. 氯化铝溶液中加入过量氨水 Al3+ + 3OH- = Al(OH)3↓
D. 澄清石灰水中通入过量CO2 OH- + CO2 = HCO3-
16.几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
下列叙述正确的是( )
A. 离子半径大小:r(M3+)>r(T2-)
B. R的氧化物对应的水化物可能具有两性
C. X单质可在氧气燃烧生成XO3
D. L、X形成的简单离子核外电子数相等
17. 常温下将NaOH稀溶液与CH3COOH稀溶液混合,不可能出现的结果是( )
A. pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
B. pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)
C. pH=7,且c(CH3COO-)>c(Na+)>c(H+)=c(OH-)
D. pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
18. 有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
19. 室温下,pH相同体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
A. 加水稀释2倍后,两溶液的pH均减小
B. 使温度都升高20℃后,两溶液的pH均不变
C. 加适量的醋酸钠晶体后,两溶液的pH均增大
D. 加足量的锌充分反应后,醋酸产生的氢气比盐酸多
20.某同学按右图所示的装置进行电解实验。下列说法正确的是( )
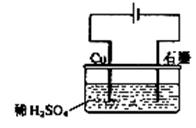 A.电解过程中,铜电极上有H2产生
A.电解过程中,铜电极上有H2产生
B.电解初期,主反应方程式为:Cu+H2SO4![]() CuSO4+H2↑
CuSO4+H2↑
C.整个电解过程中,H+的浓度不断增大
D.电解一定时间后,石墨电极上有铜析出
第二部分 非选择题 (共80分)
三、(本题包括3小题,共30分)
21、(10分)(1)向H2O2溶液中滴加FeCl3溶液,可发生下列反应:
H2O2+2Fe3+=2Fe2++ O2↑+2H+, H2O2+ 2Fe2++2H+ =2Fe3++ 2H2O 。
在以上反应中Fe3+实际上起着 作用,总反应式为 。
(2) I2与Fe3+一样也可以发生上述类似反应,类比(1)在下面填入合适的化学反应方程式:
H2O2+I2=2HIO, 。
总反应式为 。
(3)在硫酸和KI的混合溶液中加入足量的H2O2,放出大量的无色气体,溶液呈棕色,并可使淀粉变蓝色。该反应的离子方程式为: 。
(4)铁酸钠(Na2FeO4)可作为一种新型净水剂,在反应中Na2FeO4被还原为Fe3+离子,请简述铁酸钠之所以能净水,除了具有强氧化性,能消毒杀菌外,另一原因是
。
(5)铁酸钠的制备常用氧化铁在碱性溶液中与硝酸钠反应制得:
Fe2O3 + NaNO3 + NaOH → Na2FeO4 + NaNO2 + H2O
配平化学方程式,并标出电子转移的方向和数目。
Fe2O3 + NaNO3 + NaOH — Na2FeO4 + NaNO2 + H2O
22、(8分)某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。
(1)提出假设:该反应的气体产物全部是二氧化碳。
(2)设计方案:如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
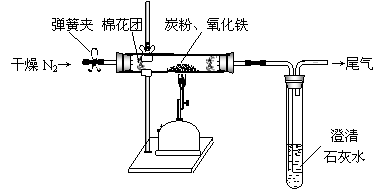
(3)查阅资料:氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气。
请写出该反应的离子方程: 。
(4)实验操作及实验现象:
①按上图连接装置,并检查装置的气密性,称取3.20g氧化铁与2.00g炭粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水变浑浊;
④待反应结束,再通一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g。
(5)数据处理,经计算,参加反应的碳元素质量为0.48g氧元素为0.96g。得出原假设不成立,理由是 。
(6)得出结论:根据数据处理结果判断该实验中发生的化学方程式为:
。
(7)为了保护环境,充分利用原料,实现绿色化学,请你根据实验得出的结论,应对该实验装置进一步完善,你的措施是 。
23、(12分)铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4·5H2O呈蓝色等。研究性学习小组甲为检测实验室的Cu2O试样中是否含有Cu进行了认真的探究。
Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生自身氧化还原反应(Cu2O+2H+=Cu+Cu2++H2O)。
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察是否有残渣
方案3:称得干燥坩埚的质量为a g ,取红色试样置于坩埚中称得总质量为b g,在空气中充分灼烧至完全变黑,并在干燥器中冷却,再称量。如此反复多次直到质量不变,称得最后质量为c g。分析数据,作出合理判断。
(1)请你评价方案1和方案2。如果你认为该方案合理,请简述其工作原理;如果你认为该方案不合理,请简述原因。
。
(2)方案3中,如果a、b、c的关系符合c= 可确认红色粉末是Cu2O。
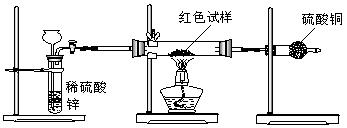 Ⅲ.研究性学习小组乙,设计了新的探究方案,装置如图所示。
Ⅲ.研究性学习小组乙,设计了新的探究方案,装置如图所示。
(3)简述新探究方案中,气体发生装置的气密性如何检验(操作、现象、结论):
。
(4)你认为依据新方案测定上述红色试样成分必须获得下列哪些物理量:(选填序号) 。
①通入氢气体积;②反应前,红色试样+硬质试管的总质量;③完全反应后红色固体+硬质试管的总质量;④实验前,干燥管(含药品)的质量;⑤硬质试管质量;⑥锌粒质量;⑦稀硫酸中含溶质的量;⑧实验后,干燥管(含药品)的质量
(5)有人提出,在氢气发生器与硬质试管之间应加一个干燥装置,你认为 (选填“需要”或“不需要”),简述理由 。
四、(本题包括3小题,共32分)
24、(10分)钼(元素符号Mo)是银灰色的难熔金属,常见化合价为+6、+5、+4,常温下钼在空气中很稳定,高于600 ℃时很快地氧化生成三氧化钼(MoO3);
辉钼精矿(主要成分为MoS2)是生产钼的主要原料。制取过程包括氧化焙烧,三氧化钼、钼粉和致密钼的制取等主要步骤,工艺流程如图:
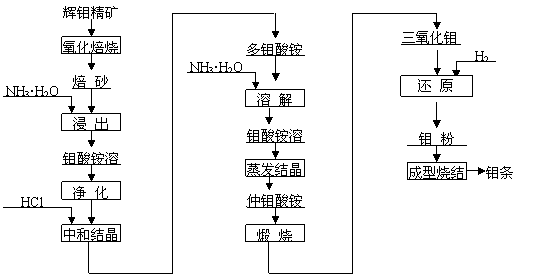 |
(1).辉钼精矿在600℃下进行氧化焙烧 转化为MoO3,同时产生SO2气体。主要反应的化学方程式为: 。钼冶炼厂对大气的污染主要来自于 ,你认为利用并处理该副产物的最好措施是 ;
(2)三氧化钼的制取
将焙砂(主要成分:MoO3)用氨水浸出,与氨水反应生成钼酸铵[(NH4)2MoO4]溶液:反应的离子方程式为: ;
该反应: (填是或不是)氧化还原反应。
将所得钼酸铵[(NH4)2MoO4]溶液加热到55~65 ℃,用盐酸调节至溶液的pH为2,搅拌析出多钼酸铵[(NH4)2O·mMoO3·nH2O]晶体;为除去钙、镁、钠等杂质,将多钼酸铵重新溶于氨水形成钼酸铵,使氨挥发后生成仲钼酸铵晶体[(NH4)2O·7MoO3·4H2O],将仲钼酸铵晶体脱水、煅烧得纯度为99.95%的三氧化钼(MoO3)。
(3)金属钼粉的生产:工业上在管状电炉中用氢气分两步还原三氧化钼得到钼粉:
① 在450~650℃下: MoO3 + 3H2 === MoO2 + 3H2O
② 在900~950 ℃下:MoO2 + 2H2 === Mo + 2H2O
根据上述还原原理,你认为还可用 等还原剂还原MoO3得到钼粉。
 25、(10分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
25、(10分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
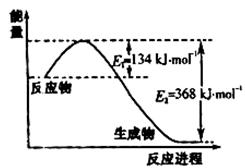
(1)右图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 。
(2)在一定体积的密闭容器中,进行如下化学反应:
![]() N2(g)+3H2(g) 2NH3(g),
N2(g)+3H2(g) 2NH3(g),
其化学平衡常数K与温度t的关系如下表:
| t/K | 298 | 398 | 498 | … |
| K/(mol·L-1)2 | 4.1×106 | K1 | K2 | … |
完成下列问题:
①比较K1、K2的大小;K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保护不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出墁酸肼第一步水解反应的离子方程式 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
C.2 c(N2H62+)+ c([N2H5·H2O+])+c(H+)= c(H+)+c(OH-)
D.c(N2H62+)> c(Cl-)>c(H+)>c(OH-)>
 26、(10分)中国的二氧化硫排放量居世界第一。因此国家环保总局“2006年环境监测公报”指出,减少SO2的排放和生活废水的处理是我国“十一五”期间环境保护的主要任务。请回答下列问题:
26、(10分)中国的二氧化硫排放量居世界第一。因此国家环保总局“2006年环境监测公报”指出,减少SO2的排放和生活废水的处理是我国“十一五”期间环境保护的主要任务。请回答下列问题:
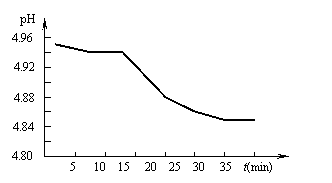
Ⅰ.SO2的排放是造成酸雨的主要因素之一。某地区酸雨的pH随时间的变化如右图所示。请用化学方程式表示该变化的原因
。
Ⅱ.(1)工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,工业上采用了新型氨法烟气脱硫技术采用氨吸收烟气中SO2,该技术的优点是 。
(2)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个反应的化学方程式:
; 。
(3)为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及到的化学反应为:SO2+2CO=2CO2+![]() Sx 、CO+
Sx 、CO+![]() Sx=COS、
Sx=COS、
2COS+SO2=2CO2+![]() Sx 。其中COS分子的空间构型为 。
Sx 。其中COS分子的空间构型为 。
五、(本题包括1小题,10分)
27、(10分)已知:
|
|
![]()
![]()
![]()
![]()
![]() R—CH2—C—CH2—R’
R—CH2—C—CH2—R’
|
|
|
|
已知:A的结构简式为:CH3—CH(OH)—CH2—COOH ,现将A进行如下反应,B不能发生银镜反应, D是食醋的主要成分, F中含有甲基,并且可以使溴水褪色。
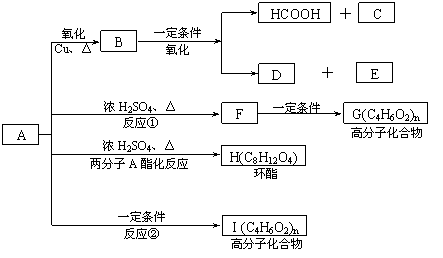 |
(1)写出C、E的结构简式:C_________ _、E_______ ;
(2)反应①和②的反应类型:①____________反应、②____________ 反应;
(3)写出下列化学方程式:
② F→G:_________________________________________________ ;
③ A→H:_________________________________________________ ;
六、选做题(本题包括2小题,每小题10分,考生只能选做一题。28小题为“有机化学基础”内容的试题,29题为“物质结构与性质”内容的试题)
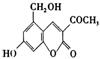
|
肾功能衰竭。“亮菌甲素”的结构简式为 ,它配以辅料丙二
|
成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强
的毒性。请回答下列问题:
(1)“亮菌甲素”的分子式为 。
(2)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。写出其属于醇类的同分异构体的结构简式 。
(3)下列有关“亮菌甲素”的叙述正确的是 (填序号)。
A.“亮菌甲素”能与H2发生加成反应
B.不能使酸性KMnO4退色
C.“亮菌甲素”分子中含氧官能团只有2种
D.1mol“亮菌甲素”最多与2molNaOH反应
(4)核磁共振仪可以测定有机物分子中处于不同化学环境的氢原子及相对数量。氢原子在分子中的化学环境不同,在核磁谱图中就处于不同的位置,化学环境相同的氢原子越多,波谱峰积分面积越大(或高度越高)。核磁共振氢谱分析,发现二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1。又知二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,1mol二甘醇与足量的金属钠反应生成1molH2。写出二甘醇与乙酸(按物质的量之比1:1)反应的化学方程式 。
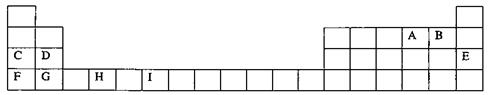
29、(10分)下表为周期表的一部分,其中的字母代表对应的元素
|
请回答下列问题:
(1)写出元素I的基态原子的价电子排布式 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族。
(2)请列举F的金属性比C强的实验事实: ,并用原子结构理论解释其原因:
。
(3)在标准状况下,根据M=m/n测定B的气态氢化物的相对分子质量,结果发现,测定结果总比理论值高,其原因是 。
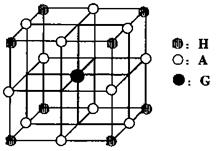
(4)H、A、G三种元素形成的晶体是一种矿物的主要成分,其晶胞结构如下图,则该晶体的化学式为 ;在该晶体中,G离子的配位数为 。
|