08�������ѧ��һѧ���������ۺ�ѵ����14��
1������̽�������ص���Ϣ�����������ϴ���������[Goethite����ѧʽ��FeO(OH)]�ͻƼ�����[Jarosite]���Ӷ�֤�����DZ����������ڹ�ˮ����һ���ֱ��������ձ�����Ϊ2004����ʮ������֮�ס���֪���ֿ��������ļ�̬��ͬ����Ƽ�����{��ѧʽ��Ϊ��KFe3(SO4)2(OH)n}��nֵΪ
A��4��������������������������B��5�������� C��6���������������������������� D��7
2����5.4g Al Ͷ�뵽200.0mL 2.0mol��L��1��ij��Һ����������������ַ�Ӧ���н���ʣ�ࡣ����Һ����Ϊ
A��HNO3��Һ�� B��Ba(OH)2��Һ�� C��H2SO4��Һ����D��HCl��Һ
3������������ͨ�����Ϸ�Ӧֱ���Ƶõ��ǣ���FeCl2 �� ��H2SO4 ������NH4NO3���� ��HCl
A��ֻ�Т٢ڢ� B��ֻ�Тڢۡ���C. ֻ�Т٢ۢܡ�����D.ȫ��
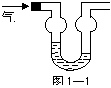 4��˫��ϴ������һ�ֶ���;������������ȥ�����ʡ��������������գ��ܷ�ֹ��������ʵ�������ͼ1��1����ˮ��������ij����ʱ�����Σ����ݱ�1��1�ж�������ı�����������
4��˫��ϴ������һ�ֶ���;������������ȥ�����ʡ��������������գ��ܷ�ֹ��������ʵ�������ͼ1��1����ˮ��������ij����ʱ�����Σ����ݱ�1��1�ж�������ı�����������
A��Cl2�� �� B��HCl���� C��H2S�� ����D��CO2
��֪������ܽ�ȷֱ�Ϊ��
| ���� | Cl2 | HCl�� | H2S�� | CO2 |
| �ܽ��1��X��� | 1��2 | 1��500 | 1��2.6 | 1:1 |
5����NA��ʾ�����ӵ�������ֵ������˵������ȷ���ǣ�
A�����CuCl2��Һ����������16gͭʱ���缫��ת�Ƶĵ�����ΪNA
B����״���£�2.24 L��ȩ��ȫȼ������CO2������Ϊ0.2 NA
C�����³�ѹ�£�22.4 L CH4�����й��ۼ�����Ϊ4NA
D��28g��ϩ�;���ϩ�Ļ������ȫȼ������CO2������Ϊ2 NA
6��ij��ɫ��Һ��NH4HCO3�����ܲ������壬����Һ�п��ܴ���������������ǣ�
A��Cl����Mg2����H����Cu2����SO![]() �� B��Na����Ba2����NO3����OH
�� B��Na����Ba2����NO3����OH![]() ��SO
��SO![]()
C��MnO![]() ��K����Cl����H+��SO
��K����Cl����H+��SO![]() �� D��K����NO
�� D��K����NO![]() ��SO
��SO![]() ��OH����Na��
��OH����Na��
7���������ӷ�Ӧ����ʽ��ȷ����
A��KHCO3��ˮ�⣺HCO3-��H2O![]() H3O++CO32-
H3O++CO32-
B��NaHSO4��Һ��Ba(OH)2��Һ��ϳ����ԣ�2HSO4��+Ba2++2OH��=BaSO4��+SO42��+2H2O
C�����������ۼ��뵽������ϡ�����У�3Fe+8H++2NO3��=3Fe2++2NO��+4H2O
D��̼�������Һ�м�������ʯ��ˮ��Ca2+��HCO3����OH-= CaCO3����H2O
8��FeS2�ڿ����г��ȼ�յĻ�ѧ����ʽΪ4FeS2 + 11O2 2Fe2O3 + 8SO2����agFeS2�ڿ����г��ȼ�գ���ת��N�����ӣ����ӵ�����(NA)�ɱ�ʾΪ��
�� A��120N��a�� B��120a��11N����C��11a��120N����D��120N��11a
9����ѧ��Ԥ�ԣ�C3N4����ܿ��ܾ��бȽ��ʯ�����Ӳ�ȣ���ÿ��ԭ������������8�����ȶ��ṹ�������й���C3N4�����˵����ȷ���ǣ�
A��C3N4 ��������Ƿ��Ӿ��壬��������ͨ�����ۼ����
B��C3N4 ���������ԭ�Ӿ��壬���нϸߵ�Ӳ��
C��C3N4 ������ÿ��Cԭ������4��Nԭ�ӣ���ÿ��Nԭ������3��Cԭ��
D��C3N4 ������N���������Ӿ�����ɼ�
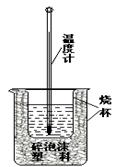 10����10�֣�ʵ������������ͼװ�ý����к��ȵIJⶨ���ش��������⣺
10����10�֣�ʵ������������ͼװ�ý����к��ȵIJⶨ���ش��������⣺
�ٸ�ͼ��������δ������������������������ ������������������ ��
���ڲ�����ȷ��ǰ��������к��Ȳⶨ��ȷ�ԵĹؼ������������� ��
�������0.5 mol/L��������������ƹ������ʵ�飬��ʵ����������ġ��к��ȡ������������ƫ����ƫС���������䡱����ԭ�������������������� ��
11����10�֣� ����500 mL0.2 mol��L-1��FeSO4 ��Һ��ʵ����������У�
��������ƽ�ϳ�ȡa���̷�(FeSO4 ��7H2O)�����������ձ��У�����������ˮʹ
����ȫ�ܽ⡡���� �ڽ�������Һ�ز�����ע��500 mL����ƿ��
�ۼ���������ƿ�м�ˮ��Һ���̶���1��2cm�������ý�ͷ�ιܼ�����ˮ��
��Һ��ײ���̶������� ��
��������ˮϴ���ձ��Ͳ�����2��3�Σ�ÿ��ϴҺ��ת������ƿ�� �ݽ�����ƿ���������ҡ��
����д���пհף� (1)a���̷���ʵ������Ϊ�������� ��������
(2)���������������ȷ˳��Ϊ�������� ����������������������������
(3)������ʱ��©����ܣ���ʹ������Һ��Ũ���������� (�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��(4)��������ˮʱ���������̶��ߣ������������������� ��������������������������
�������������ʱ����Һ���ڽ���ƿ�⣬������������������ ��������������������������
12����14�֣������¡��á��ġ��š��ơ������ɶ�����Ԫ����ɵ��������ʣ����У¡��á����ǵ��ʣ������£¡��á���Ϊ���壻�����ʵ���ɫ��Ӧ�ʻ�ɫ������ͼ�з�Ӧ�ڵIJ��ֲ���δ��ʾ��������
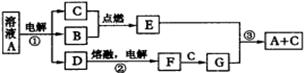
������ͼ��ʾת����ϵ�ش�
��1�����ⶨG�������ӻ���������ʽΪ___________��
��2��д��Ӧ�ڵĵ缫��Ӧʽ��
����______������������
�� ��������������������������
��
��3����Ӧ�۵Ļ�ѧ����ʽΪ����������������
___________����������������������
��
��4����Ӧ�ٵ����ӷ���ʽΪ___________���������������������� ��
��5�������������к��й��ۼ�����___________������������ ���û�ѧʽ�ش�
13.(8��) ��Դ��������ᷢչ���������ʻ������ڵ�������Դͬ��Ϣ������һ�����ִ�����������֧����
��1��Ϊ�˽�������β���Դ�������Ⱦ�������йز������ü״����Һ��ʯ������Ϊ��������ȼ�ϡ���֪����25�桢101kPa�£�1g�״�ȼ������CO2��Һ̬ˮʱ����akJ����д����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽ����������������������������������������������������
��2���ⶨ��ҵ�״���CH3OH�����������ɰ��·���ȡ0.1000g��ҵ�״���Ʒ��������H2SO4�ữ����20.00mL 0.2000mol/L��K2Cr2O7��Һ������0.3000mol/L (NH4)2Fe(SO4)2����Һ�ζ�����ȥ�˱�Һ20.00mLʱ���պõ���ζ��յ㡣
��֪��CH3OH��Cr2O72-��8H����CO2����2Cr3+��6H2O��
��д��H2SO4�ữ��K2Cr2O7��Һ��(NH4)2Fe(SO4)2��Һ��Ӧ�����ӷ���ʽ��
��������������������������������������������������
����˹�ҵ�״���CH3OH������������
�ۺ�ѵ����14���ο���
1��C��2��D�� 3.D��4.B�� 5.D��6.D�� 7��D�� 8��D����9��BC
10. �� ���β������� ��ĭ���ϸǡ��� ���װ�õı���Ч������ƫ�� ����NaOH����ˮ����
11.��1��27.8�� ��2���٢ڢܢۢݡ� ��3��ƫ�͡� ��4���������� ��������
12. ��1��Na��[��H]����2�֣�
������2��������4�ϣ�����4��������������2��2�ϣ�2�֣� ������4��a����4������4Na��2�֣�
������3��NaH��HCl��NaCl����2����2�֣���4��2Cl- + 2H2O===
2OH- + H2��+ Cl2��
������5����2��Cl2��NaOH��HCl ��4�֣�
13.��1��CH3OH��l����3/2O2��g����CO2��g����2H2O��l���� ��H������725.8kJ/mol��2�֣�
��2�� ��Cr2O72-��6Fe2����14H����2Cr3����6Fe3����7H2O��������96%�� ��4�֣�