������ѧ��ϰ��Ԫ���ԣ�6��������Ԫ�� ��������
���Ծ��ֵڢ����ѡ���⣩�͵ڢ������ѡ���⣩�����֣�����108�֣�����ʱ�䣺60���ӣ������õ���ԭ������ H��1��C��12��O��16��S��32��N:14��Cu:64��Fe��56 Ag��108
�ڢ����ѡ���⣬��48�֣�
һ��ѡ���⣨ÿС��ֻ��һ��ѡ��������⣬ÿС��4�֣���12�⣩
1.(2007��߿�ȫ�����۾�I)�����йػ��������˵����ȷ����
(A)ȼúʱ��������ʯ��ʯ���ɼ��ٷ�����SO2����
(B)�����������������10��4%�Ŀ������������彡��
(C)pH��5.6��7.0֮��Ľ�ˮͨ����Ϊ����
(D)���ϳ�ϴ�Ӽ����ڱ�ϸ���ֽ⣬�ʲ��ᵼ��ˮ����Ⱦ
2��(2007��߿��㶫��������������)��ˮ��������Ҫ�����У����кͷ����ڻ�ѧ����������������ԭ�����ܹ��˷����������ڻ�ѧ��������
(A)�٢ڢۡ��� (B)�٢ڢܡ��� (C)�ڢۢܡ��� (D)�٢ڢۢ�
3��(2007��߿����ϻ�ѧ��������)����ʵ������������������
(A)������������ȼ��������ɫ����
(B)���ȵ���˿��������ȼ�գ��������䣬���ɺ�ɫ�������
(C)��ȼ�����������о���ȼ�գ���������ɫ����
(D)���ڿ�����ȼ�գ�������ɫ�Ļ��棬���ɵ���ɫ����
4��(2007��߿��Ϻ���ѧ������)�й�����ȼ��ʱ������ɫ�����������
(A)������������ȼ�� �� ��ɫ����(B)���ڿ�����ȼ�� �� ��ɫ
(C)�Ҵ��ڿ�����ȼ�� �� ����ɫ����(D)����������ȼ�� �� ��ɫ
5��(2007��߿��㶫����������)ij��Һ�п��ܺ���SO42 ����CO32 ����Cl����Ϊ�˼��������Ƿ���SO42 ������BaCl2��Һ�⣬����Ҫ����Һ��
(A)H2SO4����(B)HCl���� (C)NaOH���� (D)NaNO3
6.��06�㶫6������þ���Ͻ��ĩ�ֱ�������4�ֹ�������Һ��ַ�Ӧ���ų�����������
A��2mol��L-1H2SO4�� B��18 mol��L-1H2SO4��ҺC��6 mol��L-1KOH��ҺD��3 mol��L-1HNO3��Һ����
7. ��������ʵ�Ľ��ʹ������
A�������Ǽ���ŨH2SO4����ַ�������˵��ŨH2SO4������ˮ��
��B����50mLl8mol��L��H2SO4��Һ�м�������ͭƬ���ȳ�ֺ���ԭ��H2SO4�����ʵ���С��0��45mol
C�������£�ŨH2SO4�����������������棬˵������Ũ�����Ӧ
D����ӦCuSO4+H2S===CuS+H2SO4�ܽ��У�˵����ͭ�Ȳ�����ˮ��Ҳ������ϡ����
8. ���й���Ũ�����������ȷ���ǡ�������������������������������������������������������������������
���� A��Ũ���������ˮ�ԣ������ʹ����̿����
������B��Ũ�����ڳ����¿�Ѹ����ͭƬ��Ӧ�ų�������������
���� C��Ũ������һ�ָ�������ܹ����ﰱ�������������塡
������D��Ũ�����ڳ������ܹ�ʹ�������Ƚ����ۻ�
9.��֪I����Fe2+��SO2��Cl����H2O2���л�ԭ�ԣ�������������Һ�л�ԭ��ǿ����˳����SO2��I����H2O2��Fe2+��Cl���������з�Ӧ�����ܷ�������
A.2Fe3++SO2+2H2O====2Fe2++SO![]() +4H+���� B.2Fe2++Cl2====2Fe3++2Cl��
+4H+���� B.2Fe2++Cl2====2Fe3++2Cl��
C.I2+SO2+2H2O====H2SO4+2HI������������ D.H2O2+H2SO4====SO2+O2+2H2O
10. .���������ʵ���Ũ�ȶ�Ϊ0.1 mol��L��1��KCl��(NH4)2SO4��NH3��H2O��H2SO4��ƿ��ɫ��Һ������ʵ�鷽����ѵ���
A.��pH��ֽ���𡡡����������������������������������������������� B.�ֱ�������ζ��pH��ֽ����
C.�ֱ���BaCl2��NaOH��Һ���𡡡����������������������� D.��Ba(OH)2��Һ����
11. �������ӷ���ʽ��д��ȷ���ǣ�
A����Ba(OH)2��Һ���ϼ���KAl(SO4)2��Һ�з�Ӧ���������ʵ������
3Ba2+ + 6OH�C + 2Al3+ + 3SO42�C== 3BaSO4��+ 2Al(OH)3��
B������������Һ�м��������ˮ��Ag+ + NH3��H2O =AgOH����+ NH4+
C��CuSO4��Һ��Ba(OH)2��Һ��ϣ�Ba2+ + SO42�C == BaSO4��
D���������������������Fe(OH)3 + 3H+ = Fe3+ + 3H2O
12. .������Һ�У���������SO2��CO2������ǡ���������������������������������
��ʯ��ˮ����KMnO4��Һ������ˮ�����ữ��Ba(NO3)2��Һ����Ʒ����Һ
A���٢ڢۢݡ�����B���ڢۢܢݡ���������C��ֻ�Т١���������D���٢�
��I��������������� �������� ��������������������� ������
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| �� |
�ڢ������ѡ���60�֣�
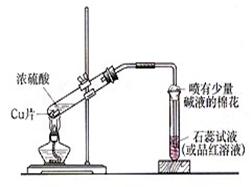 13.(18��)ʵ���ҳ�������װ��������ͭ��Ũ���ᷴӦ��һϵ��ʵ�顣��1������ʲô������ж�ͭ��Ũ���ᷴӦ��SO2���ɡ�_____________��������������������������������������
��
13.(18��)ʵ���ҳ�������װ��������ͭ��Ũ���ᷴӦ��һϵ��ʵ�顣��1������ʲô������ж�ͭ��Ũ���ᷴӦ��SO2���ɡ�_____________��������������������������������������
��
����ʲô������ж�ͭ��Ũ���ᷴӦ������ͭ����_____________________________________________________��
д����װ���з�������Ҫ��Ӧ�Ļ�ѧ����ʽ_____________________________________________________��
��2������ʵ�����н������ʵ��ʱ�����ˣ�1��С����ָ����ʵ�������⣬�����Թ۲쵽����������ʵ��������д�����֣� ____________���������������������������������������� ,
________________���������������������������������������� ��
��3��װ���ҵ��Թܿڲ�����һ�Ž��м�Һ����������ͨ���ǽ��б���̼������Һ��д�����з�����Ӧ�Ļ�ѧ����ʽ___________________________________��
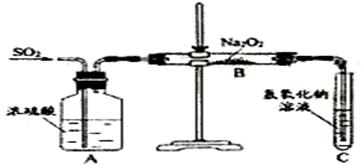
14. (12��)������ʵ��С���ͬѧΪ̽�������������������ķ�Ӧ����������ͼ��ʾ��װ�ý���ʵ�顣ͨ��SO2���壬���������ľ�������Թ�C�У�ľ����ȼ��
������ ��ش��������⣺
������ (1) ��1С��ͬѧ��ΪNa2O2��SO2��Ӧ������Na2SO3��O2���÷�Ӧ�Ļ�ѧ����ʽ�ǣ������� ���������������������������� ��������������������������
������ (2) �����һ��ʵ�鷽��֤��Na2O2��SO2��Ӧ���ɵİ�ɫ�����к���Na2SO3��
������ ���������������������������������������������������� ��
(3) ��2С��ͬѧ��ΪNa2O2��SO2��Ӧ������Na2SO3��O2�⣬����Na2SO4���ɡ�Ϊ�����Ƿ���Na2SO4���ɣ�������������·�����

������ ���������Ƿ�������������� �����Ҫ˵�����ɣ�
������ �� ���������������������������������� ������������������������������ ��
15.(2007��߿�ȫ�����۾�I��15��)A��B��C��D��E��Ϊ������ˮ�Ĺ��壬������ǵ�������
| ������ | Na�� | Mg2�� | Al3�� | Ba2�� | |
| ������ | OH�� | Cl�� | CO32 �� | SO42 �� | HSO4�� |
�ֱ�ȡ���ǵ�ˮ��Һ����ʵ�飬������£�
��A��Һ��B��Һ��Ӧ���ɰ�ɫ����������������E��Һ��
��A��Һ��C��Һ��Ӧ���ɰ�ɫ����������������E��Һ��
��A��Һ��D��Һ��Ӧ���ɰ�ɫ�������������������
��B��Һ������D��Һ��Ӧ���ɰ�ɫ�������������D��Һ����������С��������ʧ��
�ݴ��ƶ�������A__________��B___________��C__________��D___________��E___________��
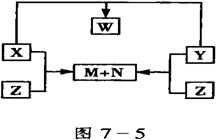 16.��15�֣�������X��Y��Z���ɶ����ڵ�����Ԫ��������϶��ɣ�X��Y��Z֮���ת����ϵ��ͼ7-5��ʾ���ޱ�ʡ�Ե����ʣ�����֪��X��N��W��ΪҺ̬���ʣ���X��N�����Ԫ����ͬ���Իش�
16.��15�֣�������X��Y��Z���ɶ����ڵ�����Ԫ��������϶��ɣ�X��Y��Z֮���ת����ϵ��ͼ7-5��ʾ���ޱ�ʡ�Ե����ʣ�����֪��X��N��W��ΪҺ̬���ʣ���X��N�����Ԫ����ͬ���Իش�
��1������ת����ϵͼ������W�漰���Ļ�����Ӧ������__________________��
��2��X��Y��Z��W�Ļ�ѧʽ�����ǣ�X_________��Y_________��Z____________��W____________��
��3��д��X��Y��X��Z��Ӧ�Ļ�ѧ����ʽ��X+Y��_________________________________��
X+Z��_________________________________��
������ѧ��ϰ��Ԫ���ԣ�6��������Ԫ�� ���������ο���
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| �� | A | A | A | D | B | A | C | D | D | A | A | C |
13. ��1������Ʒ���ʳ���ɫ��������Һ����ɫ��Cu+2H2SO4(Ũ)=CuSO4+SO2��+2H2O��
��2��װ�ü��Թ�����Һ���ɫ���ǣ�װ�ü����Թ��ϲ��а�������Ӧ��ʼʱͭƬ�����ڲ������ݲ�������
��3��Na2CO3+SO2=Na2SO3+CO2��
14. ���𰸡�20. (12��)(1) 2Na2O2��2SO2��2Na2SO3��O2
������ (2) ȡ��ɫ���壬��ϡ���ᣬ������ʹƷ����Һ��ɫ�����塣
������ (3) ��������ϡ�����ܽ������ᱵ����Ϊ���ᱵ�������Ӧ��Ĺ����л�����Na2O2����������ˮ���ܽ�������������������
15. �۴𰸣�A��Na2CO3��B��Al2(SO4)3��C��MgCl2��D��Ba(OH)2��E��NaHSO4[��Mg(HSO4)2]��
16. ��1�����Ϸ�Ӧ����2��![]() ��
��![]() ��
��![]() ��
��![]()
��3��![]()