08届高三化学第一学期联考后综合训练(5)
13.下列说法正确的是 ( )
A.将pH试纸浸在溶液中,观察其颜色变化,跟标准比色卡比较
B.电解饱和食盐水时,阴极室得到氢氧化钠溶液和氢气
C.铁器上镀银,必须把铁器接电源的正极,银接电源负极,用银离子的可溶盐溶液作
电解液
D.用盐酸滴定NaOH溶液的实验中,锥形瓶用水洗后,再用NaOH冲洗2~3次
14.X、Y、Z三种元素,已知X和Y原子核外电子层数相同,Y和Z原子最外层电子数相同,又知三种元素原子最外层电子数总和为14,而质子数总和为28,则三种元素为( )
A.N、P、O B.N、C、Si C.B、Mg、Al D.C、N、P
15.同主族元素所形成的同一类型的化合物,其结构和性质往往相似,化合物PH4Cl是一种无色晶体,下列对它的描述中不正确的是 ( )
A.在加热时此化合物可以分解 B.它是一种共价化合物
C.这种化合物能跟碱发生反应 D.该化合物可以由PH3跟HCl化合而成
16.下列离子方程式中正确的是 ( )
A.亚硫酸氢钙与稀硝酸反应:HSO3-+H+=H2O+SO2↑
B.澄清石灰水与醋酸溶液混合:Ca(OH)2+2CH3COOH=Ca2++2CH3COO-+2H2O
C.氢氧化镁溶于稀硫酸:Mg(OH)2+2H+=Mg2++2H2O
 D.向酸性FeSO4溶液中滴入H2O2:Fe2++H2O2+2H+=Fe3++2H2O
D.向酸性FeSO4溶液中滴入H2O2:Fe2++H2O2+2H+=Fe3++2H2O
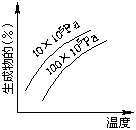
18.由可逆反应测绘出图象如右图,纵坐标为生成物在平衡混
合物中的百分含量,下列对该反应的判断正确的是( )
A.反应物中一定有气体 B.生成物中一定有气体
C.正反应一定是放热反应
D.无法判断出该正反应是吸热反应还是放热反应
19.在第三届东北师大附中体育节上使用的发令枪中所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学反应方程式为:
5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是 ( )
A.上述反应中氧化剂和还原剂的物质的量之比为5:6
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成酸滴(雾) C.上述反应中消耗3molP时,转移电子的物质的量为15mol
D.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
20.X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法不正确的是:( )
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H2YO4
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z>Y>X
22.将等物质的量的X、Y 气体充入一个密闭、体积恒定的容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)![]() 2Z(g);ΔH<0. 当改变某个条件并维持新条件直至新平衡,下表中关于新平衡与原平衡的比较,正确的是 ( )
2Z(g);ΔH<0. 当改变某个条件并维持新条件直至新平衡,下表中关于新平衡与原平衡的比较,正确的是 ( )
| 改变的条件 | 新平衡和原平衡的对比 | |
| A | 升高温度 | X的体积分数变大 |
| B | 体积不变的前提下,充入不参加反应的稀有气体,增大压强 | Z的浓度变大 |
| C | 加入正催化剂 | Y的体积分数变大 |
| D | 充入一定量Y气体 | X的体积分数变大 |
18.(12分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
![]()
(1) 试剂1是 ,加入新制氯水后溶液中发生的离子反应方程式是:
, ;
(2) 加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是 ;
(3) 在实验中发现放置一段时间,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
| 编号 | 猜 想 |
| 甲 | 溶液中的+3价Fe又被还原为+2价Fe |
| 乙 | 溶液中的SCN-被过量的氯水氧化 |
| 丙 | 新制的氯水具有漂白性,将该溶液漂白 |
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确。写出有关的实验操作、预期现象和结论。(不一定填满,也可以补充)
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
19.(10分)游泳池中的水经常要消毒杀菌。某化学兴趣小组对游泳池中使用的消毒剂进行了研究性学习。(1)氯气是游泳池中水体消毒杀菌的常用消毒剂之一,它能消毒杀菌的原因是(用离子方程式表示) 。
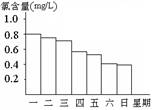 (2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8∶00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5 mg/L至1.0 mg/L之间时,效果最好。右图是该组测定某星期中每天19∶00时游泳池中水的氯含量。根据图示判断,哪几天的天气炎热、阳光强烈,并说明理由 ;
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8∶00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5 mg/L至1.0 mg/L之间时,效果最好。右图是该组测定某星期中每天19∶00时游泳池中水的氯含量。根据图示判断,哪几天的天气炎热、阳光强烈,并说明理由 ;
(3)游泳池也可使用漂白液(主要成份是NaClO)来进行消毒杀菌。与氯气相比较,请写出使用漂白液的优点之一 ;
(4) 广谱消毒剂ClO2已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。若消毒同一游泳池中的水,达到同样的消毒效果,所需ClO2与Cl2的物质的量之比为_____(单位物质的量的物质得到的电子数可以表示该物质的消毒效率)
(5)用于游泳池消毒杀菌的消毒剂还有很多。下列物质中,也可以用于游泳池杀菌消毒的有___________ A、二氧化硫 B、臭氧 C、活性炭 D、高锰酸钾
综合训练(5)参考答案
18.(每空2分,共12分)(1)稀盐酸(或稀硫酸溶液);2Fe2++Cl2=2Fe3++2Cl- ;
Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=[Fe(SCN) 3]);
(2)少量的Fe2+被空气中的氧气氧化;
(3)
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 取少量褪色后溶液,加入KSCN溶液 | 如果溶液变红色,说明乙同学的猜想是合理的;如果溶液不变红色,说明乙同学的猜想是不合理的 |
| 或 | 取少量褪色后溶液,加入FeCl3溶液 | 如果溶液仍不变红色,说明乙同学的猜想是合理的;如果溶液变红色,说明乙同学的猜想是不合理的 |
四.(本题包括1小题,共10分)
19.(每空2分,共10分) (1) Cl2 + H2O == H+ +Cl- + HClO ;
(2) 星期四、星期六 阳光强烈HClO更易分解,致含氯量下降明显;
(3) NaClO更稳定,使用方便、储存和运输等; (4) 2:5; (5) BC