08�������ѧ�����ڵ����ܲ�����
��
�����õ���ԭ������C~12 H~1 O~16 N~14 S~32 Cl~355 Na~23 K~39 Cr~52 Fe~56 Mn~55
ע���뽫I������2BǦ��Ϳ�ڴ���ϣ�II�������ڴ�����ϡ�
I����ѡ���⣨��63�֣�
һ��ѡ���⣨�������9С�⣬ÿС��3�ֹ�27�֣�ÿС��ֻ��һ��ѡ��������⣩
1��2007��9��1�գ�������Ժ�������ҷ���ί����������ʮ�߸���ί���������þ��С����ܼ���ȫ���ж���������ʽ��Ҫ����ȫ����Χ���γ�ȫ����ܼ��ŷ�Χ�������й�������������һҪ����ǣ�������
|
������B���������ϰ�װ����β����ת��װ�ã�ʹ֮�������·�Ӧ��2CO+2NO����2CO2+N2
������C���ڴ����ƹ��Ҵ����͵�ͬʱ���о�����̫������������ȼ�ϵ������
 ������D����ˮ�����硢�������硢���ܷ���ͷ��������У�Ҫ������չ��������
������D����ˮ�����硢�������硢���ܷ���ͷ��������У�Ҫ������չ��������
2����ͼΪ���϶�һ�š��������Ǵ��صĵ�һ������ͼ���ҹ�̽�µ�Ŀ��֮һ��̽������������Ⱥ�3He����Դ����3He���ȫ��������Դ�������Ͻ���15 t���ң��������ϵ�3He������1.0��106 t~1.5��106 t��
���й���3He��˵����������(����)
A��������2�����ӡ���������������
B����4He��Ϊͬλ��
C��������1�����ӡ���������������
D����4He��ͬ��������
3�����������һ�ֳ�Ϊ�����ᡱ������[H(CB11H6Cl6)]��C60��Ӧ��ʹC60���һ�����ӣ��õ�һ���������ӻ�����[HC60]+[CB11H6Cl6]-�������Ӧ��������һ����ѧ��
Ӧ������(����)
A. HCl + NH3 = NH4Cl��������������������������B.SO3 + H2O = H2SO4
C. CH2=CH2 + HCl�� CH3CH2Cl���������������� D.2Na + Cl2 ��ȼ 2NaCl
4�����и���������ָ����Һ���ܴ���������� (����) ����������������������
����ɫ��Һ�У�K+��Cu2+��Na+��MnO4����SO42��
��ʹpH=11����Һ�У�CO32����Na+��AlO2����NO3��
�ۼ���Al�ܷų�H2����Һ�У�Cl����HCO3����NO3����NH4+
������ˮ�������c(OH��)=10��13mol��L��1����Һ�У�Na+��Ba2+��Cl����I��
����ʹpH��ֽ��Ϊ��ɫ����Һ��Na+��C1-��S2-��SO32-
��������Һ�У�Fe2+��Al3+��NO3����I����Cl��
A���٢ڢݡ��� ����B���٢ۢޡ��������� C���ڢܢݡ���������D���٢ڢ�
5���������ʼ�����;����ȷ����(����)
�� A��﮵������һ���ɳ�����ɫ��أ���Ϊ�ʼDZ����ԡ��ƶ��绰�ȵ��ĵ������������
B��ͭ����Һ���ж���������ͭ���������Ƶ��Һ��ũҩ���������������У�ͭҲ��һ
�ֲ���ȱ�ٵ���Ԫ��
C��������ˮ�ࡢ�մɺ�������ǵĹ����β�Ʒ��Ӧ��������������ĸ�������
D������һ����Ҫ�Ļ�����Ʒ���ǵ��ʹ�ҵ���л��ϳɹ�ҵ���������ᡢ��κʹ����
ԭ��
6����Ϥ�����˻���ʹ�õķ���ǹ���õġ���ҩ���ɷ�������غͺ��ף���ײ������������ͬʱ������ɫ������ײ��ʱ�����Ļ�ѧ��Ӧ����ʽΪ��5KclO3+6P=3P2O5+5KCl���������й������������ǣ�������
������ A��������Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ5:6
������ B��������ɫ������ԭ�������ɵ�P2O5��ɫ����С�������̣���ˮ�Ժ�ǿ�����տ�����
������ ��ˮ�֣���������СҺ�Σ�����
������ C��������Ӧ������3molPʱ��ת�Ƶ��ӵ����ʵ���Ϊ15mol
������ D������Ͱ���Ϊͬ���칹�壬����������ҩ�еĺ������ð��״���
7��Ba2+��Ȼ�ж���������ҽ������У�BaSO4ȴ����������ϵͳ��X�����С�Ϊ�˼�ǿ��ȫ�ԣ���ǰ���߳Խ���BaSO4����һ����Һ���Ƴɵĺ�״�����ҺӦ���ǣ����� ��
A��Na2SO4��Һ�� B��ϡHCl����C��NaCl��Һ����D��Na2CO3��Һ
8���������ǵ��Ӳ��ϵ����㣬���Ⱦ��й���Ĵ��ԣ��־���Һ��������ԡ��Ʊ�ʱ�������ʵ���FeSO4��Fe2(SO4)3��Һ��ϣ������Թ���������������Һ����������������Һ���������ɺ�ɫ�ķ�ɢ������ֱ����5.5��36nm�������塣����˵������ȷ����(����)
A�����õķ�ɢϵ������Һ
B�����õķ�ɢϵ�з�ɢ��ΪFe2O3
C����һ��ǿ�ɼ���ͨ���÷�ɢϵʱ����ֹ�����ͨ·
D���÷�ɢϵ�ܲ��ȶ�
9��ͭ����������������ʶ��������ֽ�������Ϊ����ͱ���������Ǯ�ң�����С����ҽ�����֮�ơ��������Ľ����Ա�ͭ��������ǿ����Զ��ԣ�������ʶ��������ij�о���ѧϰС��Ϊ��֤�����Ľ�����Ա�ͭǿ��������������·�����������������������������������
�� ��1����Ƭ��������ͭ��Һ����ͭ����
�� ��2������ͭ��������Ӧ�ֱ�����FeCl3��CuCl2
�� ��3�����������ۺ�ͭ�ۺ�Ũ���ᷴӦ����FeSO4��CuSO4
�� ��4��ͭƬ����FeCl3��Һ��ͭƬ���ܽ�
�� ��5������Ƭ��ͭƬ����ʢ��ϡ������ձ��У����õ������ӣ���Ƭ�������ݲ�������ͭƬ�������ݲ���
�� ��6������Ƭ��ͭƬ����ʢ��Ũ������ձ��У����õ������ӣ���Ƭ�������ݲ�������ͭƬ�������ݲ�����������ƺ������У�������
������ A�����ַ���������������B�����ַ���������������C�����ַ���������������D�����ַ���
����ѡ���⣨�������9С�⣬ÿС��4�ֹ�36�֣�ÿС����һ������ѡ��������⣩
10�����з�Ӧ�����ӷ���ʽ�������(����)
A����̼�������Һ�м��������������
Ca2����2HCO3����2OH��== CaCO3����2H2O��CO32��
B������������ʵ���Ũ�ȵ�����������Һ��̼�������Һ���
Ba2����2OH����NH4����HCO3�� == BaCO3����NH3��H2O��H2O
C���������ƹ�����ˮ��Ӧ�� 2O22��+2H2O == 4OH��+O2��
D��������������Һ��ͨ�������CO2��CO2��2OH��==CO32��+H2O
11����ͼ��һ������Ͷ�������Ĵ������ϵͳ��ԭ��ͼ������е���������Ϊ�缫���м�Ϊ����ѡ����Ĥ���ڵ�طŵ�ͳ��ʱ��Ĥֻ����������ͨ������س䡢�ŵ�Ļ�ѧ��Ӧ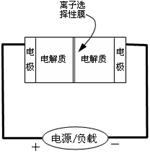 ����ʽΪ��
����ʽΪ��
���й��ڴ˵��˵����ȷ����(����)
A�����Ĺ����е�0.1molNa+ͨ�����ӽ���Ĥʱ������ͨ��
0.1mol����
B����طŵ�ʱ��������ӦΪ��3NaBr��2e����NaBr3��2Na��
C���������������Ӵ��ҵ���ͨ�����ӽ���Ĥ
D���ŵ�����������Ӵ��ҵ���ͨ�����ӽ���Ĥ
12��Ϊʵ��2008�������Ƽ����ˡ�ս�ԣ��ҹ��˷ܼ��������оƬװ��
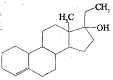 �Ѷ��ͺ������������ɿ�ݼ�ⳣ����16���˷ܼ�����֪ij�˷�
�Ѷ��ͺ������������ɿ�ݼ�ⳣ����16���˷ܼ�����֪ij�˷�
���һ���ϩ����etylestrenol���Ľṹ����ͼ��ʾ��������������ȷ
���ǣ�������
A.�����ʿ�����Ϊ����
B.��Ũ���������£���������ȥһ��ˮ���ӣ������ж���ͬ���칹��
C.��ʹ������Ȼ�̼��Һ��ɫ��������D.�����ʷ����е�����̼ԭ�Ӿ�����
13��NAΪ�����ӵ�����������˵������ȷ���ǣ�������
A������ͭ��ϡ���ṹ��ԭ��أ���ת����NA������ʱ���������������һ��Ϊ11.2 L
B��1mol/L Mg(NO3)2��Һ�к���NO3-����ĿΪ2NA
C�������£�28.0g��ϩ�ͱ�ϩ��������к��е�̼ԭ����Ϊ2NA
D��2.24 L CO2�к��е�ԭ����Ϊ0.3��6.02��1023
14�����볣��(Ka)���ܽⳣ��(Ksp)�ȳ����DZ�ʾ���ж��������ʵ���Ҫ���������й�����Щ���������ô�����ǣ�������
A��Ka(HCN)<Ka(CH3COOH) ��˵����ͬŨ�ȵ�����������Ա���ͬŨ�ȵĴ�����Һ��������
B��CH3COONH4��Һ����Ϊ���ԣ�˵��Ka(CH3COOH)��Kb(NH3��H2O)�������
C��Ksp(AgI)<Ksp(AgCl)���ɴ˿��ж�AgCl(s)+I-=AgI(s)+Cl-��Ӧ�ܹ�����
D��Ksp(Cu((OH)2)<Ksp(AgCl)��������ƶ�AgCl������ϡ���ᣬCu(OH)2Ҳ������ϡ����
15��������أ�K2FeO4����һ�����͡���Ч�����ˮ������������ˮ�����ӷ�Ӧ�ǣ�
4FeO42��+10H2O = 4Fe(OH)3�����壩+3O2��+8OH��
��ҵ�����Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���һ������KOH�Ϳ��Ƶø�����ء��Ʊ��������Ƶ����ַ�������Ҫ��Ӧԭ�����£�
ʪ���Ʊ�����2Fe(OH)3+3ClO��+4OH��= 2FeO42��+3Cl��+5H2O
�ɷ��Ʊ�����2FeSO4+6Na2O2 = 2Na2FeO4+2Na2O+2Na2SO4+O2��
�����й�˵������ȷ���ǣ�������
����A�����������ˮ��Ӧʱ��ˮ������ԭ��Ӧ
����B��ʪ����ÿ����1molNa2FeO4��ת��3mol����
����C���ɷ���ÿ����1molNa2FeO4��ת��4mol����
D��K2FeO4����ˮʱ��������ɱ�������ܳ�ȥH2S��NH3�ȣ���ʹ�������ʳ���
16������ͼ��ֱ��ʾ�йط�Ӧ�ķ�Ӧ�����������仯�Ĺ�ϵ
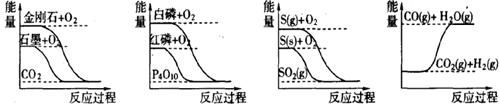
�� �ݴ��ж�����˵������ȷ����(����)
A��ʯīת��Ϊ���ʯ�����ȷ�Ӧ������������
B�����ױȺ����ȶ�
C��S(g)+O2(g)��SO2(g)����H1������ S(s)+O2(g)��SO2(g)����H2������H1����H2
D��CO(g)+H2O(g)��CO2(g)+ H2 (g)����H1��0
17��������ĸ������ܿ��ø���Ч�ʣ�1m3������ʵ������ˮ��������������������ijЩ������ĸ���Ч���������£�
| ���� | MgO | CaO | ZnCl2 | ZnBr2 |
| ������ | 0.008 | 0.2 | 0.8 | 1.1 |
�����������ݣ��ж�����������������(����)
A��CaO�ĸ������ܱ�MgO�á���������������
B��MgCl2�����DZ�CaCl2���õĸ����
C������������������ӶԸ�������ܵ�Ӱ��������ӶԸ�������ܵ�Ӱ��С��������
D������Ч�ʿ��������������������ӵİ뾶��С�й�
18�������£������й�������ȷ����(����)
A��Na2CO3��Һ�У�2c(Na��)��c(CO32��)��c(HCO3��)��c(H2CO3)
B��NaB��Һ��pH��8��c(Na��)��c(B��)��0.99��10��6mol/L
C��pH��ȵĢ�NH4Cl��(NH4)2SO4��NH4HSO4������Һ�У�c(NH4��)��С˳�٣��ڣ���
D��10mL pH��12������������Һ�м���pH��2��HA��pH�պõ���7��������Һ���
V(��)��20mL
II�� ����87�֣�
��������⣨������� 3С�⣬��33�֣�
19��12�֣�I(4��)����ʵ��������ʵ����ʵ�������в���ȷ����______________��
�� ��ȼ�ŵľƾ��Ʋ�������ʧ�𣬿�������ʪ������
�ڵζ��õ���ƿ�͵ζ��ܶ�Ҫ����ʢ��Һ��ϴ
�۷�Һʱ����Һ©�����²�Һ����¿��������ϲ�Һ����Ͽڵ���
������������Һʱ����������Ͳ�ڼ���һ�������ˮ�����ڽ�������������Ũ����
�ݲ�����Ũ����Һմ��Ƥ���ϣ�Ҫ�����ô���ˮ��ϴ��Ȼ��Ϳ��������Һ
����������ƽ����ʱ������ҩƷ���ɷ���ֽ�ϣ���������ƽ������
�߲ⶨ��Һ��pHʱ�����ýྻ������IJ�����պȡ��Һ������pH��ֽ�ϣ��������ɫ���Ƚ�
��Ũ������Ũ������ӷ����ʾ�Ӧ��������ɫ�Լ�ƿ�У�������������
������һ�����ʵ���Ũ�ȵ���Һ������ʱ��������ƿ�Ŀ̶��ߣ���ʹ������Һ��Ũ��ƫ��
���������ʽ�ζ�����ȡ20.00mL0.1000mol��L��1KMnO4��Һ
II (8��)ʿ����Ұ�����ʳ��ʱͨ�����á�����ʳ���������������Ҫ��ѧ�ɷ�Ϊþ�ۡ����ۡ��Ȼ��ƣ�ʹ��ʱ����ˮ�����е�þ��Ӧ�ų�����������������ͬ�������¶Ըò�Ʒ������̽��ʵ�飺
�� ��ʵ��1������е���ˮ�ĸ��������зֱ�������и������ʣ�����μ���ͼ1��
�� ��1.0molþ����0.10mol���ۡ�0.10mil�Ȼ��Ʒ�ĩ��
�ڽ�1.0molþ������100�ݡ�0.10mol���ۡ�0.10mil�Ȼ��Ʒ�ĩ��
��1.0molþ�ۡ�0.10mol���ۡ�0.10mil�Ȼ��Ʒ�ĩ��
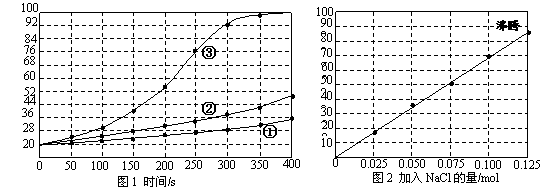 |
��ʵ��2�������100mLˮ�ĸ��������зֱ����0.10molþ�ۡ�0.50mol���ۼ���ͬ�����Ȼ��Ʒ�ĩ�����Ͻ��裬��15minʱ��¼�¶����ߵķ��Ȳμ���ͼ2��
��ش��������⣺
��ʵ��1֤ʵӰ��þ��ˮ��Ӧ���ʵ���Ҫ������_________________��
��A����Ӧ�¶ȡ���B��NaCl���������� C�������������� D��þ�ı����
��ʵ��2�е�NaCl����������0.125molʱ��ʵ�������������ԭ����__________��
���� A����������NaCl�������ӷ�Ӧ���ʡ�����B������NaCl�����ή�ͷ�Ӧ����
C���Ѵﵽ�е㲻�����¶ȱ仯������������ D����Ҫ������������������¶�
�������ʵ��2�м�����0.060molNaCl�����15minʱ�������¶���ӽ���______��
��A��34�桡���� B��42�桡���� C��50�桡���� D��62��
�����ۡ�NaCl��ʹ��Ӧ�������ӵ�ԭ����______________________________________��
20��11�֣���֪��һ��ɫ��ĩ����NaCl��Na2SO4��Na2CO3��CuSO4��MgCl2�е�һ�ֻ�����ɡ�ijͬѧ��̽����һ��ĩ����ɣ���������ʵ�飺
��ȡ������ĩ����ˮ�ܽ⣬����ɫ����Һ��
��ȡ������Һ����������NaOH��Һ����������������
����ȡ������ĩ������ϡ���ᣬ��������������
��1��������ݸ�ͬѧʵ�����������Ʋ���һ��ĩ�Ŀ�������������������������� __��
��2�����Ʋ�÷�ĩֻ��Na2SO4��ɣ������ڸ�ͬѧʵ���������ƺ���ʵ�飬��ȷ�������ĩ����ɡ��ۿɹ�ѡ����Լ��У�BaCl2��Һ��AgNO3��Һ��ϡHNO3��NaOH��Һ��Na2CO3��Һ��Ba��NO3��2��Һ��ϡ�����
����ʾ�����ڴ���ϰ����·�ʽ����ע��ǰ�����ݶ�Ӧ��
����������ע�����ּ�࣬ȷ������������ռ䡣
�ܢݿ�������Ҳ�ɲ����������������Ӣޢߡ�����
| ��� | ʵ����� | Ԥ������ͽ��� |
| �� | ||
| �� | ||
21��10�֣���ȩ��һ�ֳ��õ��л��Լ���Ҳ��������һ���ڼ��Ժͼ��������£�����������Һ��Ӧ��������������������ʵ���������������ȵطֲ����Թܱ��ϣ��γɹ�������������������Ӧ�ֽ�������Ӧ�������Ĺ����̶��뷴Ӧ�����йء�ͬѧ���ڿ����ж���ȩ��������Ӧ������̽����
��̽��������Ӧ�����ʵ������
����ʵ���������±���
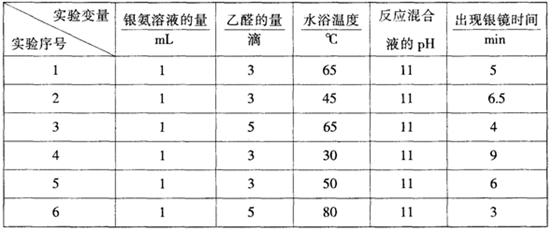
��ش��������⣺
��1������ ��ֻ����ʵ��1��ʵ��3����̽��Ŀ�������������������������������� ��
��2������ ��������Һ����Ϊ1mL����ȩ����Ϊ3�Σ�ˮԡ�¶�Ϊ40�棬��Ӧ���ҺpHΪ11ʱ������������ʱ���������������������������������� ��Ҫ̽����ͬˮԡ�¶�����ȩ����������Ӧ��������������˲����������ֵ�ʱ���⣬����Ҫ�Ƚϲ�ͬ�������γɵ����������������������������������������������������� ��
��3����һ��ʵ�顡����Ҫ̽��������Һ�������Գ�������������Ӱ�죬��ν���ʵ�飿
�������������������������������������������������������������������������� ��
��̽���Է�Һ�Ļ��մ���
������Һ�žú���ɵ�����������ը��ֱ���ŷŻ���Ⱦ���������������Դ���˷ѡ�ͨ���������ϣ���֪��������Һ����ȡ����һ��ʵ������Ϊ��

�����ܵķ����ǣ���Ag2S�����۷ŵ��ձ��м�Ũ���������У�ʹAg2S������ۡ���Ӧ�Ļ�ѧ����ʽΪ��Ag2S+Fe+2HCl2 Ag+ FeCl2+H2S��
��4������õ������к�������û�з�Ӧ������ۣ���ȥ���ķ�Ӧ�����ӷ���ʽΪ����������
��Ҫ�õ��IJ��������������������������������������������� �����ţ���
��5��������Ӧ�ڣ���ʵ�����豸���ƣ��������������������������������������н��С�
��6��Ҫϴȥ�Թܱ��ϵ����������õ��Լ������������������������������� �������ƣ���
�ġ�����⣨������� 3С�⣬��35�֣�
22��12�֣������Ĺ������ƣ�CaO2���ǰ�ɫ�Ľᾧ��ĩ��������ˮ���������Ҵ������ѣ������½�Ϊ�ȶ�����һ������ˮ����ֳ���������������ʻ�ˮ��Ʒ�����䡣
��֪�����ڳ�ʪ������CaO2�ܹ��ֽ⣺CaO2+2H2O== Ca��OH��2+H2O2��
2CaO2+2CO2==2CaCO3+ O2
��CaO2��ϡ�ᷴӦ�����κ�H2O2��CaO2+2H+== Ca2++ H2O2
��ʵ���ҿ��ø�����ȡCaO2��8H2O���پ���ˮ�Ƶ�CaO2��CaO2��8H2O��0��ʱ�ȶ���������ʱ��������ͷֽ⣬������130��ʱ��Ϊ��ˮCaO2��
���Ʊ��������£�
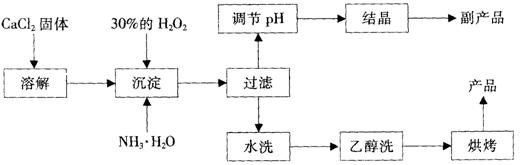
����������Ϣ���ش��������⣺
��1��������������ȡ�������ƵĻ�ѧ����ʽ���������������������������������� ��
��2��Ϊ�˿��Ƴ����¶�Ϊ0�����ң���ʵ�����˲�ȡ�ķ����������������������� ��
��3�����Ʒ��ĸ���ƷΪ���������������� ���ѧʽ����Ϊ����߸���Ʒ�IJ��ʣ��ᾧǰҪ����Һ��pH���������ʷ�Χ���ɼ�����Լ��������������� ��
A�����ᡡB����ˮ
��4��Ϊ�˼��顰ˮϴ���Ƿ�ϸ�ȡ����ϴ��Һ���Թ��У��ٵμ��������������� ��
��5���ⶨ��Ʒ��CaO2�ĺ�����ʵ�鲽���ǣ�
��һ����ȷ��ȡa g��Ʒ��������ƿ�У�������������ˮ������b g��KI���壬�ٵ�������2mol/L��H2SO4��Һ����ַ�Ӧ��
�ڶ�������������ƿ�м��뼸�ε�����Һ��
����������μ���Ũ��Ϊc mol/L��Na2SO3��Һ����Ӧ��ȫ������Na2S2O3��ҺVmL������֪��I2+2S2O32��==2I��+S4O62������ɫ����
�ٵ�������˵����Ӧǡ����ȫ�������������������������������������������������� ��
��CaO2����������Ϊ�������������������������������������������� ������ĸ��ʾ����
��ijͬѧ��һ���͵ڶ����IJ������ܹ淶������������̫����������õ�CaO2�������������������������������Ӱ�족����ƫ�͡���ƫ�ߡ�����ԭ������������ ��
23 ��11�֣��������һ����Ҫ�ķǽ������ϡ��Ʊ��������Ҫ�������£�
![]() �ٸ�������̼��ԭ���������Ƶôֹ�
�ٸ�������̼��ԭ���������Ƶôֹ�
�ڴֹ������HCl���巴Ӧ�Ƶ�SiHCl3��Si��3HCl��������SiHCl3��H2
��SiHCl3�����H2��1000��1100 �淴Ӧ�Ƶô���
��֪SiHCl3����H2Oǿ�ҷ�Ӧ���ڿ���������ȼ��
��ش��������⣺
��1���ֹ���HCl��Ӧ��ȫ�������õ���SiHCl3���е�33.0�棩�к�������SiCl4���е�57.6�棩��HCl���е㣭84.7�棩���ᴿSiHCl3���õķ���Ϊ������ ������������
��2����SiHCl3�����H2��Ӧ�Ʊ������װ�����£���Դ���г�װ����ȥ����
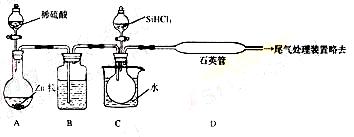
��װ��B�е��Լ�����������������װ��C�е���ƿ��Ҫ���ȣ���Ŀ���ǣ�������������������������������������������������������
��װ�ã��з�����Ӧ�Ļ�ѧ����ʽΪ������������������������������������ ��װ��D���ܲ�����ͨ�����ܵ�ԭ������������������������������������
��Ϊ��֤�Ʊ�����ʵ��ijɹ��������Ĺؼ��Ǽ��ʵ��װ�õ������ԣ����ƺ÷�Ӧ�¶��Լ���������������������������������������������
��Ϊ������Ʒ�����Ƿ��������ʣ������ʵ����м��飬�ڴ����Ӧλ������ʵ�������Ԥ������ͽ��ۡ�
24(12��) ��ѧƽ��ԭ���ڻ�������������ҪӦ�á�
I(6��) ˮú�� (��Ҫ�ɷ֣�CO��H2 ) ����Ҫȼ�Ϻͻ���ԭ�ϣ�����ˮ����ͨ�����ȵ�̿���Ƶã�
C (s) + H2O(g)�PCO (g) +H2 (g)����H =+131.3kJ•mol��1
��1��ij�¶��£��ĸ������о�������������Ӧ����������̿�������������ʵ����ʵ���Ũ�ȼ����淴Ӧ���ʹ�ϵ���±���ʾ������д������Ӧ�Ŀո�
| ������� | c(H2O)/mol��L��1 | c(CO)/mol��L��1 | c(H2)/mol��L��1 | V����V���Ƚ� |
| I | 0.06 | 0.60 | 0.10 | V��=V�� |
| II | 0.06 | 0.50 | 0.40 | ? |
| III | ��0.12���� | 0.40 | 0.80 | V��<V�� |
| IV | 0.12 | 0.30 | �� | V��=V�� |
��2������һ���ݻ��ɱ���ܱ����������º�ѹ�£������м���1.0mol̿�� 1.0mo lˮ���� (H216O)������������Ӧ���ﵽƽ��ʱ�������������Ϊԭ����1.25 ����ƽ��ʱˮ������ת����Ϊ������ ����������в��� a mol ̿��ˮ������ת���ʽ����������� ����������С���������䡱�����ٲ��� a mol ˮ���� (H218O), ����������C16O��C18O �����ʵ���֮��Ϊ���������� ��
��3����֪��C (s)��+ ![]() O2(g)=CO (g)����H = ��110.5kJ��mo1��1
O2(g)=CO (g)����H = ��110.5kJ��mo1��1
������ ������ CO(g) + ![]() O2(g) =CO2 (g)����H =��283.0 kJ��mo1��1
O2(g) =CO2 (g)����H =��283.0 kJ��mo1��1
������ ������ H2 (g) + ![]() O2
(g) =H2O (g)����H = ��241.8kJ��mo1��1
O2
(g) =H2O (g)����H = ��241.8kJ��mo1��1
��ô����2.4 g ̿��ȫת��Ϊˮú����Ȼ����ȼ�գ��������̡�H =���������� kJ��mo1��1
��(6��)��ͼ��������Ϊ��Һ��pHֵ��������ΪZn2+���ӻ�Zn��OH��42-�������ʵ���Ũ�ȵĶ������ش��������⡣
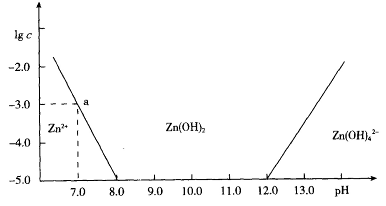
��1����ZnCl2��Һ�м�������������������Һ����Ӧ�����ӷ���ʽ�ɱ�ʾΪ��
���������������������������� __________________�������������������������� ��
��2����ͼ�����ݼ���ɵ�Zn��OH��2���ܶȻ���Ksp��==�������� ____������ ��
��3��ij��Һ�к�Zn2+���ӣ�Ϊ��ȡZn2+���ӿ��Կ�����Һ��pHֵ�ķ�Χ������ ___����
��4����1.00L 1.00mol��L��1 ZnCl2��Һ�м���NaOH������pH=6����NaOH����____��mol
��5����֪����ZnCl2��Һ�м�������Ǧ�����Ǧ��Һ�����Ƶ�PbCl2��ɫ���壻25��ʱ��PbCl2�����������е��ܽ�����£�
| C(HCl)/(mol��L-1) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| C(PbCl2)/(mol��L-1����10-3 | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
�����ϱ������ж�����˵����ȷ���������������� ������ĸ��ţ�
A����������Ũ�ȵ�����PbCl2������ܽ���ȱ�С���ֱ��
B��PbCl2������0.50 mol��L��1�����е��ܽ��С���ڴ�ˮ�е��ܽ��
C��PbCl2����Ũ���ᷴӦ����һ���ѵ���������ӣ���������ӣ�
D��PbCl2��������ڱ���ʳ��ˮ
�塢����⣨������� 1С�⣬��9�֣�
25��9�֣�2006��5��15�չ���ʳƷҩƷ�ල������ͨ������������ڶ���ҩ����˾��ҩ��������������ҩ��Υ���涨�����빤ҵ�á����ʴ���(��ѧʽΪC4H10O3)����ҽ�ñ�����(��ѧʽΪC3H8O3)�����ϣ����ڡ��������ء�ע��Һ�����������²��������ܼ���˥�ߣ���ɶ������������ʴ��ֳ��Ҷ����ѣ�����ʽC4H10O3 (HO��CH2��CH2��O��CH2��CH2��OH)���Զ��ʴ�Ϊԭ�ϣ�����ȡ�ѡ��ᡢ�������ȶ��ֻ�����Ʒ������Ҫ��Ʒ����������������1��4��������(1��4����������ϩ)�����ʴ���(˫)�ѣ����ʴ�����(�������Ͳ�������)�ȣ����㷺Ӧ����ʯ�ͻ����������ϡ���֯��Ϳ�ϡ�ճ�ϼ�����ҩ����ҵ����;ʮ�ֹ㷺�����ʴ�һ��ĺϳ�·��Ϊ��
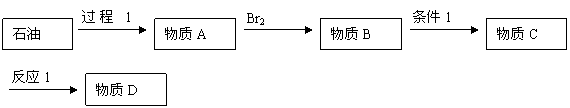
��ش��������⣺
��1����2������1��ʯ�ͼӹ��г��ò��裬������Ϊ���������������������������������� ��
��2��������B������C�Ĺ�������������Ʋ��û�������һ������E��E�����ڽ��������������������Ϊ���ܵõ����ʴ�D������B������C�ķ�Ӧ������������������ ���÷�Ӧ������������������������������������������ (���л���Ӧ����)��
��3������D���Ƕ��ʴ�����ϳ�·���е�����A��B��C�Ľṹ��ʽ�ֱ�Ϊ��
A������������������ ��B������������������ ��C���������������������� ��
��4����Ӧ1�Ļ�ѧ����ʽΪ���������������������� �������������������������� ��
����ѡ���⣨�������2С�⣬ÿС��10�֣�����ֻ��ѡ��һ�⡣28С��Ϊ���л���ѧ���������ݵ����⣬29С��Ϊ�����ʽṹ�����ʡ����ݵ����⣩
26(10��) ��1���±�Ϊϩ��������巢���ӳɷ�Ӧ��������ʣ�����ϩΪ������
| ϩ����� | ������� |
| (CH3)2C��CHCH3 | 10.4 |
| CH3CH��CH2 | 2.03 |
| CH2��CH2 | 1.00 |
| CH2��CHBr | 0.04 |
�ݱ������ݣ��ҳ��������ɣ�
���������������������� ����������������������������������������������
��������������������������������������������������������������������
��2��ϩ�����廯�⡢ˮ�ӳ�ʱ������������֮�֣����磺
CH2=CHCH3 + HBr �� CH3CHBrCH3 + CH3CH2CH2Br
�������������������� (��Ҫ����)����(��Ҫ����)
|
CH2=CH CH2CH3 + H2O �� CH3CH��OH��CH2CH3 + CH3CH2CH2 CH2 OH
(��Ҫ����)���������� (��Ҫ����)
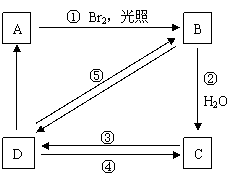 ���п�ͼ��A��DΪ����B��C��D������ط�Ӧ�е���Ҫ��������������Լ���ʡ�ԣ����һ�����B�н���4��̼ԭ�ӡ�1����ԭ�ӡ�1����ԭ�ӡ���ش��������⣺
���п�ͼ��A��DΪ����B��C��D������ط�Ӧ�е���Ҫ��������������Լ���ʡ�ԣ����һ�����B�н���4��̼ԭ�ӡ�1����ԭ�ӡ�1����ԭ�ӡ���ش��������⣺
�١���ͼ�У�D�Ľṹ��ʽΪ____________________________��
�ڡ����� B �� C�ķ�Ӧ������___________��D �� A�ķ�Ӧ������____________��
a. ȡ����Ӧ�������� b. �ӳɷ�Ӧ�������� c. ˮ�ⷴӦ�������� d. ��ԭ��Ӧ
�ۡ����� д����Ӧ�ܵĻ�ѧ����ʽ��������Ӧ�����Ͳ������Σ��� ______���� ___________��
27��10�֣��±���Ԫ�����ڱ��е�һ���ڶ�����10��Ԫ�ص�ij�����ʵ�һ�����ݣ��������ݵĵ�λ����ͬ�ģ���������������������Ԫ�س��⣬����Ԫ�ض������˸���Ԫ�ص�ȫ���������ݡ�
| (H) 13.6 | (He) 24.6 54.4 | ||||||
| (Li) 5.4 75.6 122.5 | (Be) 9.3 18.2 153.9 217.7 | (B) 8.3 25.2 37.9 259.4 340.2 | (C) 11.3 24.4 47.9 64.5 392.1 489.9 | (N) 14.5 29.6 47.4 72.5 97.9 552.1 ���� | (O) 13.6 35.1 ���� ���� ���� ���� ���� ���� | (F) 17.4 34.9 ���� ���� ���� ���� ���� ���� ���� | (Ne) 21.6 41.6 ���� ���� ���� ���� ���� ���� ���� ���� |
�о���Щ���ݣ�
(1)ÿ�����ݿ����Ǹ�Ԫ�صģ�������
(A)ԭ�ӵõ��������ų����������� (B)ԭ�Ӱ뾶�Ĵ�С
(C)ԭ�����ʧȥ���������յ����� (D)ԭ�Ӽ��γɲ�ͬ���ӵİ뾶�Ĵ�С
(2)����ͬ�����������Ҹ�Ԫ��ԭ�ӵĵ�һ������
������仯������_______�������С����������ǰ��Ԫ����ȣ����ڸ�Ԫ�ص���ֵ����ý϶����Ϊ������Ԫ������________�壬�������ǵ�ԭ�Ӻ�������Ų���ָ�����������������Ŀ���ԭ���ǣ�������
(A)���ǵ�ԭ�Ӱ뾶ͻȻ��СЩ���� (B)���ǵĺ�������Ų����ڱ���״̬
(C)���ǵ�ԭ�Ӱ뾶ͻȻ���Щ���� (D)���ǵĺ�������Ų����ڰ������ȫ����״̬
�����������Ϲ��ɣ����Ʋ�þ�����ĵ�һ�����ݵĴ�СMg(1)_____Al(1)
(3)ͬһԪ��ԭ�ӵ�һ��������Լ�Ա��ȹ�ϵ��������˵�����ܵ�һ��ԭ����_________________________________________________��ÿ��Ԫ�ص�һ�������и���ط�����ı����ر���γ�ͻԾ��������������ҳ���Щ���ݣ���������Щ���ݳ��ֵĹ��ɣ�����Ϊ��Ԫ�س��ָ����������Ӧ������Ԫ��8�����ݵĵ�_______����
�������ɿ���֤��ԭ�ӽṹ��_______________________________�Ľ��ۡ�
�������ڻ�ѧ������ܲ�ο���
1~5 D��D��A��C��C��6~10 D��A��C��A��CD��
11~15 AD��BC��C��D��BD��16~18 A��AC��BC
19��12�֣����ڢܢޢ�(4�֣���һ����ȷ�𰸿�1�֡���ѡһ������1�ֿ���Ϊֹ)
II��D����C����D����þ�ۡ�������NaCl��ˮ��Һ������ԭ��ء���(ÿ��2��)
20��11�֣�
��1��ֻ��![]() ��1�֣���ֻ��
��1�֣���ֻ��![]() ��1�֣�����
��1�֣�����![]() ��
��![]() ��ɣ�1�֣���
��ɣ�1�֣���
��2��
| ��� | ʵ����� | Ԥ������ͽ��� |
| �� | ȡ������Һ�������Թ��У���1�֣� �μ������ữ�� | ������ɫ���� ˵�� |
| �� | ȡ������Һ�������Թ��У��μ����������ữ�� �У���1�֣� �ټ��������ữ�� | ���������� ˵����Һ����Cl����1�֣� ���Ը÷�ĩ���ֻ�� |
21��10�֣�
��1���Ƚ���ȩ������ͬʱ����������ʱ�䣨�ٶȻ��������ɣ���2�֣�
��2����6.5��9min֮�䣻�����̶ȣ������ȡ���ۡ�Ч���ȣ��������ɸ��֣�����1�֣���2�֣�
��3������������ʵ���������䣬�ı�������Һ����������������������ʱ�䡣�������ı������ɸ��֣���2�֣�
��4��Fe+2H+==Fe2++H2����1�֣�������������Ҳ�ɸ��֣���Fe+2 Fe3+==3Fe2+����bef��1�֣�
��5��ͨ�����1�֣�
��6�����ᣨ1�֣�
22��12����
��1��CaCl2+H2O2+2NH3+8H2O== CaO2��8H2O��+2NH4Cl��2�֣�
��2����ˮԡ��ȴ����Ӧ���������ڱ�ˮ�У���1�֣�
��3��NH4Cl��A ����1�֣���2�֣�
��4��ϡ�����ữ����������Һ��1�֣�
��5������Һ����ɫ��Ϊ��ɫ��1�֣�
��![]() ��2�֣�
��2�֣�
��ƫ�ߣ�1�֣��������������¿����е�O2Ҳ����KI����ΪI2��ʹ���ĵ�Na2S2O3���࣬�Ӷ�ʹ��õ�CaO2����������ƫ�ߡ���2�֣�
23( 11��)
��1����������1�֣�
![]() ��2����Ũ���� ��1�֣���ʹ������ƿ�е� SiHCl3 ���� ��1�֣��Ӷ���H2��ֻ��
��2����Ũ���� ��1�֣���ʹ������ƿ�е� SiHCl3 ���� ��1�֣��Ӷ���H2��ֻ��
��SiHCl3+H2�� ���������� Si+3HCl��2�֣�����1000��1100��ʱ��ͨ�����ܻ�������1�֣���
���ž�װ���еĿ��� ��2�֣�
�����Թ��м���������Ʒ���������ϡ���ᣬȡ�������ᷴӦ�������Һ��1�֣�����������ϡ���ᣨ����ˮ����������������KSCN��1�֣�����Һ��Ѫ��ɫ��˵����Ʒ�к�Fe��1�֣���˵���������������۸�1�ֹ�3�֣���07��㶫ʡ�߿�����ϸ������Ԫ��ʱ�ȼ�KSCN�ټ�������ϡ�������������÷ֵ㲻������
24��10�֣���6�֣���1��
| V�� < V����1�֣� | ||||
| 0��40��1�֣� |
��2��25%��1�֣���������1�֣���1��a��1�֣�����(3)-78.7 ��1�֣�
��6������1��Zn2++ 4OH��==[Zn��OH��4]2����1�֣���
��2��10��17��1�֣�������3����8.0��12.0����1�֣�������4��1.80��1�֣�д1.8���÷֣���
��5��A B C D ��2�֣�д�ԣ����ã��֣�д�ԣ����ã��֣�д��4���ã��֣�©1����1�֣�����Ϊֹ����
25��9�֣���1���ѽ⣻��2�֣���2��NaOHˮ��Һ��ȡ����Ӧ��
|
|
26��10�֣���1����C��C�ϼ������ڼӳɷ�Ӧ���ڼ�Խ�࣬����Խ�죻��C��C��±ԭ�ӣ��壩�����ڼӳɷ�Ӧ����д������1������2�֣���4�֣�
��2���� CH2=C(CH3)2�� ��1�֣� �� a��c������1�֣�b��d��1�֣�
�� CH2=C(CH3)2
+ H2O![]() (CH3)3COH + (CH3)2CHCH2OH����3�֣�
(CH3)3COH + (CH3)2CHCH2OH����3�֣�
������������������������������ ����Ҫ����� ����Ҫ�������
27 ��10�֣�(1) C��(1��)��(2) ���� ��A����A ��D�� >��(5��)
��(3) ԭ��ʧȥһ�����Ӻ�,��Ϊ�����ӣ���ʧ���Ӹ��ѣ����յ������ɱ����ӡ�(1��)���� (1��) ԭ�Ӻ�������Ƿֲ��Ų��� (1��)