08届高三化学上学期第二次月考试卷
化学试题
可能用到的相对原子质量:H―1 C―12 N―14 O―16 Na―23 Mg―24 Al―27 S―32 Cl―35.5 K―39 Ca―40 Fe―56 Cu―64
第Ⅰ卷(选择题 共50分)
一、选择题(本题包括20小题,每小题2分,共40分。只有一个选项符合题意。)
1.从硫元素的化合价态上判断,下列物质中的硫元素不能表现氧化性的是
A.Na2S B. S C.SO2 D. H2SO4
2.下列各物质中,所有原子都满足最外层为8电子结构的是
A.BeCl2 B.PCl3 C.PCl5 D.NH3
3.下列各组物质在不同条件下反应时,均能得到不同产物,其中主要是由温度不同而引起的是
①Na+O2 ②P+ Cl2 ③ C2H5OH+ H2SO4 (浓) ④Cu+HNO3 ⑤CO2+NaOH ⑥C2H2+HCl ⑦Fe+ H2SO4 ⑧Cl2+NaOH
A.①③⑧ B.②⑤⑦ C.③④⑧ D.②③⑥
4、下列化学式能真实表示物质分子组成的是
A.NaOH B.S03 C.CsCl D.Si02
5.对于某一已达化学平衡状态的可逆反应,如果改变某种条件,结果使某生成物的浓度增大,则
A.平衡一定向正反应方向移动 B.平衡一定向逆反应方向移动
C.反应物的浓度相应减小 D.平衡可能移动也可能不移动
6. 下列事实不能用勒沙特列原理解释的是:
A. 氨水应密闭保存,放置低温处
B. 在FeSO4溶液中,加入Fe粉以防止变质
C. 打开汽水瓶,看到有大量的气泡逸出
D. 实验室常用排饱和食盐水的方法收集Cl2
7.下列条件一定能使反应速率加快的是:①增加反应物的物质的量②升高温度③缩小反应容器的体积 ④加入生成物 ⑤加入MnO2
A.全部 B.①②⑤ C.② D.②③
8.在其它条件不变时,10℃时以某物质表示的反应速率为3 mol/L・ s ,已知温度每升高10℃反应速率是原来的2倍,则温度为50℃时,该反应的速率为
A.48 mol/L ・s B.36mol/L・ s
C.24 mol/L ・s D.12 mol/L・ s
9.下列物质中属于非电解质,但放入水中后所得溶液导电性明显增强
A.金属钠 B.三氧化硫 C.氯化钠 D.乙醇
10.在二氧化碳的饱和溶液中,C(H+)和C(CO32-)的比值
A.等于1 B.等于2 C.大于2 D.1―2之间
11.室温时,pH=2的一元酸溶液与pH=12的NaOH溶液等体积混合,则溶液的pH为
A.一定不大于7 B.一定不小于7
C.一定等于7 D.可能大于7
12.物质的量浓度相同的下列溶液中,NH4+浓度最大的是
A.NH4Cl B.NH4HSO4
C.CH3COONH4 D.NH3・H2O
13.某溶液中,由水电离出来的c(OH-)=1×10-9mol/L,则此溶液不可能是
A.pH=5的强酸或弱酸溶液
B. pH=9的K2CO3溶液
C.pH=5的NaHSO4溶液 D. pH=9的强碱或弱碱溶液
![]() 14.某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:
,若维持温度和压强不变,当达到平衡时,容器的体积为VL,其中C气体的体积占10%,下列推断正确
14.某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:
,若维持温度和压强不变,当达到平衡时,容器的体积为VL,其中C气体的体积占10%,下列推断正确
①原混合气体体积为1.2VL; ②原混合气体的体积为1.1VL;
③反应达平衡时气体A消耗0.05VL; ④反应达平衡时气体B消耗掉0.05VL。
A.②③ B.②④ C.①③ D.②①
![]() 15.某可逆反应:mA(气)+nB(气) pC(气)(反应热为
15.某可逆反应:mA(气)+nB(气) pC(气)(反应热为![]() H),其温度T、时间t与生成物C的体积百分数C%、平衡混合气体的平均相对分子质量M的关系如下图所示,下列结论正确的是 ( )
H),其温度T、时间t与生成物C的体积百分数C%、平衡混合气体的平均相对分子质量M的关系如下图所示,下列结论正确的是 ( )
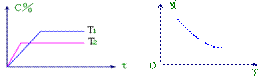 A.m+n>p
A.m+n>p ![]() H>0
H>0
B.m+n>p ![]() H<0
H<0
C.m+n<p ![]() H>0
H>0
D.m+n<p ![]() H<0
H<0
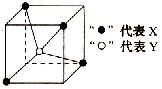 16.常见的离子晶体类型有五种,右图是其中的一种空间构型。则该晶体的化学式可能为
16.常见的离子晶体类型有五种,右图是其中的一种空间构型。则该晶体的化学式可能为
A.YX4 B.YX2
C.YX D.XY2
17.在2A+B ![]() 3C+4D中,表示该反应速率最快的是
3C+4D中,表示该反应速率最快的是
A.υ(A) = 0.5mol・L-1・S-1 B.υ(B) = 0.3 mol・L-1・S-1
C.υ(C) = 0.8mol・L-1・S-1 D.υ(D)= 1 mol・L-1・S-
18.在石墨晶体中,每一层有无数个正六边形构成,同一层内每个碳原子与相邻的三个碳原子以C―C键相结合。则石墨晶体中碳原子数与C―C键之比为
A.1:1 B.2:1 C.2:3 D.3:2
19.在密闭容器中投入1mol
CO(g)和3mol H2O(g), 下列反应:CO(g)+H2O(g) ![]() CO2(g)+H2,达到平衡后,测得CO2(g)为0.75mol, 再向其中加入5mol H2O(g),达到新平衡后,CO2(g)的物质的量可能的是
CO2(g)+H2,达到平衡后,测得CO2(g)为0.75mol, 再向其中加入5mol H2O(g),达到新平衡后,CO2(g)的物质的量可能的是
A.0.50mol B. 0.75mol C. 0.85mol D. 1.1mol
20.在一固定容积的容闭容器中,加入2 mol X 和3 mol Y 气体,发生如下反应:n X(g) +
3Y(g) ![]() 2Z(g) + R(g),反应平衡时,已知X 和Y 的转化率分别为30%和60%,则化学方程式中的n 值为
2Z(g) + R(g),反应平衡时,已知X 和Y 的转化率分别为30%和60%,则化学方程式中的n 值为
A.1 B.2
C.3
D.4
二、选择题(每题一到二个选项正确,每题2分)
21.能增加反应物分子中活化分子的百分数的是
A.升高温度 B.使用催化剂 C.增大压强 D.增加浓度
22.在1L密闭容器中通入2mol氨气,在一定温度下发生反应;2NH3 ![]() N2+3H2,达平衡时,N2的物质的量分数为a %,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a %的是
N2+3H2,达平衡时,N2的物质的量分数为a %,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a %的是
A.3mol H2和1mol N2 B.2mol NH3和1mol N2
C.2mol N2和3mol H2 D.0.1mol NH3、0.95mol N2、2.85mol H2
23.过量锌粉跟100mL6mol/L盐酸反应,在一定温度下,为加快反应速率但又不影响生成氢气的总量,可向反应混合物中加入适量的
A.铜粉 B.醋酸锌溶液
C.氯化铜固体 D.氧化铜
24.最近科学家成功地合成了一种新型的化合物,该化合物晶体中,每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是
A.该物质的化学式为CO4
B.晶体的熔、沸点高,硬度大
C.晶体中C原子数与C―O化学键之比为1:4
D.晶体的空间最小环共由12个原子所构成
 25.右上图中a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是
25.右上图中a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是
A.b元素除0价外,只有一种化合价
B.五种元素中,c元素的性质最稳定
C.b、d气态氢化物溶于水,溶液的酸性:b > d
D.e元素最高价氧化物的水化物和不同量的氢氧化钠溶液反应,可能生成三种盐
第Ⅱ卷(非选择题,共50分)
三、填空题
26.(9分)短周期元素的A、B、C在元素周期表中的位置如图所示,已知A、B、C三种元素的原子核外电子数之和等于B的质量数,B原子核内质子数和中子数相等。据此填空:
| A |
| C |
|
| B |
|
(1)A的氢化物分子式为 ;
(2)B的元素符号为 ,原子结构示意图为 ,在周期表中位于第 周期 族;
(3)C的单质分子式为 ,C的单质溶于水所得溶液叫 。写出所得溶液与石英反应的化学方程式:
27.(8分)现有下列溶液:①20mL0.1mol・L-1H2SO4溶液
②40mL0.1mol・L-1CH3COOH溶液③40mL0.1mol・L-1HCl溶液
④40mL0.1mol・L-1NaOH溶液⑤20mL0.1mol・L-1Ba(OH)2溶液。其中:
(1)c(H+)最小的是
(2)任取2份溶液混合,混合后溶液的pH为7,有 种取法。
(3)②和④混合后,溶液的pH 7(填>、<、=)
(4)混合后出现白色沉淀的两种溶液是:
28.(10分)在元素周期表中,元素的金属性和非金属性及其强弱比较与周期数(n)和主族数(A)(将稀有气体看作主族元素)有如下经验公式:K=A/n (K为A与n的比值)。请选编号回答下列问题:
A.两性 B.金属 C.非金属 D.稀有气体
(1)当n一定时,K值越大,则元素的_____________性越强。
(2)当A一定时,K值越小,则元素的________性越强。
(3)当K=0,则该元素系_________元素,
当K=l时,则该元素系_________元素,
当K<1时,则该元素系_________元素。
![]() 29、(10分)在一定温度下,在一个容积为2 L的密闭容器中,二氧化硫和氧气发生如下反应: 2SO2(g)+ O2 (g) 2SO3(g) △H=- 196.6kJ・mol-1
29、(10分)在一定温度下,在一个容积为2 L的密闭容器中,二氧化硫和氧气发生如下反应: 2SO2(g)+ O2 (g) 2SO3(g) △H=- 196.6kJ・mol-1
在反应进行至10min和20min时,改变了影响反应的一个条件,反应进程如右图所示。
(1)前10min正反应速率变化趋势是 (填增大、减小或不变)
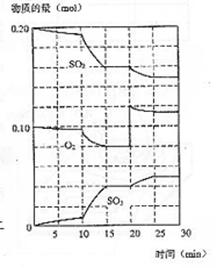 前15min平均反应速率用SO3 浓度变化可表示
前15min平均反应速率用SO3 浓度变化可表示
为: 。
(2)在如图所示的反应进程中,表示正反应速率与逆反应速率相等的时间段是
。
(3)据图判断:
10min时改变的反应条件可能是
(填写编号,下同);20min时改变的反应条件可能 是 。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加O2的物质的量
30.(7分) (1)常温下,将pH=11的氢氧化钠溶液aL与pH=2的稀硫酸bL混合(设混合后溶液体积的变化忽略不计),若所得混合液为中性,则a∶b= ;
(2)常温下,将pH=11的氢氧化钠溶液与pH=3的醋酸溶液等体积混合,所
得溶液的PH__________7(选填“>”.“<”或“=”),此溶液中各种离子的
浓度由大到小排列顺序是 。
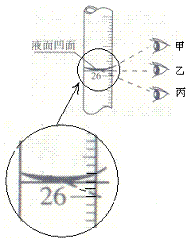
31.(6分)下图所示的滴定管(已有部分刻度数字隐去),甲.乙.丙三位同学按不同方法读数,其中正确的是 ,甲同学读数
为 mL;如图所示,滴定管内实际所装的液体体积为 。
A. 26.00mL B. 25.80mL
C. 4.20mL D. 无法确定
一、选择题
1、A 2、B 3、A 4、B 5、D 6、D 7、C 8、A 9、B 10、C
11、A 12、B 13、B 14、A 15、B 16、D17、B 18、C 19、C
20、A 21、AB 22、AD 23、AC 24、A 25D
26.(每空1分,共7分)(1)NH3 (2)S ;略;三 ⅥA (3)F2 氢氟酸
27.(每空2分)(1)⑤ (2)4 (3)> (4)①⑤
28、1)C (2)B (3)D A B (每空2分)
29、⑴减小 0.04/30 mol・L-1・min-1
⑵15∽20min, 25∽30min
⑶a,b d
30. (6分)
(1)10 (2)< , C(CH3COO-)> C(Na+) >C(H+) >C(OH-)
31.(3分)乙;25.70;D
26.(每空1分,共7分)(1)NH3 (2)S ;略;三 ⅥA (3)F2 氢氟酸
27.(每空2分)(1)⑤ (2)4 (3)> (4)①⑤
28、1)C (2)B (3)D A B (每空2分)
29、⑴减小 0.04/30 mol・L-1・min-1
⑵15∽20min, 25∽30min
⑶a,b d
30. (6分)(1)10 (2)< , C(CH3COO-)> C(Na+) >C(H+) >C(OH-)
31.(3分)乙;25.70;D