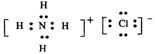08届高三化学上册月考试卷
满分108分,考试用时90分钟。
可能用到的相对原子质量:H1 C12 N14 O16 S32 Fe56 Pb207
一.选择题(每小题都只有一个正确答案,每小题3分,共48分)
1.化学是一门实用的、中心的学科,生活中的许多问题常涉及到化学知识。它在给经济发展
和生活带来方便的同时,如果运用不当也会产生负面的影响。下列有关叙述不正确的是
A.氟氯烃为一类含有氟和氯的有机物,是制冷效果极佳的致冷剂,但它会破坏臭氧层,科研人员正在积极研发环保型的替代产品以减少氟氯烃的使用量
B.人们应用原电池原理,制作了多种电池,如干电池、充电电池、高能电池等。电池在现代生产和科学技术中发挥了重要作用,但废旧电池会对生态环境和公众健康造成危害。所以废旧电池必须回收再利用
C.明矾常用作净水剂,但人体摄入大量铝盐,易患“老年性痴呆”,所以饮用水的生产不能大量采用明矾作净水剂
D.次氯酸和臭氧都是强氧化剂,都能杀死水中的细菌。自来水常用氯气来杀菌消毒,是因为氯气杀菌消毒效果要比臭氧好,且不会残留有毒、有害物质
 2.下列实验过程中产生的现象与对应的图形符合的是
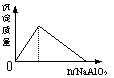
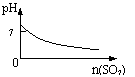
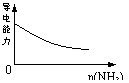
2.下列实验过程中产生的现象与对应的图形符合的是
A.盐酸中加入NaAlO2溶液 B.SO2气体通入溴水中
 | |||
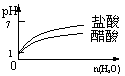 | |||
C.pH=1的醋酸与盐酸分别加水稀释 D.氨气通入醋酸溶液中
3.石棉是一类价格低廉的硅酸盐材料,但是有毒,能使人患肺癌。一种叫矿青石棉的化学式为:Na2Fe5Si8O22(OH)2。它用稀硝酸溶液处理时,还原产物只有NO,下列说法正确的是
A.该物质中Fe元素的化合价为+2价,它属于硅酸盐
B.该物质的化学组成可表示为:Na2O・3FeO・Fe2O3・8SiO2・H2O
C.1mol该物质能和18molHNO3反应,也能与18mol盐酸反应
D.这种石棉属于新型无机非金属材料
4.进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习方法之一。下列对有关实验事实的解释正确的是
A.溴水中通入SO2后,颜色褪去,说明SO2表现了漂白性
B.用惰性电极电解相同浓度的Cu(NO3)2和AgNO3混合溶液,阴极首先析出的是Ag,说明Ag+ 的还原性比Cu2+ 强
C.常温下,将铝片放入浓硫酸中无明显现象,说明铝不和冷的浓硫酸反应
D.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
5.近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:
|
KI+3H2O KIO3+3H2↑。下列有关说法正确的是( )
|
| |
C.电解时,阴极区域溶液酸性增加
D.电解时,阳极反应是:I¯-6e¯+3H2O=IO![]() +6H+
+6H+
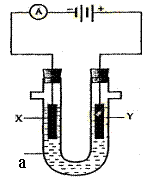
6.有机电解制备的金属醇盐,可直接作为制备纳米材料的前体。以下是一种电化学合成金属醇盐的主要装置。在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
2CH3CH2OH+2e¯=2CH3CH2O-+H2↑
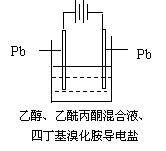
![]()
下列说法正确的是
A.阳极Pb失去电子,发生还原反应
B.当阳极失去2 mol e―时,阴极产生2 mol氢气
C.电解过程中,阳离子向阳极移动
D.已知Pb-4e¯=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol
7.下列操作中,完全正确的一组是
① 用试管夹夹持试管时,试管夹从试管底部上套,夹在试管的中上部
② 给盛有液体的体积超过1/3容积的试管加热 ③ 把鼻孔靠近容器口去闻气体的气味
④ 将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤ 取用放在细口瓶的液体时,取下瓶塞倒立放在桌面上,倾倒液体时,瓶上的标签对着地面
⑥ 将烧瓶放在桌上,用力塞紧塞子 ⑦ 用坩埚钳夹取加热后的蒸发皿
⑧ 将滴管垂直伸进试管内滴加液体 ⑨ 稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑩ 检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热。
A.①④⑦⑩ B.①④⑤⑦⑩ C.①④⑤⑦⑧⑩ D.④⑤⑦⑧⑩
8.某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种,则这种烃可能是
①分子具有7个碳原子的芳香烃 ②分子中具有4个碳原子的烷烃
③分子中具有12个氢原子的烷烃 ④分子中具有8个碳原子的烷烃
A.①② B.②③ C.③④ D.②④
9.下图是2008奥运吉祥物,其外材料为纯羊毛,内充聚酯纤维,该聚酯纤维的化学式为 (COC6H4COOCH2CH2O)n。下列说法中不正确的是





A.羊毛与聚酯纤维的化学成分不相同 B.由单体合成聚酯纤维的反应属加聚反应
C.该聚酯纤维单体为对苯二甲酸和乙二醇 D.聚酯纤维和羊毛一定条件下均能水解
10.下列离子方程式不正确的是
A.100mL0.1mol・L-1的Na2CO3溶液中加入0.01molCH3COOH
CO32―+ CH3COOH = HCO3― + CH3COO―
B.4mol・L-1的NaAlO2溶液和7mol・L-1的HCl等体积互相均匀混合
4AlO2―+ 7H+ + H2O = 3Al(OH)3↓+ Al3+
C.在含有Mn2+的溶液中加入HNO3再加入PbO2,则反应体系显紫红色
5PbO2 + 2Mn2+ + 4H+ = 5Pb2+ + 2MnO4― + 2H2O
D.甲醛溶液中加入足量的银氨溶液并加热
HCHO+2[Ag
(NH3)2]++2OH―![]() HCOO―+NH4++2Ag↓+3NH3+H2O
HCOO―+NH4++2Ag↓+3NH3+H2O
11.下列三种有机物是某些药物中的有效成分。
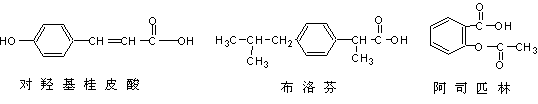
下列说法正确的是
A.三种有机物都能发生水解反应
B.三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
C.使用FeCl3溶液和稀酸可以鉴别这三种有机物
D.将等物质的量的三种物质加入氢氧化钠溶液中,对羟基桂皮酸消耗氢氧化钠最多
12.某溶液中含有NaCl和H2SO4两种溶质,它们的物质的量之比为3:1。用石墨作电极电解该混合溶液时,根据电极产物,可明显地分为三个阶段。下列叙述中错误的是
A.阴极始终只析出H2 B.阳极先析出Cl2,后析出O2
C.电解的最后阶段是电解水 D.溶液的pH不断增大,最后pH小于7
13.2008年北京奥运会“祥云”火炬用的是环保型燃料――丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为:![]() ,下列有关说法正确的是( )
,下列有关说法正确的是( )
A.奥运火炬燃烧主要是将化学能转变为热能和光能
B.丙烷的沸点比正丁烷高
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ/mol
14.下列叙述正确的是( )
A.火法炼铜的反应为Cu2S+O2高温2Cu+SO2,此反应中Cu2S只作氧化剂
B.由海水制淡水可用太阳能蒸发的方法
C.合成纤维的年产量是衡量一个国家石油化学工业发展水平的标志
D.含铅汽油的停止使用是因为铅资源紧张
15.MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中正
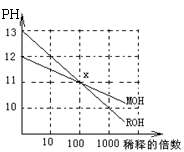 确的是
确的是
A.MOH和ROH都是强碱
B.稀释前,c(ROH)=10c(MOH)
C.常温下pH之和为14的醋酸和ROH溶液等体积混合,
所得溶液呈碱性
D.在x点,c(M+)=c(R+)
16.萜类物质中有许多都已被用于香料工业。常见的有如下几种结构(括号内表示④的结构简式), 关于上述四种香料,下列说法正确的是
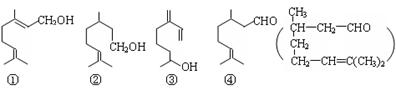
A.④是②的还原产物 B.①③互为同系物
C.②③均属于烯烃 D.③④均能发生消去、酯化反应
08届高三化学月考答卷(六)
一.选择题(本题包括16小题,每小题3分,共48分。每小题只有一个选项符合题意)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | ||||||||
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 |
卷Ⅱ(共60分)
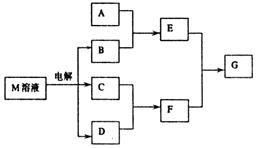
17.(8分)已知物质M由X、Y两种短周期元素组成,X原子的最外层电子数是最内层电子数的![]() ,Y元素最高正价与它的负价代数和为6。M与其它物质的转化关系如下图所示(部分产物已略去):
,Y元素最高正价与它的负价代数和为6。M与其它物质的转化关系如下图所示(部分产物已略去):
|
(1)若A是与X、Y同周期元素的一种常见金属单质,则A与B溶液反应的化学方程式是:
(2)若A是一种常见酸性氧化物,且可用于制造玻璃则E与F反应的离子方程式是:
|
则G的电子式是
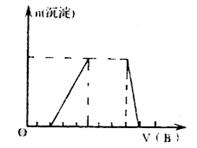
(4)若A是一种溶液,只可能含有H+、NH4+、
Mg2+、Fe3+、Al3+、CO32¯、SO42¯中的某
些离子,当向该溶液中加入B溶液时,发
现生成沉淀的物质的量随B溶液的体积变
化如图所示,由此可知,该溶液中肯定含
有的离子是(写离子符号) 。
18.(12分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH¯、Cl¯、CO32¯、NO3¯、SO42¯ |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能有D反应产生沉淀。
试回答下列问题:
(1)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(2)写出E溶液与过量的B溶液反应的离子方程式:
。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-aKJ・mol-1。请写出B与C的稀溶液反应的热化学方程式
。
(4)在100mL0.1mol・L-1E溶液中,逐滴加入35mL 2mol・L-1NaOH溶液,最终得到沉淀的物质的量为 。
19.(12分)铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
⑴对于问题1,同学们上网查寻,有两种解释:
A、因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属。
B、因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属。
①你认为正确的说法是 。
②若有一黑色粉末,你如何鉴别是铁粉,还是Fe3O4粉末。
③若有一黑色粉末,为铁和四氧化三铁的混合物,你如何证明其中有Fe3O4(只要求简述实验方法)。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A:将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B:将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在 (填仪器名称)中灼烧。
②方法A中,如果高温灼烧后颜色由 变为 ,说明Fe2O3确实发生了变化。能说明生成的一定为FeO吗? ,理由是 。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为 ,
但是,实验结果固体灼烧前后质量比为30 :29,则高温灼烧后生成物是 。
④比较两种方法,你认为较好的方法是 。
20.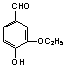 乙基香草醛( )是食品添加剂的增香原料,其香味比香草醛更加浓郁。
乙基香草醛( )是食品添加剂的增香原料,其香味比香草醛更加浓郁。
(1)写出乙基香草醛分子中两种含氧官能团的名称 。
(2)乙基香草醛的同分异构体A是一种有机酸,A可发生以下变化:
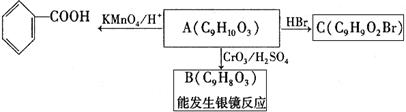
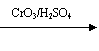 |
提示:①RCH2OH RCHO
②与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧基
(a)由A→C的反应属于 (填反应类型)。
(b)写出A的结构简式 。
![]()
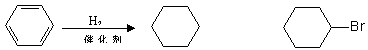
![]() (3)乙基香草醛的一种同分异构体D(
)是一种医药中间体。请设计合理方案
(3)乙基香草醛的一种同分异构体D(
)是一种医药中间体。请设计合理方案
用茴香醛( )合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)。
 |
![]() 例如:
例如:
。
21.A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含有一种官能团,且每个碳原子上最多只连一个官能团:A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请填空:
⑴ A的分子式是 ,其结构简式是 。
⑵ 写出A与足量乙酸在浓H2SO4作用下反应的化学方程式:
。
⑶ 写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是
____________________ __。
![]() 22.快乐是什么?精神病学专家通过实验发现:在大脑的相应部位―“奖赏中心”给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺的结构为:
22.快乐是什么?精神病学专家通过实验发现:在大脑的相应部位―“奖赏中心”给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺的结构为:
回答下列问题:
⑴、多巴胺的分子式为 。
⑵、写出多巴胺与浓溴水反应的化学方程式:
。
⑶、多巴胺可由香兰素与硝基甲烷反应后再经锌汞齐还原水解制得。合成过程可表示如下:
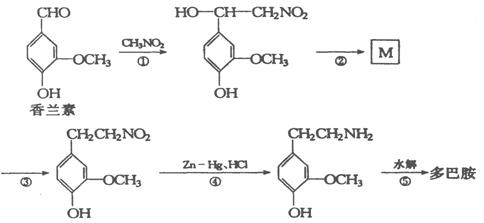
① 反应①属于 反应(填反应类型)。
②写出M的结构简式 。
③多巴胺分子中羟基处于苯环上不同位置时的同分异构体(苯环上的其它结构不变)。
共有 种 。
08届高三化学月考答案(六)
一.选择题: 1~4;DCBD 5~8;DDAC 9~12;BD CD 13~16:ABDB
17.(8分)(1)2Al+2NaOH+2H2O=2NaAlO2+3H2↑(2分)
(2)SiO32-+2H+=H2SiO3↓(2分)
|
(2分) (4)H+、NH4+、Al3+、SO42-(2分)
18.(12分) (1)c(Na+) > c(Cl-) > c(HCO3-) > c(OH-) > c(H+) > (CO32-)
或c(Na+) > c(Cl-) > c(HCO3-) > c(OH-) > c(H+) (3分)
(2)2Al3++3SO42-+3Ba2++8OH-= 2AlO2-+3BaSO4↓+3BaSO4↓+4H2O (3分)
(3)OH-(aq) + H+(aq) = H2O(l);△H=-a KJ/mol
或![]() Ba(OH)2(aq)+HCl(aq)=
Ba(OH)2(aq)+HCl(aq)=![]() BaCl2(aq) + H2O(l);△H=-a KJ/mol
BaCl2(aq) + H2O(l);△H=-a KJ/mol
或Ba(OH)2(aq)+2HCl(aq) = BaCl2(aq) + 2H2O(l);△H=-2a KJ/mol (3分,物质聚集状态、反应热任一方面错都不给分) (4)0.01mol (3分,无单位只给1分)
19.(12分)⑴ ① A (1分)
②取黑色粉末少许于试管中,加适量稀盐酸或稀硫酸,有气泡产生的原黑色粉末为铁,若无气泡产生则原粉末为Fe3O4(2分,其它合理答案亦可)
③用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测有水产生或用纯净的一氧化碳与与黑色粉末加热反应,用澄清石灰水检测有二氧化碳产生(2分,其它合理答案亦可)
(2)①坩埚(1分) ②颜色由红棕色变为黑色。不能,也可能为Fe3O4(3分)
③10/9 ,Fe3O4(2分) ④B(1分)
20. (10分,(1)醛基 (酚)羟基 醚键(两种即可)(2分)(2)(a)取代反应 (2分)
![]()
|
|
CH2OH
![]() (3)
(4分)
(3)
(4分)
21. (12分)I.⑴ C5H12O4
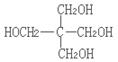 ⑵ C(CH2OH)4+4CH3COOH
⑵ C(CH2OH)4+4CH3COOH![]()
![]() C(CH2OCCH3)4+4H2O
C(CH2OCCH3)4+4H2O
⑶ CH3![]()
![]()
![]() CH2OH HOCH2CH2
CH2OH HOCH2CH2![]()
![]() CH2OH HOCH2
CH2OH HOCH2![]() CH2
CH2![]() CH2OH
CH2OH
22. (6分)(1)C8H11NO2 (2)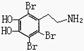
![]() +3Br2→
+3HBr
+3Br2→
+3HBr
![]() (3)①、加成反应 ②、
③、 6
(3)①、加成反应 ②、
③、 6