08届高三上册第二月考考试化学试题
可能用到的相对原子质量:H 1 Cu 64 B 10.8 C 12 N 14 O 16 F 19 Na 23 Mg 24
Al 27 Si 28 S 32 Cl 35.5 Ca 40 Mn 55 Fe 56 Br 80 Ag 108
班级: 姓名: 成绩:
第Ⅰ卷(选择题 共70分)
一、选择题(本题包括10小题,每小题3分,共30分。每个小题只有一个正确选项)
1、正确掌握化学用语和化学基本概念是学好化学的基础。下列有关表述中正确的一组是
A.过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团相同;两者互为同分异构体
B.16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体
C.P4、CH4、NH4+粒子的空间构型均为正四面体型;CO2、C2H2均为直线型分子
D.Ca2+的结构示意图为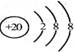 , NH4Cl的电子式为
, NH4Cl的电子式为![]()
2、金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的一些说法不正确的是
A.合金的性质与其成分金属的性质不完全相同
B.工业上金属Mg、Al都是用电解熔融的氯化物制得的
C.金属冶炼的本质是金属阳离子得到电子变成金属原子
D.越活泼的金属越难冶炼
3、阿伏加德罗常数约为6.02×1023 mol-1,下列说法不正确的是
A.常温常压下,22g氧气和26g臭氧所含氧原子总数为3 NA
B.6.2g白磷P4中所含的P-P键的个数为0.3 NA
C.在标准状况下,V L CH2O中含有的氧原子个数为![]()
D.1L 0.5 mol/L CH3COONa溶液中含有的CH3COO-个数为0.5 NA
4、居室装修用石材的放射性常用![]() 作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖。下列叙述中正确的是
作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖。下列叙述中正确的是
A.一个![]() 原子中含有138个中子
原子中含有138个中子
B.Ra元素位于元素周期表中第六周期ⅡA族
C.RaCl2的熔点比CaCl2高
D.Ra(OH)2是一种两性氢氧化物
5、从海水中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳; ②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物; ③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物; ④将得到的产物熔融电解得到镁。下列说法不正确的是
A.此法的优点之一是原料来源丰富
B.①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及化合、分解和复分解反应
D.第④步电解时阴极产生氯气
6、在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M。关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3;② 还原性:Cl->As;③ 每生成7.5gAs,还原剂失去的电子为0.3 mol;④ M为OH-;⑤ SnCl62-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
7、绿色化学是从源头上防止污染产生或将化学过程对环境的负面影响降低到最低限度的化学。不仅化工生产应遵循绿色化学的原则,化学实验也应遵循绿色化学原则,实现原料和过程的绿色化。下列实验或实验过程遵循绿色化学原则的是
A.用多量的氯气进行性质实验
B.用双氧水代替高锰酸钾制氧气
C.用溴水代替碘水进行萃取实验
D.用铜粉代替铜丝进行Cu和浓HNO3的反应
8、2007年3月22日是第十五届“世界水日”。我国纪念“世界水日”和开展“中国水周”活动的宣传主题为“水利发展与和谐社会”。下列有关活动不符合这一主题的是
A.大力提倡全民节约用水,加强城市生活污水处理,坚持达标排放
B.大力推广使用纯净水代替自来水作生活用水,以保障用水安全
C.加快产业结构调整,建立水资源节约型、环保型的国民经济体系
D.加强工业用水净化系统工程的改造,提高水的重复利用率
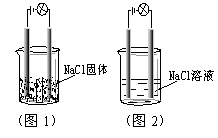 9、一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
9、一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl在水溶液中电离出了可以自由移动的离子
D.NaCl溶液中水电离出大量的离子
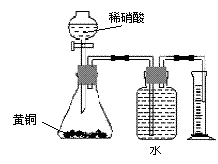
10、下列实验的设计不可行的是
A.在浓氨水中加入生石灰可以制取少量的NH3
B.用水就一次性鉴别溴苯、苯、乙酸三种物质
C.用如图所示的装置测定黄铜(Cu、Zn合金) 中Zn的含量
D.除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质是H2O、 Ba(OH)2、Na2CO3、HCl
二、不定项选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
11、下列离子方程式书写正确的是( )
A.等体积等物质的量浓度的氢氧化钡稀溶液与碳酸氢铵稀溶液混合
Ba2++OH一+HCO3一=BaCO3↓+H2O
B.氯化铝溶液中加入过量的氨水
A13++4NH3・H2O=4NH4++A1O2-+2H2O
C. 向次氯酸钙溶液中通人过量的二氧化硫
Ca2++2C1O一+SO2+H2O=CaSO3↓+2HClO
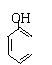 D. 碳酸钠溶液中加入过量的苯酚
D. 碳酸钠溶液中加入过量的苯酚
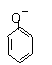 |
+CO32-→ +HCO3-
12、2004年7月德俄两国化学家共同宣布,在高压下氮气会聚合生成高聚氮,这种高聚氮的晶体中每个氮原子都通过三个单键与其它氮原子结合并向空间发展构成立体网状结构。已知晶体中N-N键的键能为160 kJ・mol-1,而N≡N的键能为942 kJ・mol-1(键能表示形成化学键释放的能量或者破坏化学键消耗的能量)。则下列有关说法不正确的是
A.键能越大说明化学键越牢固,所构成物质越稳定
B.高聚氮晶体属于原子晶体
C.高聚氮晶体中n(N)∶n(N-N)=1∶3
D.用作炸药或高能材料可能是高聚氮潜在的应用
13、一定条件下,体积为10L的密闭容器中,1mol X和1mol Y进行反应:
2X(g)+Y(g)![]() Z(g),经60s达到平衡,生成0.3mol Z。下列说法正确的是
Z(g),经60s达到平衡,生成0.3mol Z。下列说法正确的是
A.若增大压强,则物质Y的转化率减小
B.将容器体积变为20 L,Z的平衡浓度变为原来的![]()
C.以X浓度变化表示的反应速率为0.001mol/(L・S)
D.若升高温度,X的体积分数增大,则该反应的△H>0
14、臭氧分子的结构与SO2(极性分子)相似,可读做二氧化氧,在臭氧层中含量达0.2 ppm(ppm表示百万分之一)。臭氧是氧气吸收了太阳的波长小于242 nm的紫外线形成的,不过当波长在220 nm~320 nm的紫外线照射臭氧时,又会使其分解。下列说法中正确的是
A.打雷时也能产生臭氧,臭氧分子是直线型分子
B.臭氧转化为氧气和氧气转化为臭氧均须吸收能量
C.臭氧和氧气的相互转化能保持大气中臭氧的含量基本稳定
D.向大气中排放氮的氧化物和氟氯代烃均能加快臭氧的分解
15、常温下,下列各溶液的叙述中正确的是
A.0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后溶液显酸性
c (Ac-)>c (Cl-)>c (H+)>c (HAc)
B.pH=7的醋酸钠和醋酸混合液中:c(Na+)= c(CH3COO-)
C.0.1mol/L的醋酸的pH=a,0.01mol/L的醋酸的pH=b,则a+1>b
D.已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,
[c(Na+)-c(F-)]< [c(K+)-c(CH3COO-)]
16、用右图表示的一些物质或概念间的从属关系中不正确的是
| X | Y |
| |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 苯的同系物 | 芳香烃 | 芳香族化合物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 电解质 | 离子化合物 | 化合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
17、X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A.X与W可以形成W2X、W2X2两种化合物
B.Y元素最高价氧化物对应水化物的化学式为H2YO4
C.原子序数由小到大的顺序为W<X<Y<Z
D.Y、Z两元素的简单离子的半径Y>Z
![]()
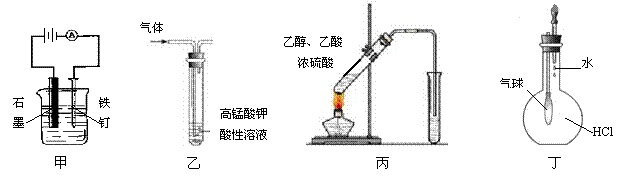 18、用下列实验装置进行的实验中,能达到相应实验目的的是
18、用下列实验装置进行的实验中,能达到相应实验目的的是
A.装置甲:防止铁钉生锈 B.装置乙:除去乙烯中混有的乙炔
C.装置丙:实验室制取乙酸乙酯 D.装置丁:验证HCl气体在水中的溶解性
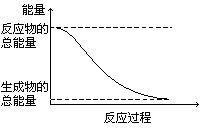
19、下列变化为放热反应的是
A.H2O(g)=H2O(l) △H=-44.0 kJ/mol
B.2HI(g)=H2(g)+I2(g) △H=+14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如右图所示的化学反应
20、镍-镉可充电电池,电极材料是Cd和NiO(OH),电解质是KOH,放电时的电极反应式是
 Cd+2OH-―2e-===Cd(OH)2,2NiO(OH)+2H2O+2e-===2Ni(OH)2+2OH- 下列说法不正确的是
Cd+2OH-―2e-===Cd(OH)2,2NiO(OH)+2H2O+2e-===2Ni(OH)2+2OH- 下列说法不正确的是
A.电池的总反应式是Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2
B.电池充电时,镉元素被还原
C.电池放电时,电池负极周围溶液的pH不断减小
D.电池充电时,电池的负极和电源的正极连接
第Ⅱ卷(共80分)
三、填空题(本题包括3小题,共28分)
21.(8分)工业上制取CuCl2的生产流程如下:
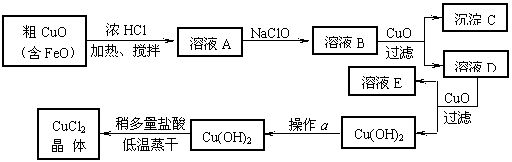
请结合下表数据,回答下列问题:
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 溶度积/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
⑴ 溶液A中加入NaClO的目的是 ;
⑵ 在溶液B中加入CuO的作用是 ;
⑶ 操作a的目的是 ;
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
22.(8分)合成氨是人类科学技术发展史上的一项重大突破,解决了地球上因粮食不足而导致的饥饿与死亡。
⑴ 合成氨反应的热化学方程式如下:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ/mol。为了提高NH3的产率,应如何选择反应条件
;
2NH3(g) ΔH=-92.4kJ/mol。为了提高NH3的产率,应如何选择反应条件
;
⑵ 在一密闭容器中以体积比1∶3通入氮氢混合气体,使N2的物质的量浓度为amol/L。在一定条件下发生反应,经ts后达到化学平衡,混合气体中NH3的体积分数为b。则从反应开始至达到化学平衡时H2的平均反应速率为 ,该条件下反应的平衡常数K= (用含a、b的函数式表示,不必化简)。
⑶ 液氨与水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为:
2NH3![]() NH4++ NH2ˉ(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4=
。
NH4++ NH2ˉ(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4=
。
23.(12分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O NH4HCO3 ; NH4HCO3+NaCl NaHCO3↓+NH4Cl ;
![]() 2NaHCO3 Na2CO3+CO2↑+H2O
2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的
方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
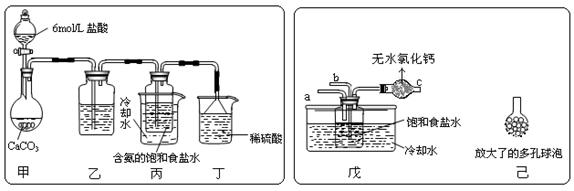
试回答下列有关问题:
![]() (Ⅰ)乙装置中的试剂是 ;
(Ⅰ)乙装置中的试剂是 ;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是 ;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法: 。
四、(本题包括3小题,共32分)
24.(12分)茶是我国人民喜爱的饮品。某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有Ca、A1、Fe三种元素。
【查阅部分资料:草酸铵[(NH4)2C2O4]属于弱电解质;Ca、A1、Fe完全沉淀的pH:Ca(OH)2:pH≥13;A1(OH)3;pH≥5.5;Fe(OH)3:pH≥4.1)
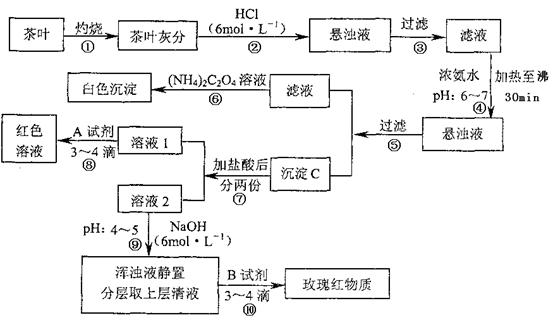
试根据上述过程及信息填空:
(1)步骤④用浓氨水调节pH后,加热至沸30min的作用是 。
(2)写出检验Ca2+的离子方程式 。
(3)写出沉淀C所含主要物质的化学式 。
(4)写出步骤⑧用A试剂生成红色溶液的离子方程式 。
(5)步骤⑨的作用是 ,猜测步骤⑩的目的是 。
25.(10分)如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:
2
A(?)+B(?)![]() x C(g);ΔH<0
x C(g);ΔH<0
平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。
 |
⑴根据题中数据计算,x =_________、y =_________;
⑵如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
| 可能的情形 | A、B是否为气态 | z与y的大小关系 | M(B)与M(C)的大小关系 (M表示摩尔质量) | |
| A | B | |||
| ① | 是 | 不是 | z = y | 前面的结论与此无关 |
| ② | ||||
| ③ | ||||
26.(10分)“在火星上找到水存在的证据”位居《Science》杂志评出的2004年10大科技突破之首,由此火星问题引发了科学家的极大关注,也引起了广大群众的兴趣。
(1) 火星大气中二氧化碳占95.23%(体积分数),氧气约占0.13%,岩层中含有较丰富的镁资源。如果让火星上的镁单质燃烧,可以作为未来火星的燃料,则发生的主要反应的化学方程式为: 。
(2) 2004年,美国科学家通过“勇气”号太空车探测出火星大气中含有一种称为硫化羰的物质,已知硫化羰分子式为COS,与二氧化碳的结构相似,但能在氧气中完全燃烧。请画
出硫化羰的电子式 ;硫化羰在氧气中完全燃烧的化学方程式为 。
(3) “机遇号”火星车发回来的信息经检测,火星上有针铁矿[FeO(OH)]和黄钾铁矾,黄钾铁矾的化学式为KFe3(SO4)2(OH)6 ,从而证明火星表面曾经存在过水。两种铁的化合物中铁元素的化合价为 ,铁在周期表的位置是 ,生铁、钢、不锈钢都属于铁的 。
五、(本题包括1小题,共10分)
27.(10分)以石油裂解得到的乙烯和1,3-丁二烯为原料,经过下列反应合成高分子化合物H,该物质可用于制造以玻璃纤维为填料的增强塑料(俗称玻璃钢)。
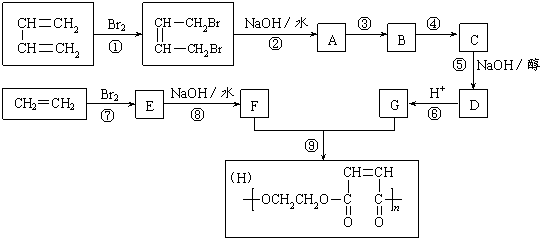
请按要求填空:
(1)写出下列反应的反应类型:
反应①________________,反应⑤________________,反应⑧________________。
(2)反应②的化学方程式是______________________________________________。
(3)反应③、④中有一反应是与HCl加成,该反应是________(填反应编号),设计这一步反应的目的是__________________________________________________,物质C的结
构简式是_______________________。
六、选做题(本题包括2小题,各10分,任选一道题作答。作答两道题,以第28题计分)
28.(A)有机化学(10分)
(1)苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如图所示:
![]() 则苯氯乙酮不可能具有的化学性质是 (填字母序号)。
则苯氯乙酮不可能具有的化学性质是 (填字母序号)。
a.加成反应 b.取代反应 c.消去反应
d.水解反应 e.银镜反应
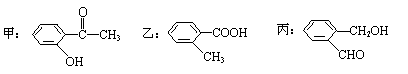
(2)今有化合物
①请写出丙中含氧官能团的名称: ;
②请判别上述哪些化合物互为同分异构体: ;
③请按酸性由强至弱排列甲、乙、丙的顺序: ;
(3)由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。
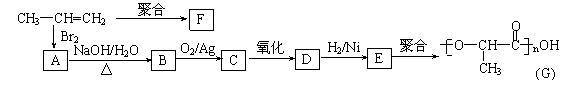
①丙烯分子中,最多有 个原子在同一个平面上;
②聚合物F的结构简式: ;
③B转化为C的化学方程式: ;
④在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式: 。
(B)物质结构与性质(10分)
碳是形成化合物最多的元素,其单质与化合物广布于自然界。
 (1)碳原子的核外电子排布式为 。与碳同周期的非金属元素N的第一电离能大于O的第一电离能,原因是
;
(1)碳原子的核外电子排布式为 。与碳同周期的非金属元素N的第一电离能大于O的第一电离能,原因是
;
(2) CS2是一种重要的有机溶剂,CS2分子的空间构型为 ;写出一种与CS2互为等电子体的物质的化学式 ;
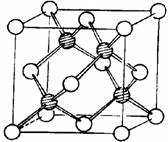
(3) 冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如右图
其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立
方体内)类似。每个冰晶胞平均占有 个水分子,冰晶胞与金刚
石晶胞微粒排列方式相同的原因是 。
高三第二月考考试化学试题答案
第I卷(共70分)
一、二题答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | B | D | A | D | A | B | B | C | C |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | D | C | C | CD | BC | C | A | AD | D | D |
第Ⅱ卷(共80分)
三、填空题(本题包括3小题,共28分)
21.(8分)⑴ 将Fe2+氧化为Fe3+而使分离更加完全
⑵ 调节溶液的pH为3~4,使Fe3+完全转变为Fe(OH)3沉淀而分离Fe3+
⑶ 洗涤Cu(OH)2表面的可溶性杂质
⑷ 抑制Cu2+的水解(每空2分,本题共8分
22.(8分)⑴ 增大压强,适当降低温度
⑵ ![]() mol/(L・s)
mol/(L・s) 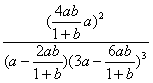
⑶ 15 (每空2分,本题共8分)
23.(12分) (1)c (1分) (2)①(Ⅰ)饱和碳酸氢钠溶液;
(Ⅱ)吸收未反应的NH3(答“防止倒吸”或“吸收CO2”不给分));
(Ⅲ)过滤 (每空1分,共3分)
②(Ⅰ)a、NH3, b、CO2; (每空1分,共4分)
(Ⅱ)增大气体与溶液接触面积,提高CO2吸收率; (2分)
(3)用碳酸氢铵与适量饱和食盐水反应。(或往烧碱溶液中通入过量CO2 ;往饱和Na2CO3 溶液中通入过量CO2 等。其他合理方法均可) (2分)
四、(本题包括3小题,共32分)
24.(12分)(1)使Al3+、Fe3+完全沉淀(2分)
(2)Ca2++(NH4)2C2O4 CaC2O4↓+2NH4+(2分)
(3)Fe(OH)3、Al(OH)3(各1分,共2分)
(4)Fe3++3SCN―
Fe(SCN)3(写成其它正确的络合离子形式给分,2分)
(5)使Fe3+转化为Fe(OH)3沉淀;(2分)检验Al3+(或铝元素)存在。(2分)
25.⑴ x =2 y =1.6 (4分)
⑵(A、B的状态合起来算一格,每格1分,共6分)
| 是 | 是 | z < y | 前面的结论与此无关 | |
| 不是 | 是 | z < y | M(B)<M(C) | |
26.(10分)
(1) 2Mg+CO2![]() 2MgO+C (2分)
2MgO+C (2分)
(2) ![]() (2分)
2COS+3O2
(2分)
2COS+3O2![]() 2CO2+2SO2 (2分)
2CO2+2SO2 (2分)
(3) +3,第四周期第Ⅷ族,合金(共4分)
五、有机题(本题包括1小题,共10分)
27.⑴加成反应 消去反应 取代反应 (3分)
⑵![]() +2NaOH→
+2NaOH→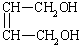 +2NaBr (2分)
+2NaBr (2分)
⑶ ③ 保护A分子中C=C不被氧化 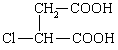 (5分)
(5分)
六、选做题(本题包括2小题,各10分,任选一道题作答。作答两道题,以第28题计分)
28.(A)有机化学(10分)
(1)c、e (1分)(2)①醛基、羟基(1分) ②甲 乙 丙(1分) ③乙>甲>丙(1分)
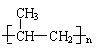 |
(3)① 7 (1分) ② (1分)
![]()
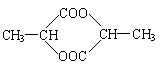 ③ (2分)
③ (2分)
④ (2分)
(B)物质结构与性质(10分)
⑴ 1s22s22p2 N原子2p轨道半充满,能量低
⑵ 直线形 CO2
⑶ 8 氢键具有方向性,每个水分子与相邻的4个水分子形成氢键
(第1小题每空1分,其余每空2分,本题共10分)
 Z
Z