2008级高三理综化学第二次诊断性考试
理科综合能力测试化学试题
本试卷分第I 卷(选择题)和第II卷(非选择题)两部分,两卷共8 页.满分300 分,考试时间150 分钟.第I 卷答案涂在答题卡上,第II卷答案写在答题卷上。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Fe 56 Cu 64
第I 卷
(选择题,共126 分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号、考试科目用4B 或5B 铅笔准确涂写在答题卡上,同时将第II 卷答卷密封线内的项目填写清楚.
2.第I 卷每小题选出答案后,用4B 或5B 铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦擦干净后,再选涂其它答案,不能答在试题卷上。
一、选择题(本题包括13 小题。每小题只有一个选项符合题意。每小题6 分)
6.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)等种类。PE 保鲜膜可直接接触食品,PVC 保鲜膜则不能直接接触食品,它对人体有潜在危害。下列有关叙述不正确的是
A.PE、PVC 都属于链状高分子化合物,受热易熔化
B.PE、PVC 的单体都是不饱和烃,能使溴水褪色
C.焚烧PVC 保鲜膜会放出有毒气体HCl
D.废弃的PE 和PVC 均可回收利用以减少白色污染
7.科学家已获得了极具理论研究意义的N4 分子,其结构为正四面体(如右图所示),与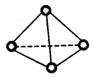 白磷分子相似。已知断裂1 mo1N 一N 键吸收193kJ 热量,断裂1 molN≡N 键吸收94IkJ 热量,则
白磷分子相似。已知断裂1 mo1N 一N 键吸收193kJ 热量,断裂1 molN≡N 键吸收94IkJ 热量,则
A.N4 的熔点比P4 高
B.1 molN4气体转化为N2时要吸收748kJ 能量
C.N4是N2的同系物
D.1 mol N4 气体转化为N :时要放出724kJ 能量
8.氟气是氧化性最强的非金属单质。等物质的量的F2与NaOH 在稀溶液中反应生成NaF、H2O 和一种气体,该气体是
A.HF B.OF2
C.H2 D.O2
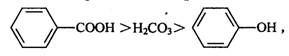
9.已知酸性: 综合考虑反应物的转化率和原
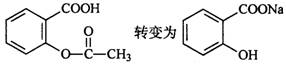
料成本等因素,将 的最佳方法是
A.与稀H2SO4 共热后,加人足量的NaOH 溶液
B.与稀H2SO4 共热后,加人足量的NaHCO3 溶液
C.与足量的NaOH 溶液共热后,再通人足量CO2
D.与足量的NaOH 溶液共热后,再加人适量H2SO4
10.56 gFe 粉投人500g 稀HNO3中,两者恰好完全反应放出NO,溶液增重26g ,则反应后溶液中的金属阳离子
A.只有Fe3+
B.只有Fe2+
C.有Fe2+和Fe3+ D.无法确定
11.常温下,对于物质的量浓度相等、体积相同的NaCl溶液与NaF 溶液,下列判断错误的是
A.在NaCl 溶液中一定有c(Na+)+ c ( H+) = c (OH一)+ c(
Cl-)
B.在N 亦溶液中一定有:c(Na+)+ c ( H+) = c (OH一)+ c(F-)
C.NaCl 溶液中的氢离子浓度比NaF
溶液中的氢离子浓度大
D.由于F-水解,NaF 溶液中F- 减少n molF-,必然增加n mol OH-
12.八角茴香含有一种抗禽流感病毒的重要成分一一莽草酸,其结构简式为:
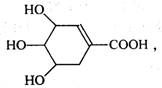
则莽草酸不具有的性质是
A.遇FeC13 溶液呈紫色
B.能发生消去反应
C.能与H2发生加成反应
D.1 mol 莽草酸只能与1 mol NaOH 反应
l3.在一定温度、一定体积的密闭容器中有如下平衡:H2 (g) + I2 (g)![]() 2HI (g),已知H2和I2
的起始浓度均为a mol / L ,达平衡时HI 的浓度为bmol / L;若H2和I2的起始浓度均为2a mol / L,则平衡时H2的物质的量浓度是
2HI (g),已知H2和I2
的起始浓度均为a mol / L ,达平衡时HI 的浓度为bmol / L;若H2和I2的起始浓度均为2a mol / L,则平衡时H2的物质的量浓度是
A.b mol / L B.mol / L
C.(2a 一b)mol / L D.( a 一 )mol / L
高中2008 级第二次诊断性考试
理科综合能力测试化学试题
第II卷
(非选择题,共 10 题,共 174 分)
注意事项:
答第II卷前,考生务必将自己的姓名、准考证号用钢笔或圆珠笔(蓝、黑色)写在答题券密封线内相应的位置。答案写在答题卷上,不能答在试题卷上。
26.(18 分)某化学学习小组的同学设计实验来探究草酸受热分解的产物,他们将草酸受热分解得到的气体通过如下图所示装置:
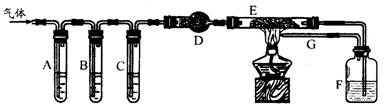
A、C、F 中盛装澄清石灰水,B 中盛NaOH 溶液,E 中装有CuO 。请填写下列空白:
(l)证明产物中有CO2的现象是___________________________________,证明产物中有CO 的现象是__________________________________________________。
(2)导管G 的作用是_______________________________________________。
(3)小李同学查阅相关资料发现:草酸是二元酸,酸性比碳酸强,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色不溶物。小李通过进一步研究认为:草酸蒸气与石灰水反应生成草酸钙白色沉淀,对实验有干扰,因此需要在装置A 之前增加一个装有________(填写下列编号字母)的洗气装置。
a.水 b.NaOH 溶液 c.Na2CO3 溶液 d.饱和NaHCO3 溶液
(4)如果在E 管中盛装CuO 和Cu2O的混合物,根据F 瓶增重可以测定混合物中CuO 的质量。当CuO 和Cu2O的混合物7.6g 全部被还原后,F 装置增重3.3g ,混合物中CuO 的质量为____________g ;当原混合物质量为a g ,反应后F 装置增重bg 时,b 的取值范围是___________________________________(用含a 的代数式表达)。
27.( 16 分)A、B、C、D、G 都是含有同一种短周期元素的化合物,E 是氧化物,H 是单质。根据下图转化关系(反应条件及部分产物已略去)填空:
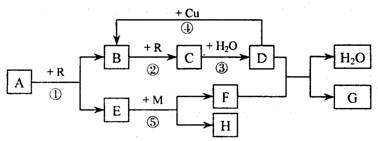
( l )若A、B、C、D、G 均含X 元素,且A 的一个分子中只含有10 个电子,G 是复合肥料,则反应①、②、③ 是工业生产__________________的基本原理,M 的化学式是__________。其中反应① 的化学方程式是_________________________________________;反应④ 的离子方程式是________________________________________________。
( 2 )若A、B、C、D、G 均含Y 元素,Y 元素处于X的相邻周期、相邻族,G 可作净水剂,则反应①、②、③ 是工业生产______________________的基本原理,M 元素在周期表中的位置是____________________________。其中反应① 的化学方程式是_________
________________________;反应①一⑤ 中,既属于化合反应又属于非氧化还原反应的是___________________________。
28.( l 2 分)有机物A 只含C、H、O 三种元素,相对分子质量为130 ,在酸性条件下,1 molA 水解得到1mol B 和l mol 乙二醇。B 能使溴水褪色,还能溶解碳酸钙,B 与H2的加成产物分子中有2 个甲基。请回答下列问题:
( l ) B 的相对分子质量为_____________________,结构简式是_______________。
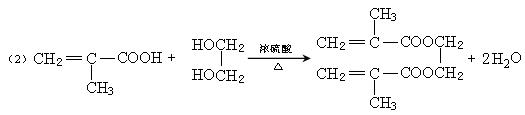
( 2 ) 1 mol 乙二醇与2 mol B 反应的化学方程式是__________________________________________________________________________。
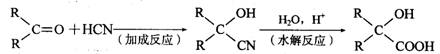
已知:
由丙烯合成B 可以经过下列五步反应:①与H2O 加成 ②催化氧化 ③与HCN 加成 ④水解 ⑤消去, 则反应② 的化学方程式是______________________________________,反应④ 的产物结构简式是________________。
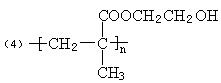
( 4 )软质隐形眼镜常用A 经加聚反应生成的HEMA 制成超薄镜片,HEMA 的结构简式是_________________________________________________________________________。
29.( 14 分)2007 年11 月,我国自行研制的长征三号甲运载火箭载着“嫦娥一号”探测器升空,成功实现了绕月飞行。第一、二级火箭使用的推进剂是液态偏二甲肼和四氧化二氮。已知偏二甲肼含C、H、N 三种元素,其中C、N 两元素的质量分数分别为40.0 %和46.7 % , 在气态时,偏二甲肼的密度是相同条件下H2密度的30 倍。请填写下列空白:
( l )偏二甲肼的分子式为________________;若0 . 2 mol 液态偏二甲肼与液态N2O4 完全反应,生成气态的N2、H2O 和CO2,同时放出510 kJ 热量,试写出该反应的热化学方程式:__________________________________________________________________________
( 2 )满足偏二甲肼分子式的同分异构体有____________ 种。写出符合分子中含两个甲基的结构简式:_________________________________________________。
( 3 )肼(N2H4)又称联氨,是一种可燃性液体,也可用作火箭燃料。肼一空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH 溶液,放电时生成氮气和水,则肼一空气燃料电池放电时,负极的电极反应式是____________________________________。
( 4 )肼可看作是氨分子内的一个氢原子被氨基取代的衍生物,肼的水溶液呈弱碱性,是因为溶液中存在平衡:H2N一NH2+HZO![]() ___________________________。
___________________________。
参 考 答 案
第I卷
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | B | D | B | C | A | BD | A | C |
注:11题可能有问题,B、D是相关联的选项,即D错,B也错;B对,D也对。
第II卷
26.(1)A中出现白色浑浊 F中出现白色浑浊
(2)把未反应的CO导入酒精灯火焰燃烧,防止CO污染空气
(3)a
(4)3.51g () < b < (1.25a)
27.(1)硝酸 K(或K2O2、KO2)
4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
3Cu+8H++2NO3-=3Cu2=+2NO↑+4H2O
(2)硫酸 第3周期IIIA族
4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
③
28.(1)86 CH2=C(CH3)COOH
(3)CH3CH(OH)CH3![]() CH3COCH3+H2O
CH3COCH3+H2O
(CH3)2C(OH)COOH
29.(1)C2H8N2
C2H8N2(l)+2N2O4(l)==3N2(g)+4H2O(g)+2CO2(g); ΔH==-2550kJ/mol
(2)6 CH3NHNHCH3 (CH3)2NNH2
(3)N2H4-4e-+4OH-=N2+4H2O
(4)H2N-NH3++OH-