08届高三实验班化学第三次月考
本试题分为第Ⅰ卷和第Ⅱ卷两部分,总分108分,
第Ⅰ卷(共48分)
一、选择题(本题共16个小题,每小题3分,共48分。每小题只有一个选项符合题意)
1、接触法制硫酸的过程中,对废气、水、渣、热的处理正确的是①尾气用氨水处理②污水用石灰乳处理③废渣用来制水泥、炼铁④设置热锅炉产生蒸气、供热或发电
A.①②③④都正确 B.只有①②③正确
C.只有②③④ 正确 D.只有①②④ 正确
2、下列有关实验事故的处理或实验操作的叙述中,正确的是
A.浓硫酸不小心沾到皮肤上,立即用稀NaOH溶液洗涤
B.用分液漏斗将甘油和水的混合液体分离
C.若皮肤不慎沾到苯酚,应立即用酒精清洗
D.为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
3、在某澄清、透明的浅黄色溶液中,可能含有下列八种离子:H+、NH4+、![]() 、Ba2+、Al3+、SO42-、HCO3-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括K+和OH-)有
、Ba2+、Al3+、SO42-、HCO3-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括K+和OH-)有
A、4种 B、5种 C、6种 D、7种
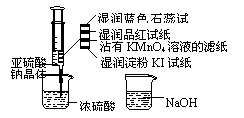 4、如图,在注射器中加入少量Na2SO3晶体,并吸 入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
4、如图,在注射器中加入少量Na2SO3晶体,并吸 入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
A.蓝色石蕊试纸先变红后褪色
B.品红试纸、沾有KMnO4溶液滤纸均褪色证明了SO2漂白性
C.湿润淀粉KI试纸未变蓝说明I2的氧化性弱于SO2
D.NaOH溶液可用于除去实验中多余的SO2
7、下列4组连线中,完全正确的一组是( )
A. B.
B.
C. D.
D.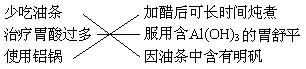
8、下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是:①碳酸钠溶液与盐酸;②偏铝酸钠溶液与盐酸;③苯酚钠溶液和CO2;④硝酸银溶液和氨水;⑤氯化铝溶液与氨水;⑥碳酸氢钠溶液与澄清的石灰水。
A.③⑤ B.①③⑥ C.仅有⑤ D.②④
9、已知几种阴离子还原性强弱顺序为OH-<Cl-<Br-<I-<S2-。若在某溶液含有相同浓度的OH-、Cl-、Br-、I-、S2-,当向其中逐滴加入新制的饱和氯水直至过量时,最后被氧化的离子是
A. Br- B. Cl- C. OH- D. S2-
10、某有机化合物仅由碳、氢、氧三种元素组成,其相对分子质量小于200,若已知其中氧的质量分数为40%,则分子中碳原子的个数最多为( )
A、5 B、6 C、7 D、8
11.用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是
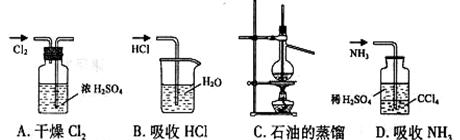 |
12、工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2。为了便于监控,实施环境保护,下列适合测定硫酸尾气SO2含量的是
A、品红溶液 B、氨水、酚酞试液
C、碘水、淀粉溶液 D、以上都能
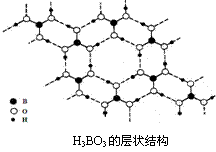 13、正硼酸(H3BO3)是一种类似于石墨的片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如右图所示)。下列有关说法正确的是
13、正硼酸(H3BO3)是一种类似于石墨的片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如右图所示)。下列有关说法正确的是
A.正硼酸晶体属于原子晶体
B.H3BO3分子熔沸点较高
C.分子中硼原子最外层为8电子稳定结构
D.含1molH3BO3的晶体中有3mol氢键
14.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同
(选项中m、n均为正整数)。下列说法正确的是
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
15.下列实验报告记录的实验现象正确的是
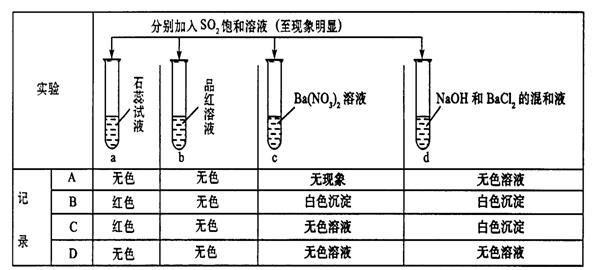 |
16. 在环境检测中常用检气管法来测定空气中S02的含量,原理是S02与KIO3发生反应,用一种有机物作指示剂,其可能反应如下(未配平):
①KIO3 + SO2 + H2O → I2 + H2SO4 + KHSO4 ②KIO3 + SO2 + H2O → KI + H2SO4
则下列说法正确的是
A.检气管法是按照反应①原理设计的
B.检气管法是按照反应②原理设计的
C.反应①②均可以设计成检气管法,但考虑到相同量KIO3 ①消耗SO2少,所以检气管法是按①设计的
D.反应①②均可以设计成检气管法,但考虑到相同量KIO3 ②消耗SO2多,所以检气管法是按②设计的
2008届高三第三次月考化学试卷答题卷
班次 姓名 计分
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 |
第Ⅱ卷(共60分)
二、填空题
17、(12分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,确定一定存在的离子是 ;可能存在的离子是 ;
一定不存在的离子是 。
18、(15分)物质A、D及F的水溶液均呈黄色,D是单质,F的溶液遇苯酚显紫色,A是一种重要工业生产中的主要原料。且A、C、D均含有某一非金属元素,C的相对分子质量与过氧化氢的相对分子质量相等。反应过程中生成的水等与转化无关的物质已经略去。这些物质有以下转化关系。试回答以下问题:
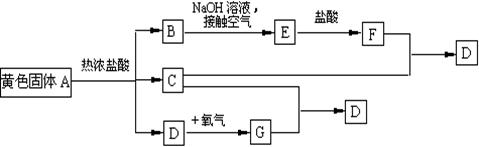
(1)A是 ,C是 ,F是 (均填化学式)。
(2)A与热盐酸反应的离子方程式为
(3)写出该框图中由B→E的化学方程式
 19、(20分)常见的粗盐主要含有NaCl和少量的MgCl2、CaCl2,由于有MgCl2和CaCl2的存在,使得食盐容易板结,下面实验可以确定粗盐中NaCl的质量分数,也可以制得纯净的NaCl,根据实验步骤填写下列空白:
19、(20分)常见的粗盐主要含有NaCl和少量的MgCl2、CaCl2,由于有MgCl2和CaCl2的存在,使得食盐容易板结,下面实验可以确定粗盐中NaCl的质量分数,也可以制得纯净的NaCl,根据实验步骤填写下列空白:
①调整托盘天平零点
②称取样品W克
③将样品溶解于适量的蒸馏水
④滴加稍过量的A溶液,有沉淀产生,沉淀完全后过滤
⑤将得到的滤渣用蒸馏水多次洗涤,烘干,得纯净固体W1克
⑥滤液中加入稍过量的B溶液,又待沉淀完全后过滤
⑦将⑥得到的滤渣用蒸馏水多次洗涤,烘干,得纯净固体W2克
⑧在最后得到的滤液中加入稍过量C溶液,加热蒸发溶剂得到纯净![]() 固体W3克
固体W3克
问题:
(1)调整天平零点时,若指针偏向左边,应将左边的螺丝帽向(填左、右) 旋转。
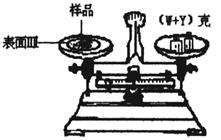
(2)某学生用已知质量Y克的表面皿,准确称取W克样品,他在托盘天平的右盘上放入(W+Y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边(如图所示),这时样品的实际质量m (填>,<,=)W。
(3)加入的试剂A是 ,B是 ,C是 。
(4)检验步骤④中A是否过量的方法是 。
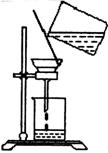 (5)过滤时,某学生的操作如图,明显的错误有 处。
(5)过滤时,某学生的操作如图,明显的错误有 处。
(6)两次洗涤沉淀,为了检验沉淀是否洗净,应在最后几滴洗出液中加入 ,若 表示沉淀已洗净。
(7)该粗盐中![]() 的质量分数的计算式是
的质量分数的计算式是
。
20、(13分)含氮废水进入水体而对环境造成的污染越来越严重,某课外兴趣小组先测定某废水中含NO3-为3×10-4mol/L,而后用金属铝将NO3-还原为N2,从而消除污染。
(1)配平下列有关反应的离子方程式:
NO3-+ Al+ H2O→ N2↑+ Al(OH)3↓+ OH-
(2)上述反应中,还原剂是________,被还原的元素是___________,每生成2molN2,将有_______mol电子发生转移。
(3)有上述废水100m3,若要完全消除污染,则所耗金属铝的质量为________kg。(需要有过程)
湖北省监利一中2008届高三化学第一次联考
答 题 卷
一、选择题(本题共12个小题,每小题4分,共48分。每小题只有一个选项符合题意)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 |
13、(12分)一定存在的离子是 ;
可能存在的离子是 ;一定不存在的离子是 。
14、(15分) A ;B ;C ;
D ;E 。
15、(20分)
(1) (2)
(3)加入的试剂A是 ,B是 ,C是 。
(4) 。
(5)
(6) , 。
(7)
。
16、(13分)
(1) NO3-+ Al+ H2O→ N2↑+ Al(OH)3↓+ OH-
(2) , , 。
(3)金属铝的质量为________kg。计算过程:
湖北省监利一中2008届高三化学第一次联考
参考答案
一、选择题(本题共12个小题,每小题4分,共48分。每小题只有一个选项符合题意)
1、A 2、A 3、C 4、B 5、A 6、B 7、A 8、C 9、D 10、B 11、D 12、D
13、(12分)一定存在NH4+ 、K+ 、CO32-、SO42- ;
可能存在Cl-; 一定不存在Ba2+、Mg2+(每空4分)
14、(15分)Na2CO3 Ba(OH)2 Mg(HCO3)2 AlCl3 Fe2(SO4)3(每空3分)
15、(20分) (每空2分)
(1)右 (2)<
(3)NaOH溶液 Na2CO3溶液 盐酸
(4)用玻璃棒蘸取试液点在红色石蕊试纸上,试纸变蓝,则加入A过量。
(5)2
(6)AgNO3溶液 无沉淀产生
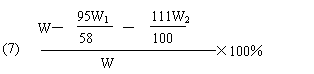 |
16、(13分) (1)6、10、18、3、10、6;(3分)
(2)Al (2分) N(2分) 20(2分)
(3)1.35;(4分)
n(NO3-)==3×10-4mol/L×l00×1000L==30mol,n(Al)==50mol。