08届高三化学第一次月考试卷
本试卷分为第I 卷(选择题)和第II卷(非选择题)两部分,第I卷1至2页,第II卷3至5页。试题分值120分。考试时间100分钟。
第I卷 (选择题 共56分)
注意事项:
1.答第I卷之前,考生务必将自己的姓名、准考证号、考试科目写清楚,用铅笔涂写在答题卡上。
2.每小题选出答案后,用铅笔把答题卡上对应的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案,不能写在试卷上。
3.考试结束,监考人将本试卷和答题卡一并收回。
可能用到的相对原子质量 H:1 O:16 P:31 Cl:35.5 S:32 Br:80
Na:23 Mg:24 Fe:56 Ba:137 Mn:55
一、选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意。)
1.下面是人们对于化学科学的各种常见认识,其中错误的是
A.化学将为环境、能源、资源等问题的解决提供有力保障
B.化学正发展成为一门实验与理论互相结合、互相渗透的科学
C.化学是一门具有极强实用性的自然科学
D.化学是一门纯实验的自然科学,实验是探究化学过程的唯一途径
2.在盛放乙醇的试剂瓶的标签上应印有下列警示标记中的




A B C D
3.选择萃取剂将碘水中的碘分离出来,这种萃取剂应具备的性质是
A.不溶于水,且比水更容易使碘溶解
B.不溶于水,且必须易与碘发生化学反应
C.不溶于水,且必须比水的密度大
D.不溶于水,且必须比水的密度小
4.下列溶液中,氯离子浓度最大的是:
A. 100mL 1mol/L的NaCl溶液 B. 150mL 1mol/L的MgCl2溶液
C. 200mL 1mol/L的HCl溶液 D. 10mL 1mol/L的AlCl3溶液
5.胶体区别于其他分散系的本质特征是:
A.胶体粒子能够发生布朗运动
B.产生丁达尔现象
C.分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在
6.如果把某元素由化合态变为游离态,则它
A.被氧化 B.被还原
C.可能被氧化,也可能被还原 D.由高价态变为零价
7.限用一种试剂即可区别Na2S、Na2S2O3、Na2CO3、NaAlO2、Na2SO4五种溶液。应选用 ( )
A.BaCl2 B.NH3・H2O C.AgNO3 D.HCl
8.下列褪色过程不是因为氧化还原反应而褪色的是 ( )
A.SO2气体通入到溴水中使溴水褪色
B.氯水使滴有酚酞的NaOH溶液褪色,加入NaOH后不变红
C.乙二酸能洗去溅在布条上的蓝墨水
D.在含有碘单质的淀粉溶液中,加入KOH溶液后蓝色褪去
二、选择题(本题包括8小题,每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分)
9.为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确,且最后能得到纯净物质的是 ( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴化钠溶液(NaI) | 氯水、CCl4 | 萃取、分液 |
| B | 氯化铵溶液(FeCl3) | 氢氧化钠溶液 | 过滤 |
| C | 二氧化碳(CO) | 氧化铜粉末 | 通过灼热的CuO粉末 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
10. 要求设计实验证明,某种盐的水解是吸热的,有四位学生分别作出如下回答,其中正确的是
A. 甲学生:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
B. 乙学生:在盐酸中加入相同温度的氨水,若实验过程中混合液温度下降,说明盐类水解是吸热的
C. 丙学生:在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的
D. 丁学生:在醋酸钠溶液中滴入酚酞试液,加热后若红色加深,说明盐类水解是吸热的
11. NA表示阿伏加德罗常数的值,下列说法不正确的是
A.将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积为22.4 L
B.14 g氮气中所含的共用电子对数为1.5NA
C.1 L 1 mol・L-1 FeCl3溶液中,含Fe3+的个数少于NA
D.合成氨反应中,当断裂3NA个H―H共价键的同时生成6NA个N―H共价键,则该反应达到平衡
12.实验室进行NaCl溶液蒸发时,一般有以下操作过程:①固定铁圈位置;②放置酒精灯;③放上蒸发皿;④加热搅拌;⑤停止加热、余热蒸干。其正确操作的顺序是 ( )
A.②①③④⑤ B.①②③④⑤
C.②③①④⑤ D.②③①④⑤
13.下列保存试剂的方法中,错误的是 ( )
A.氢氟酸要保存在塑料瓶中
B.新制的氯水要保存在无色细口瓶中,并放置在光亮处
C.少量液溴要保存在棕色细口橡皮塞瓶中,并在液溴面上加水封
D.单质碘要保存在棕色广口瓶中,并放置在阴凉处
14.氰气的化学式为(CN)2,它的性质和卤素相似,称为拟卤素,对其性质和有关化合物性质的叙述不正确的是 ( )
A.NaCN 和AgCN都易溶于水
B.HCN不易形成白雾
C.MnO2可与HCN反应生成(CN)2
D.(CN)2和NaOH溶液反应生成NaCN、NaCNO 和H2O
 15.浓盐酸和次氯酸钙能发生如下反应Ca(ClO)2+4HCl(浓)=CaCl2+Cl2↑+2H2O,用贮存较久的的漂粉精与浓盐酸反应制得的氯气中,可能含有的杂质为 ( )
15.浓盐酸和次氯酸钙能发生如下反应Ca(ClO)2+4HCl(浓)=CaCl2+Cl2↑+2H2O,用贮存较久的的漂粉精与浓盐酸反应制得的氯气中,可能含有的杂质为 ( )
A.CO2 、HCl 、H2O (g) 三种 B.HCl 、H2O、O2三种
C.只有HCl和H2O(g)二种 D.只有CO2和O2二种
16.已知H2+F2=2HF,2F2+2H2O=4HF+O2,HF+NaOH=NaF十H2O,现若将aLH2和F2的混合气体在暗处发生爆炸性化合反应用足量的NaOH溶液吸收铅制密闭容器中的气体,最后残余同条件下的气体bL,原混合和气体中F2的体积可能是 ( )
A.(a+b)/2L B.(a-b)/2L C.(2a+b)/2L D.(a-2b)/2L
第Ⅱ卷 (非选择题 共68分)
请将选择题答案填入下表
| 题号 |
|
|
|
|
|
|
|
|
| 答案 |
|
|
|
|
|
|
|
|
| 题号 |
|
|
|
|
|
|
|
|
| 答案 |
|
|
|
|
|
|
|
|
三 、实验题。(本大题包括3小题,共25分)
17.(9分)实验室配制250mL 0.5mol・L-1的Na2CO3溶液,有如下操作步骤:①将称量好的Na2CO3固体放入烧杯中,加入适量的蒸馏水溶解;②把①所得溶液小心转入250mL容量瓶中;③继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,小心滴加蒸馏水至溶液凹液面与刻度线相切;④用少量蒸馏水洗涤烧杯2~3次,每次洗涤的液体都小心转入容量瓶中并轻轻摇匀;⑤计算所需Na2CO3固体的质量并用托盘天平称取;⑥塞紧容量瓶的塞子,充分摇匀。回答下列问题:
(1)本实验操作步骤的正确顺序是(填序号) 。
(2)本实验中除用到容量瓶和烧杯外,还需要用到的玻璃仪器有
。
(3)实验中用托盘天平实际称取Na2CO3固体的质量是 g。
(4)在实验中,若出现如下情况,对所配溶液的浓度有何影响?
未进行操作④,所配溶液的浓度会 (填“偏高”、“偏低”或“无影响”,下同);定容时俯视液面,所配溶液的浓度会 。
(5)若实验过程中出现如下情况应如何处理?
加蒸馏水时不慎超过了刻度: ;
向容量瓶中转移溶液时,不慎有少量溶液液洒在容量瓶外面: 。
18(6分).回答下列问题(填序号):
(1)下列仪器中:①漏斗 ②容量瓶 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥量筒
⑦燃烧匙。常用于物质分离的是 ,其中根据物质沸点不同分离物质的仪器是 。
(2)实验室有贮存以下物质的方法:
A. 氯水不宜长期存放,若短期保存需避光;B. 浓硝酸用棕色瓶盛放,贮存在阴凉处。
C. 通常向盛有溴单质的试剂瓶中加入适量的水 D.金属钠常保存在煤油中;
E.NaOH溶液通常用带玻璃塞的磨口试剂瓶保存;
其中正确的是
19(10分).(1)有H2、O2、NO、NH3、NO2五种气体:其中与制取O2 的发生装置相同的是 ;请写出实验室制取该气体的方程式
;
 要得到干燥的该气体可选用
做干燥剂。只能用一种方法收集的是
要得到干燥的该气体可选用
做干燥剂。只能用一种方法收集的是
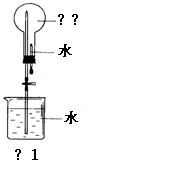
(2)用下图装置进行喷泉实验(图中夹持装置均已略去)。
上部烧瓶已装满干燥氨气,引发水上喷的操作是
,该实验的原理
是
四、填空题(本大题包括3小题,共30分)
20.(12分)在卤素单质中,与H2混合后在暗处就能发生剧烈爆炸的是______,与水剧烈反应并放出O2的是_____,不能将其它卤化物中的卤素置换出来的是______。新制备的氯水显______色,说明氯水中有______分子存在。向氯水中滴入几滴AgNO3溶液,立即有_________生成,说明氯水中有______存在。蓝色石蕊试纸遇到氯水后,首先变红,但很快又褪色,这是因为________________________________。氯水经光照后,颜色逐渐消失,并放出无色的_____气,该反应的化学方程式为__________________。
21.(10分)A是某工厂废旧机械表面上红色固体的主要成分,B、C、F都是单质,D、F都是无色无味的气体,它们之间的相互转化关系如下图:
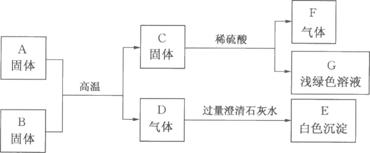
请回答:
(1)写出下列物质的化学式:
C____________,F___________,B__________,G的溶质____________。
(2)写出图中气体D和澄清石灰水反应相应的化学方程式:________________________________
22.(8分)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
![]()
![]()
![]()
![]()
![]()
![]() KClO3+ HCl(浓)= KCl+ ClO2↑+
Cl2↑+ H2O
KClO3+ HCl(浓)= KCl+ ClO2↑+
Cl2↑+ H2O
(1)请配平上述化学方程式(计量数填入框内),单线桥标出电子转移
(2)浓盐酸在反应中显示出来的性质是___________(填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1mol Cl2,则转移的电子的物质的量为________mol。
四、计算题(本大题包括2小题,共13分)
23.(4分)向密度为1.45g・cm-3的硫酸溶液逐滴加入BaCl2溶液,直到反应完全为止,生成沉淀的质量与原硫酸溶液的质量相等,则硫酸溶液中溶质的质量分数为________,物质的量的浓度为___________。
24.(9 分)有两份溶液,其中所含溶质相同,设其摩尔质量为Mg/mol。根据下表信息,回答有关问题:
|
| 溶质的质量分数 | 溶液的密度(g・cm-3) |
| 第一份溶液 | ω1 | ρ1 |
| 第二份溶液 | ω2 | ρ2 |
⑴第一份溶液中,溶质的物质的量浓度为 。
⑵取等质量两份溶液混合,则所得混合液中溶质的质量分数ω3= 。
⑶若有ω1>ω2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为ω4,试比较ω3、ω4的相对大小?