高三化学模拟试题
班级 姓名 号次
一、选择题
1.元素的性质包含金属性和非金属性,其强弱可以通过该元素对应的某些化学性质体现出来。某同学认为铝元素是金属元素,但是有一定的非金属性。下列化学反应中,你认为能支持该同学观点的是 ( )
A.铝片与盐酸反应生成氢气 B.氢氧化铝溶于强碱溶液
C.氢氧化铝溶于强酸溶液 D.铝热反应
2.下列现象不是因为发生化学变化而产生的是 ( )
A.皮肤不慎沾上浓硝酸而呈黄色
B.久置的KI溶液呈黄色
C.盛在无色试剂瓶中的浓硝酸呈黄色
D.食盐撒在燃着液化气的火焰上,火焰呈黄色
3.下列说法中正确的是 ( )
A.同分异构体分子量相同,结构不同,化学性质一定相似
B.可以用新制的Cu(OH)2悬浊液检验患者的尿液中是否含糖
C.向鸡蛋清溶液中加入(NH4)2SO4饱和溶液,有沉淀析出,再加水沉淀不溶解
D.油脂、糖类和蛋白质是食物含有的主要营养物质,他们是高分子化合物
4.下列说法正确的是 ( )
A.NaSO3与BaCl2溶液作用,有白色沉淀生成加稀硝酸后沉淀消失
B.5.6gFe与一定量的稀HNO3反应时失去0.3N A个电子
C.离子化合物中不可能有共价健
D.向淀粉溶液中加入稀硫酸,加热几分钟,再用NaOH溶液中和至中性,滴加碘水溶液不变蓝,说明淀粉水解完了
5.在0.1mol∙L-1的NaHA溶液中有如下关系:c(Na+)>c(HA-)>c(A2-)>c(H2A) 向NaHA溶液中慢慢地加入少量的NaOH溶液时,发生的主要反应的离子方程式为 ( )
A.A2-+H2O![]() HA-+OH- B.HA-+H2O
HA-+OH- B.HA-+H2O![]() H2A+OH-
H2A+OH-
C.HA-+OH-=A2-+H2O D.H2A+OH-=HA-+H2O
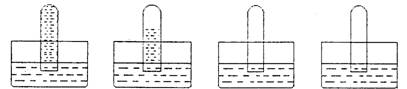
6. 四支试管分别充满O2、NO2、Cl2、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如下图所示,其中充满Cl2的试管是 ( )
|
A盐酸 B水 C饱和食盐水 D水
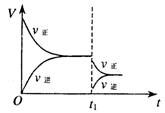
7.
|
|
刻突然变化的条件可能是 ( )
A.催化剂失效 B.减小生成物的浓度
C.降低体系温度 D.增大容器的体积
8..X、Y均为短周期元素,且X为IA族元素,Y为VIA族元素。下列说法正确的是( )
A.X的原子半径一定大于Y的原子半径
B.由X、Y形成的共价化合物中所有原子都满足最外层为8电子结构
C.X2Y既可能是离子化合物,也可能是共价化合物
D.由X、Y组成的化合物中,X、Y的原子个数比不可能是1:1
9.将0.1mol含水晶体aR•bH2O在一定温度下加热一段时间后冷却,称得固体质量减少2.7g,同时生成0.05mol含水晶体bR•aH2O,则(a+b)的值为 ( )
A.6 B.5 C.4 D.3
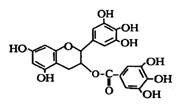 10.美国梅奥诊所的研究人员发现,绿茶中含有EGCG(表没食子儿茶素没食子酸酯)物质具有抗癌作用,能使血癌(白血病)中癌细胞自杀性死亡,已知EGCG的结构如右图所示,有关EGCG的说法中不正确的是( )
10.美国梅奥诊所的研究人员发现,绿茶中含有EGCG(表没食子儿茶素没食子酸酯)物质具有抗癌作用,能使血癌(白血病)中癌细胞自杀性死亡,已知EGCG的结构如右图所示,有关EGCG的说法中不正确的是( )
① EGCG能与碳酸钠溶液反应放出二氧化碳
② EGCG遇FeCl3溶液能发生显色反应
③ 1molEGCG最多可与含10mol氢氧化钠溶液完全作用
④ EGCG在空气中易氧化
A.①② B.①③ C.②④ D.③④
二、填空题
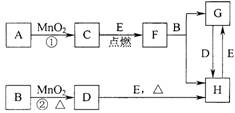 11.下图所涉及的物质均为中学化学中的常见物质,其中C和D为非金属单质、E为金属单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
11.下图所涉及的物质均为中学化学中的常见物质,其中C和D为非金属单质、E为金属单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
(1)写出有关物质的名称或化学式:
F ,H 。
(2)指出MnO2在相关反应中的作用:反应①中是 剂,反应②中是 剂。
(3)若反应①是在加热条件下进行,则A是 ;若反应①是在常温条件下进行,则A是 。写出F、D在固态时的所属晶体类型F为: :D为 。
(4)写出F与B反应的离子方程式 。
12.下图是部分短周期元素的单质熔点的变化图,根据此图,填写下列空格:
(1)③号元素位于周期表第__________周期_______族,其单质的一种同素异形体能导电,该同素异形体的名称叫______________。
(2)⑤、⑥两种元素形成的最高价氧化物对应的水化物之间相互反应的离子方程式为______________。
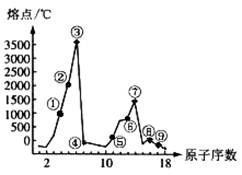 (3)⑦号元素的原子结构简图为___________。
(3)⑦号元素的原子结构简图为___________。
(4)②、④两元素形成的化合物其晶体有两种结构,其中一种结构与金刚石相似,该结构的晶体属___________晶体,若使其熔化,需破坏的作用力为___________________。
13.已知:CH2=CH2+HOCl![]() HOCH2CH2Cl
HOCH2CH2Cl
HCHO+CH3COOH![]() H
H![]() -CH2
-CH2![]() ―OH
―OH
杨梅酯是制作冰制食品、糖果等的香料,可用A、E两种烃为原料,经如下路线合成
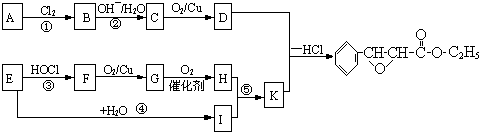
试回答下列问题:
(1)写出结构简式:D ,B ,I ________________。
(2)上述属于取代反应的有 (选填序号)
(3)写出反应⑤的化学方程式: 。
14.某学习兴趣小组取当地黏土土样进行如下实验。
(1)分析土样中铝铁含量:
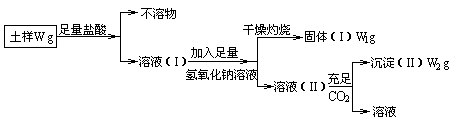
①在上述过程中反复用到的一个分离操作是_________,该操作用到的仪器有_________。
②样品中铁元素含量的数学表达式为_______________________,此结果可能比实际的铁含量____________________(填“高”或“低”),理由是________________________。
③写出上述溶液(II)中得到沉淀(II)的离子方程式__________________________。
(2)秦砖汉瓦色泽经千年而不变,是我国劳动人民智慧的结晶,该兴趣小组利用土样烧制青色和红色的砖瓦。
乙装置在烧制快结束时要通入水蒸气,并且密闭冷却。
①在上述装置中,成品为红色的是_______________________。
②现在工业上大都是烧制红色砖瓦,较少烧制青色砖瓦,你认为可能的原因是什么?________________________________。