高三化学补习班诊前模拟试题一
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 P-31 S-32 Si-28 Na-23 Cl-35.5
第Ⅰ卷(选择题 共48分)
一、单项选择题(本题包括16小题,每小题3分,共48。每小题只有一个选项符合题意)
1.某一密闭绝热容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末,下列说法正确的是
①有晶体析出 ②c[Ca(OH)2]增大 ③pH不变 ④c(H+)c(OH-)的积不变 ⑤c(H+)一定增大
A ① B ①③ C ①②④ D ①⑤
2.SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02mg/L,下列措施中能够减少SO2排放量的是 ①用天然气代替煤炭做民用燃料 ②使用水煤气或干馏煤气做燃料 ③硫酸厂使用V2O5作催化剂,加快SO2的转化速率 ④将块状煤粉碎,提高其燃烧效率 ⑤在煤中加入石灰后燃用 ⑥循环处理吸收塔放出的尾气
A.①②③④⑤ B.①③⑤⑥ C.①②⑤⑥ D.②③④⑥
![]() 3.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ根据以上信息和数据,下列说法正确的是
3.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ根据以上信息和数据,下列说法正确的是
A.N4属于一种新型的化合物 B.N4与N2互为同素异形体
C.N4沸点比P4(白磷)高 D.1mo1N4气体转变为N2将吸收882kJ热量
4.下列实验操作或事故处理中,正确的做法是
A.银镜反应实验后附有银的试管,可用稀H2SO4清洗
B.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次
C.不慎将浓H2SO4沾在皮肤上,立即用NaOH溶液冲洗
D.在250mL烧杯中,加入216mL水和24g NaOH固体,配制10% NaOH溶液
5.下列物质能通过化合反应直接制得的是
①FeCl2 ②H2SO4 ③NH4NO3 ④HCl
A.只有①②③ B.只有②③ C. 只有①③④ D.全部
6.下列说法正确的是
A.H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体;
甲醇、乙二醇和丙三醇互为同系物
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.HI的相对分子质量大于HF,所以HI的沸点高于HF
D.由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有
共价键的离子型化合物
7. 干燥剂的干燥性能可用干燥效率(1m3空气中实际余留水蒸气的质量)来衡量。某些干燥剂的干燥效率数据如下:
| 物质 | 干燥效率 | 物质 | 干燥效率 |
| MgO | 0.008 | ZnCl2 | 0.8 |
| CaO | 0.2 | ZnBr2 | 1.1 |
分析以上数据,下列有关叙述错误的是
A.MgO的干燥性能比CaO好
B.干燥效率可能与干燥剂的阴、阳离子的半径大小有关
C.MgCl2可能是比CaCl2更好的干燥剂
D.上述干燥剂中阳离子对干燥性能的影响比阴离子小
8.某研究性学习小组为了探索镁粉与溴水反应的机理,做了如下四组实验:
①将镁粉投入冷水中,未见任何现象;
②将镁粉放入溴水中,观察到只是开始时产生极少量的气泡,但溴水的颜色逐渐褪去;
③将镁粉放入液溴中,未观察到任何明显现象;
④向含足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去。
则下列关于镁与溴水的反应机理的论述中正确的是
A.镁粉只直接与溴水中的溴反应
B.镁粉只与溴水中的酸反应
C.产生极少量的气泡是由于镁粉与水反应得到
D.镁粉在水的催化下与溴发生反应
9.为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加Ag NO3溶液,产生白色沉淀。
根据实验以下推测正确的是
A.一定有SO32-离子 B.一定有CO32-离子
C.能确定C1―离子存在 D.不能确定HCO3-离子是否存在
10.化合物A、B、C、D各由两种元素组成,甲、乙、丙是三种单质。这些常见的化合物与单
质之间存在如下关系(已知化合物C是一种有机物),
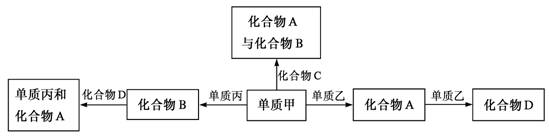
以下结论不正确的是
A.上图所示的五个转化关系中,有三个是化合反应
B.上述转化关系所涉及的化合物中有一种是电解质
C.甲、乙、丙三种单质的晶体可依次是分子晶体、原子晶体、分子晶体
D.上图所示的五个转化关系中,均为放热反应
11.在加入铝粉能放出H2的溶液中,可能大量共存的是
A.NH4+、NO3-、CO32-、Na+ B.Na+、Ba2+、Mg2+、HCO3-
C.NO3-、K+、SO42-、Cl- D.NO3-、Na+、Fe2+、K+
12.下列离子方程式中正确的是:
A.氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O
B.Fe3+的检验:Fe3++3SCN-=Fe(SCN)3↓
C.向碳酸氢钙溶液中加入过量氢氧化钠
Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
D.Na2S溶液呈碱性:S2-+H2O=HS-+OH-
13.NA为阿伏加德罗常数,下述叙述中正确的是:
A.60g SiO2与足量纯碱反应,高温下最多可释放出NA个气体分子
B.31g白磷含有NA个共价键
C.标准状况下,11.2L四氯化碳所含分子数为0.5 NA
D.58.5g氯化钠中含有6.02×1023个氯化钠分子
14. 若原子序数为 116 号元素, 其元素最外层电子数为 6, 则下列叙述不正确的是:
A. X 是金属元素 B. X的钠盐的化学式为: Na2X
C. X的最高价氧化物的化学式为: XO3 D. X的最高价氧化物的水化物是碱
15.下列对实验仪器名称的标注或实验操作,正确的是
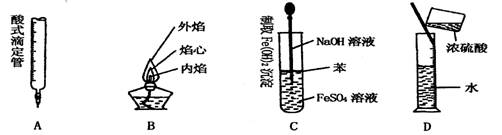
16.下列物质性质的变化规律与分子间作用力有关的是
A.F2、Cl2、Br2、I2的熔、沸点逐渐升高
B.金刚石的硬度大于硅,其熔、沸点也高于硅
C.NaF、NaCl、NaBr、NaI的熔点依次降低
D.HF、HCl、HBr、HI的热稳定性依次减弱
化学模拟试题一
姓名 班级
第Ⅰ卷(选择题 共48分)答题卡
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷非选择题(共52分)
17.(13分) 在足量的稀氯化亚铁溶液中,加入1~2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是:
(填粒子的化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物
是
(2)现提供以下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
请判断哪位同学的推断是正确的,并用两种方法加以验证,写出选用的试剂编号
及实验中观察到的现象。
| 同学正确 | 选用试剂 | 实验现象 |
| 第一种方法 | ||
| 第二种方法 |
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子
是 若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,
你认为是否可行? (填可行或不可行)
理由是:
18.( 9分)
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
| |
| |
19.(14分)硼酸晶体呈片状,有滑腻感,可作润滑剂,硼酸对人体的受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。试回答下列问题:
(1)从题目信息可知硼酸应属于 酸(弱、强、中强)
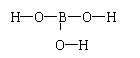
(2)硼酸的分子式为H3BO3,已知H与O成键,则其分子结构式为: 。
(3)研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外层具有达到8电子稳定结构的趋向。已知0.01mol硼酸可以被20mL 0.5mol・L -1NaOH溶液恰好完全中和,据此推测硼酸在水溶液中呈酸性的原因是
(用离子方程式表示)
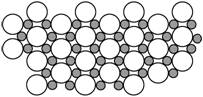 (4)科学家发现硼化镁在39 K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列,右图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。
(4)科学家发现硼化镁在39 K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列,右图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。
根据右图确定硼化镁的化学式为
(5)硼烷(B2H6)气体在空气中能剧烈燃烧生成固态氧化物,已知每生成1mol液态水可
放出722kJ的热量,请写热化学方程式:
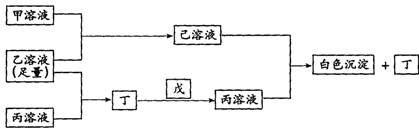 |
20、(11分) 有A、B、C三种常见的短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素最外层电子数比B多一个。甲、乙、丙是3种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液pH<7;丁为气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如上图。请回答:
(1)写出C元素的原子结构示意图__________,写出丁和戊的电子式__________、__________;
(2)用有关化学用语解释:乙溶液呈酸性的原因______________________________;
丙溶液呈碱性的原因_____________________________;
(3)写出有关反应的离子方程式:
①乙溶液+丙溶液→丁______ ________________________;
②己溶液+丙溶液→丁_________ _____________________。
21.(11分)往200mL NaOH溶液中通入CO2,充分反应后,在减压和低温下,小心将溶液蒸干,得白色固体M。通入CO2的体积V(CO2) (mL)(标准状况下)与M的质量(g)的关系如图。试通过分析和计算回答下列问题(要求写出简要计算过程):
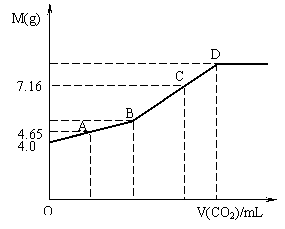

⑴ B点时,白色固体M的化学式_________,通入CO2的体积为______________mL。
⑵ D点时,通入CO2的体积为__________mL。
⑶ C点时,通入CO2的体积为__________mL。
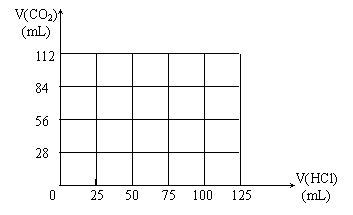 ⑷ 取组成为A点的白色固体
⑷ 取组成为A点的白色固体![]() ,向其中逐滴加入0.1mol/LHCl溶液,请在下图中画出产生CO2气体体积(标准状况下)与所加入的盐酸的体积关系:
,向其中逐滴加入0.1mol/LHCl溶液,请在下图中画出产生CO2气体体积(标准状况下)与所加入的盐酸的体积关系:
化学模拟试题一
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | D | C | B | B | D | D | D | D |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | B | D | C | C | A | B | C | A |
17.(13分)
(1)Br2 (2分);Fe3+ (2分)
(2)
| 乙 (1分) 同学正确 | 选用试剂 | 实验现象 |
| 第一种方法 | C(1分) | 有机层无色(1分) |
| 第二种方法 | D(1分) | 溶液变红(1分) |
(3)Fe2+(2分);不可以(1分),因为Br2和Fe3+都能把I―氧化成I2(1分)
18.(本题共8分)
(1) FeSO4+HNO3→Fe(NO3)3+Fe2(SO4)3+N2O+H2O(2分)
(2) FeSO4 (1分) +5价N (1分) (3) 得到(1分) 4(1分)
(4)24FeSO4+30HNO3→ (2分)
 19. (本题共10分,每空2分)
19. (本题共10分,每空2分)
(1)弱
(2)
(3)B(OH)3+H2O![]() [B(OH)4]―+H+
(4)MgB2;
[B(OH)4]―+H+
(4)MgB2;
(5)B2H6(g)+3O2(g) = B2O3(s)
+ 3H2O(l);![]() H= - 2166kJ・mol-1
H= - 2166kJ・mol-1
20、(本题11分,第(1)题每空1分,其余每空2分)
(1)
硫原子结构示意图略
, ![]() ::C::
::C::![]() , Na+[:
, Na+[:![]() :
:![]() :]2-Na+
:]2-Na+
(2) NaHSO4= Na++H++SO42-, CO32-+H2O=HCO3-+OH-(只用文字叙述,不写方程式不给分)
(3) ①2H++CO32-= CO2↑+H2O;②2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
21.(10分)
⑴Na2CO3,(2分) 1120;(2分) ⑵2240;(2分) ⑶1792mL(2分)
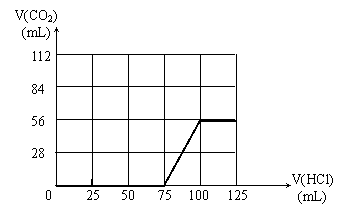
⑷(2分)